10 Aineen lämpeneminen ja jäähtyminen
FY03 Energia ja lämpö
Pohdi kaverin kanssa
50-asteista vettä yhdistetään yhtä suureen määrään 20-asteista vettä. Kuinka suuri on veden loppulämpötila?
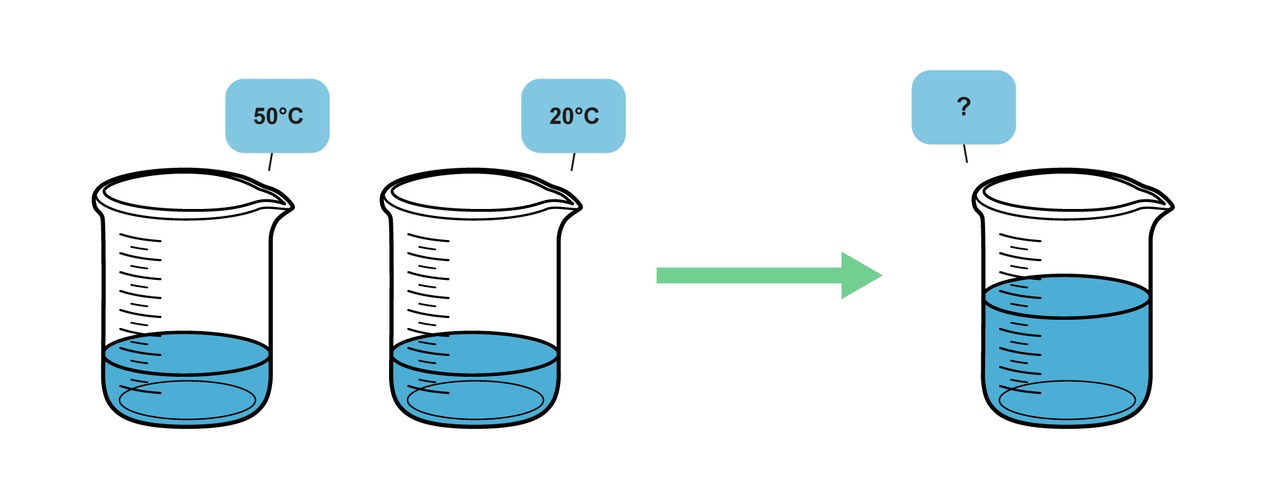
Kuva: Resonanssi 3 (e-Oppi)
Pohdi kaverin kanssa
300 grammaa 50-asteista vettä yhdistetään 600 grammaan 20-asteista vettä. Kuinka suuri on veden loppulämpötila?
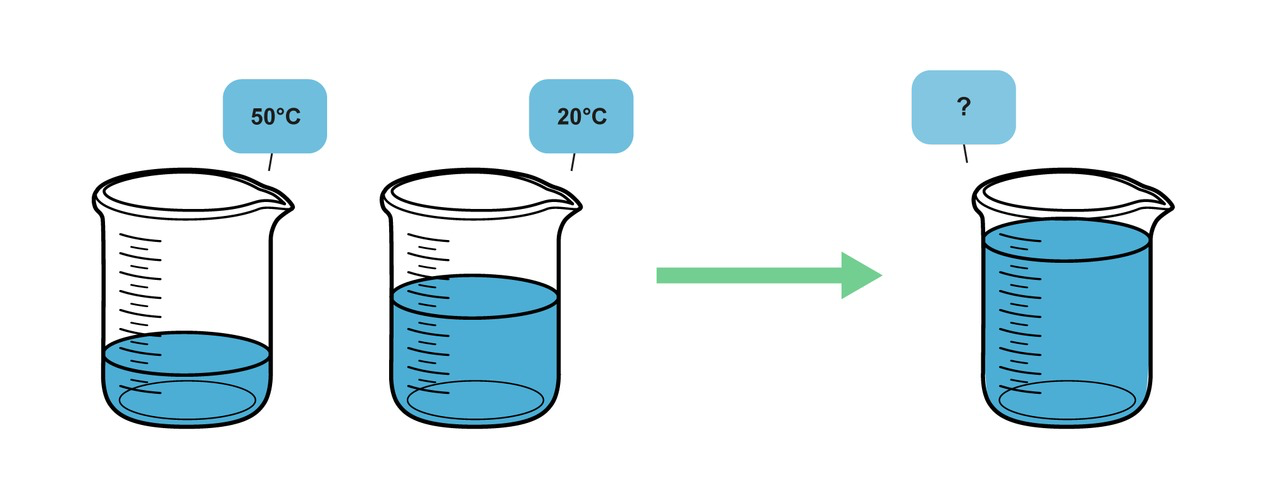
Kuva: Resonanssi 3 (e-Oppi)
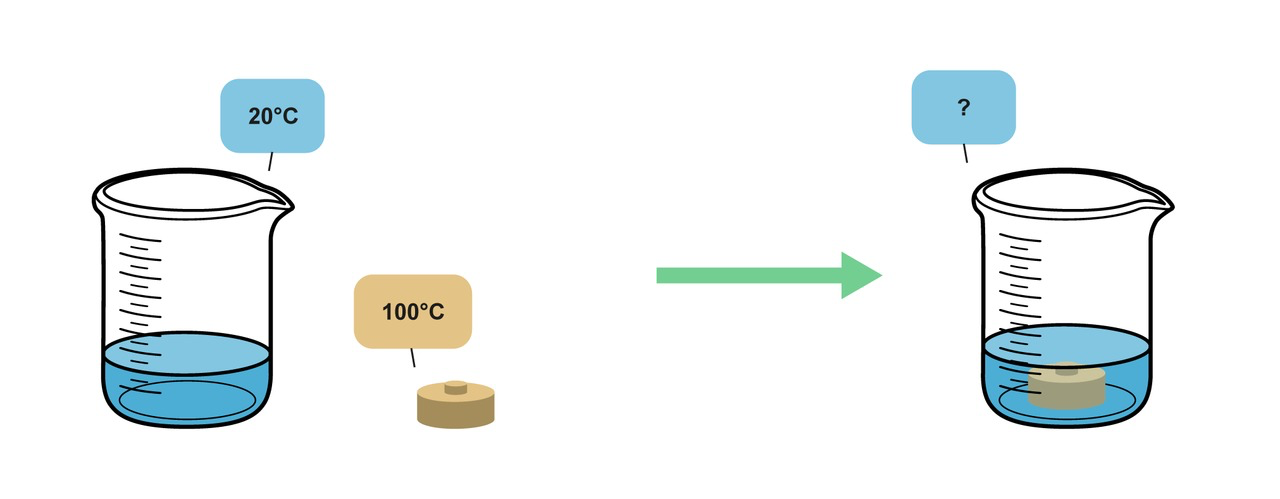
Pohdi kaverin kanssa
300 g messinkipunnus, joka lämpötila on 100 °C, upotetaan 300 grammaan 20-asteista vettä. Kuinka suuri on veden ja punnuksen yhteinen loppulämpötila?
Kuva: Resonanssi 3 (e-Oppi)
Kuuman messingin luovuttama lämpö on yhtä suuri kuin kylmän veden vastaanottama lämpö.
Ratkaistaan yhtälö CAS-laskimella.
Veden ja messingin loppulämpötilaksi saadaan


Sijoitetaan arvot ja ratkaistaan yhtälö uudestaan.
Kaavaeditorilla:
Lämpö on siirtyvää energiaa
- Lämpötilaerot pyrkivät luonnostaan tasoittumaan (termodynaaminen tasapaino)
- Kuumasta kappaleesta siirtyy energiaa kylmempään
- Kuuman kappaleen lämpötila laskee ja kylmemmän nousee
- Siirtyvää lämpöenergiaa kutsutaan lämmöksi ja merkitään tunnuksella Q
- Myös olomuodon muutoksissa aine luovuttaa tai vastaanottaa lämpöä
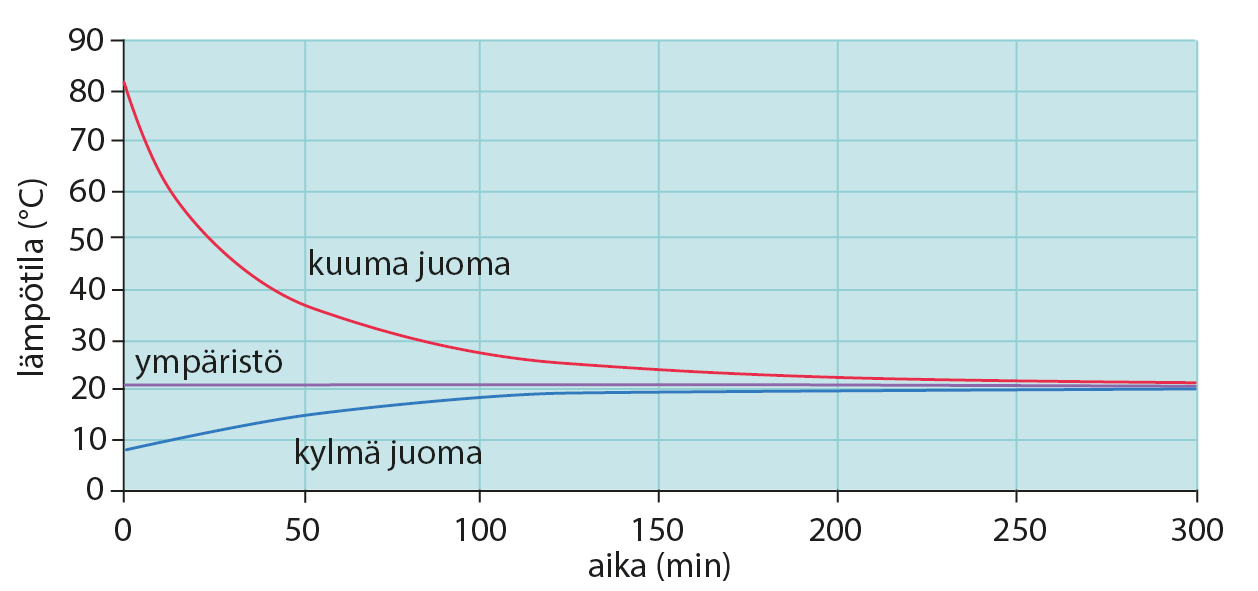
Kuva: Vipu 3 (Otava)
Lämpö- ja ominaislämpökapasiteetti
- Kappaleen lämpötilan nousu 1 °C:n (tai 1 K:n) verran vaatii aina saman määrän lämpöä Q
- Lämpenemiseen vaadittavaa energiaa eli kappaleen kykyä varastoida lämpöä kuvaa kappaleen lämpökapasiteetti C
- Kappaleen lämmetessä lämpötilan ΔT siirtyy siihen lämpö
- Suuri lämpökapasiteetti kappale voi varastoida paljon lämpöä
- Lämpenee tai jäähtyy hitaasti
- Lämpökapasiteetti C riippuu kappaleen massasta ja materiaalista, josta se koostuu
- Ominaislämpökapasiteetti c kuvaa aineen kykyä varastoida lämpöä
Energia lämpötilan muuttuessa
- Kun aineen lämpötila muuttuu, aine vastaanottaa tai luovuttaa energiaa
- Siirtynyt energia ilmenee aineen sisäenergian muutoksena
- Aineen lämmetessä siirtyy siihen lämpö
- Aineen jäähtyessä se luovuttaa vastaavan määrän energiaa
Teho ja energia
- Teho kuvaa energian siirtymis- tai muuntumisnopeutta
- Jos esim. sähköverkkoon kytketyllä laitteella lämmitetään ainetta, on laitteen lämmitysteho
- Vesi sitoo energiaa hyvin eli sen ominaislämpökapasiteetti on varsin suuri
- Lämpenee ja jäähtyy hitaasti (vakioteholla t ~ c)
Lämpölaskujen periaatteita
- Eristettyä systeemiä voidaan kuvata yhtälöllä
- Siirtyvää lämpöä laskettaessa lämpötilan muutos ΔT lasketaan alkulämpötilan T1 ja loppulämpötilan T2 erotuksena
-
Suuremmasta lämpötilan arvosta vähennetään pienempi, jolloin lämpötilan muutos tai on aina positiivinen
- Siirtyvät lämmöt Q ovat näin ollen aina suuruudeltaan positiivisia
-
Laskuissa käytetään lämpötilan yksikkönä ensisijaisesti celsiusasteita
- Lämpötilan muutos on yhtä suuri kelvineinä
- Merkitse ominaislämpökapasiteetin yksikkö lämpötilan yksikön perusteella!
Esimerkki 1
Laboratoriossa tutkittiin kuparin kykyä sitoa energiaa.
Kuparikappale, jonka massa oli 179 g, kuumennettiin kiehuvassa vedessä 100 °C:n lämpötilaan. Tämän jälkeen kappale upotettiin nopeasti kalorimetriastiassa olevaan veteen, jonka lämpötila oli 18 °C ja massa 179 g. Veden lämpötila nousi 24 °C:seen.
Määritä mittauksen perusteella kuparin ominaislämpökapasiteetti. Oleta, että kalorimetri ei lämpene.
Oletetaan, että kalorimetriastia on eristetty systeemi. Tällöin kuparikappaleen luovuttama energia on yhtä suuri kuin veden vastaanottama energia.
MAOL-taulukoiden mukaan kuparin ominaislämpökapasiteetti on 0,387 kJ/(kg °C).
Esimerkki 2
1,3 litraa 45-asteista ja 2,5 litraa 82-asteista vettä sekoitetaan toisiinsa. Mikä on vesiseoksen loppulämpötila? Lämmönvaihto ympäristön kanssa oletetaan mitättömäksi.
Tällöin kuuman veden luovuttama lämpö on yhtä suuri kuin kylmän veden vastaanottama lämpö.
Lämmönvaihto ympäristön kanssa on mitätöntä, joten voidaan olettaa systeemi eristetyksi.
Yhtälön ratkaisu TI-Nspirella

Jos ratkaiset yhtälöt laskimella, kirjoita alkuperäinen yhtälö, tuntemattoman suhteen ratkaistu lauseke, sijoitus (tai vähintään lähtöarvojen listaus) sekä vastaus selkeästi kaavaeditorilla! Kuvakaappaus laskimesta ei riitä!
Yhtälön ratkaisu: solve(yhtälö, muuttuja)
Lukuarvon sijoitus :=
Poistaminen muistista: Delvar
Yksikkö alaviivalla _
10 Aineen lämpeneminen ja jäähtyminen
By pauliinak
10 Aineen lämpeneminen ja jäähtyminen
FY03 Lämpö ja energia
- 143



