11 Energia olomuodon muutoksissa
FY03 Energia ja lämpö
Pohdi kaverin kanssa
- Jos jätät avoimen astian pohjalle vähän vettä, miksi astia on jonkin ajan kuluttua tyhjä? Miksi näin ei käy, kun astia on tiiviisti suljettu?
- Mitä veden lämpötilalle tapahtuu, kun se saavuttaa kiehumispisteensä? Miksi?
- Miksi lämpimän suihkun jälkeen tulee äkkiä kylmä?
- Miksi ukkoskuuron aikana ilman lämpötila laskee?
- Miksi pyykit voi kuivata ulkona pakkasella?
- Miksi pakastimeen kertyy jäätä?



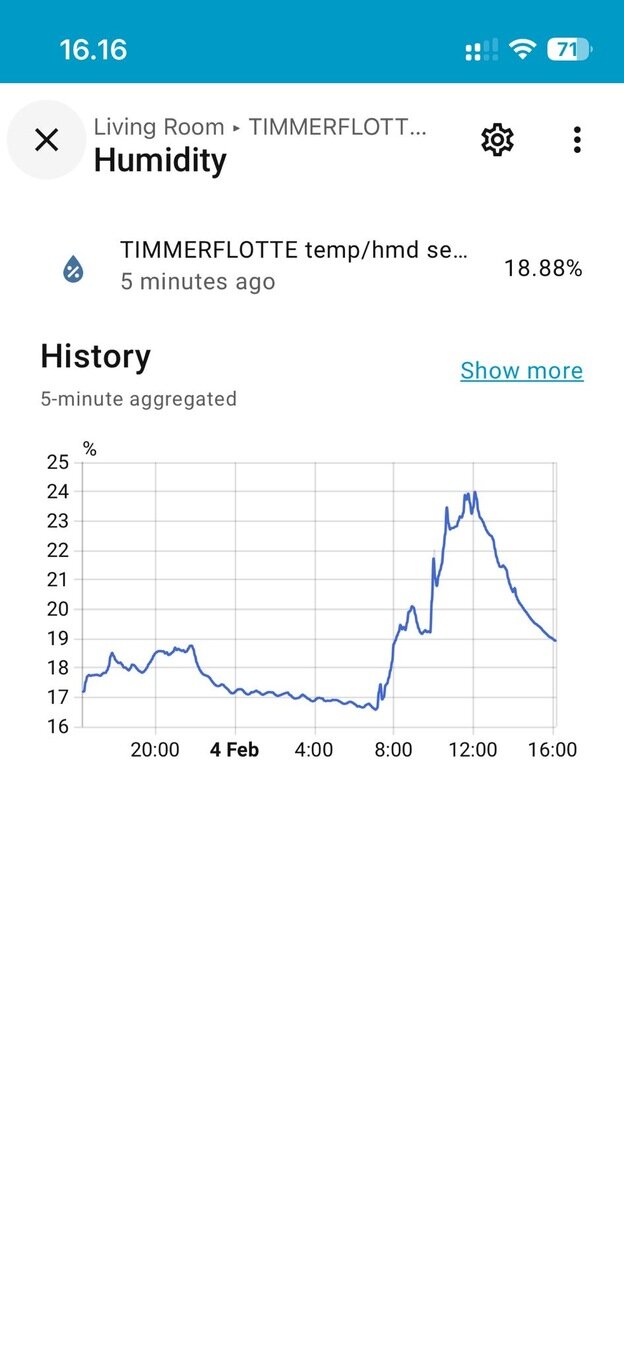
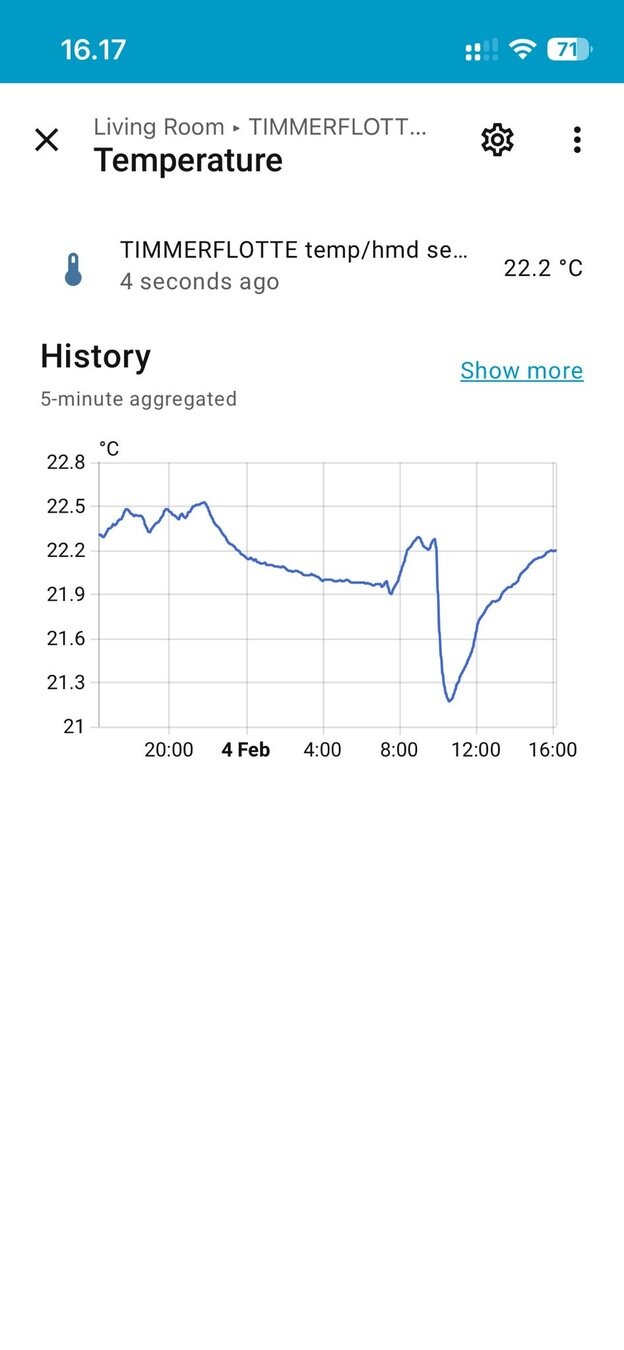
Mitä tapahtuu noin klo 10–12?
Aineen olomuodot ja niiden muutokset
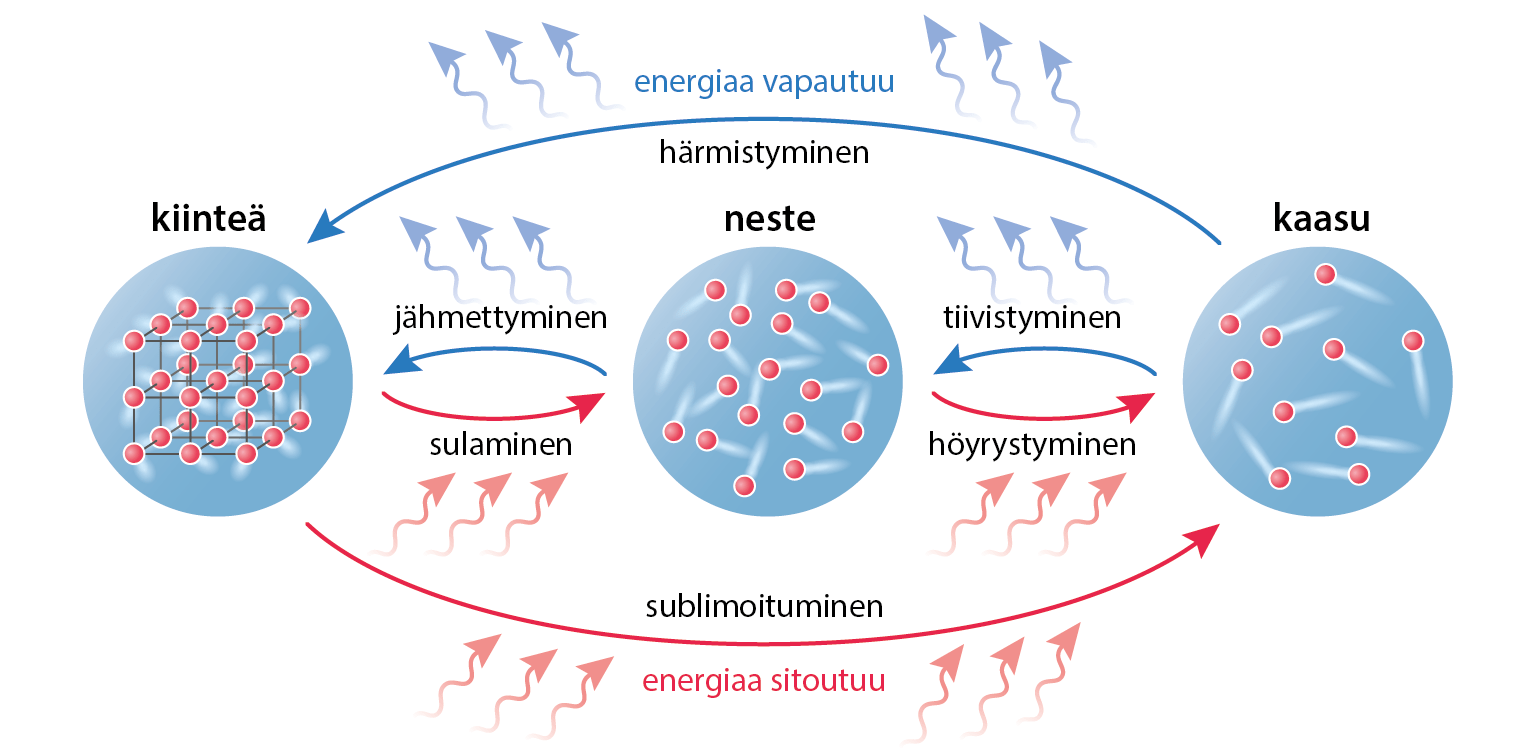
Kuva: Vipu 3 (Otava)
Aineen rakenne eri olomuodoissa
- Mikrotasolla aineen olomuotomuutokset selittyvät muutoksilla rakenneosasten välisissä sidoksissa
- Kiinteä aine muodostaa sidosten avulla hilarakenteen
- Aineen sulaessa sidoksia hajoaa
- Sidokset pitävät nestettä koossa
- Nesteen kiehuessa sidokset hajoavat
- Kaasun molekyylit eivät vuorovaikuta keskenään (ideaalikaasu)
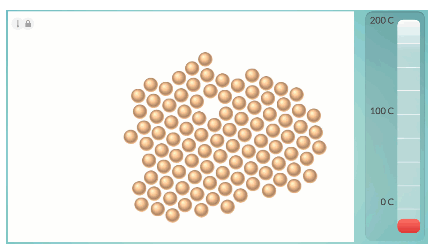
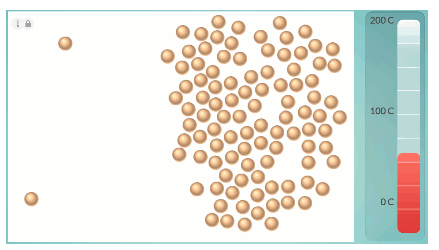
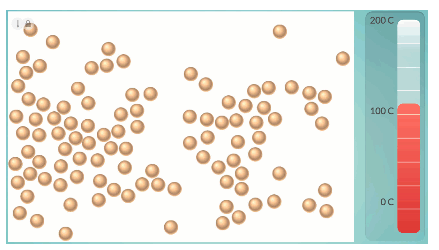
Kuvat: Resonanssi 3 (e-Oppi)
Olomuodon muutokset
- Aineeseen siirtyvä energia aiheuttaa joko aineen lämpenemistä tai olomuodon muutoksen
- Olomuodon muutoksissa aine vastaanottaa tai luovuttaa energiaa
- Sulamiseen tai höyrystymiseen vaadittu energia riippuu aineesta
- Olomuodon muutoksen aikana aineen lämpötila ei muutu
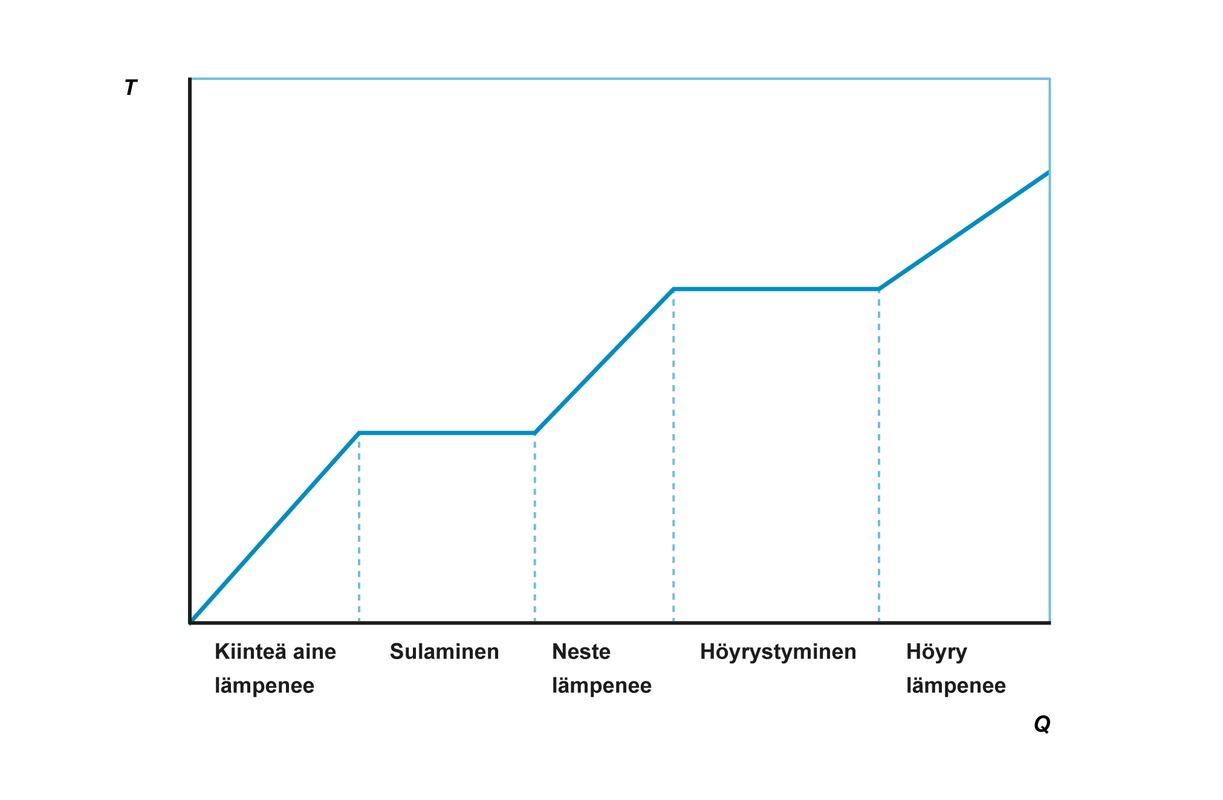
T = vakio
Energia
Lämpötila
Kuva: Resonanssi 3 (e-Oppi)
Sulamispiste
Kiehumispiste
Energia olomuodon muutoksissa
- Sulaessaan aine vastaanottaa ympäristöltään lämmön
- Jähmettyessään aine luovuttaa ympäristöön vastaavan lämmön
- Höyrystyessään aine vastaanottaa ympäristöltään lämmön
- Tiivistyessään aine luovuttaa ympäristöön vastaavan lämmön

Suorilla eri kulmakertoimet: kiinteällä aineella, nesteellä ja kaasulla eri ominaislämpökapasiteetit!
Kuva: Resonanssi 3 (e-Oppi)
Esimerkki 1
Kuinka paljon lämpöenergiaa tarvitaan muuttamaan 3,0 kg jäätä, jonka lämpötila on –15 °C, vesihöyryksi, jonka lämpötila on 120 °C?
Vesihöyryn ominaislämpökapasiteetti vakiopaineessa on

Oletetaan, että kyseessä on eristetty systeemi. Tällöin jäälle luovutettu energia on yhtä suuri kuin vastaanotettu energia.
Vastaanotettu energia menee seuraaviin prosesseihin:
- Jää lämpenee
- Jää sulaa
- Nestemäinen vesi lämpenee
- Vesi höyrystyy
- Vesihöyry lämpenee
Lasketaan siis jokaiseen prosessiin tarvittava energia ja lopulta niiden summa.
Jään lämmitys –15 °C 0 °C:
Jään sulatus 0 °C:
Veden lämmitys 0 °C 100 °C:
Veden höyrystys 100 °C:
Höyryn lämmitys 100 °C 120 °C:
Tarvittava lämpöenergia yhteensä:
Lämpölaskujen kirjoittaminen
- Kun olomuodonmuutokset huomioidaan lämpölaskuissa, on periaate sama kuin aiemmin
- Eristettyä systeemiä kuvataan edelleen yhtälöllä
- Huomioi olomuodonmuutoksiin liittyvät termit yhtälössä sen mukaan, sitoutuuko vai vapautuuko muutoksessa energiaa
- Esim. pakastimesta otetun jään lämmittäminen ja sulattaminen lämpimällä vedellä
- Lämmin vesi luovuttaa energiaa, kylmä jää vastaanottaa
- Tässä oletus, että loppulämpötila on nollan yläpuolella
Esimerkki 2
Kirjoita lämmön siirtymiseen liittyvät yhtälöt seuraavista tilanteista:
- Pakastimesta otettu jäinen keitto sulatetaan sähköliedellä.
- Kaasupolttimella lämmitetään 0-asteista lunta siten, että se höyrystyy.
- Jääkaapista otettuun virvoitusjuomaan lisätään jäitä.
Mieti, mikä luovuttaa energiaa ja mikä vastaanottaa energiaa.
Kirjoita niiden välille yhtälö, jossa luovutettu lämpö on yhtä suuri kuin vastaanotettu lämpö.
Kirjoita lopuksi kunkin lämpömäärän termi auki käyttäen sopivaa kaavaa.
Esimerkki 3
Jään ominaissulamislämpö haluttiin selvittää sulattamalla lunta. 104 g lunta tiputettiin kalorimetriin, jossa oli 214 g lämmintä vettä.
Lumen lämpötila alussa oli 0,0 °C ja lämpimän veden lämpötila alussa oli 45,5 °C. Sulaneen vesiseoksen loppulämpötilaksi mitattiin 5,8 °C.
Määritä mittausten perusteella lumen (jään) ominaissulamislämpö. Oletetaan, että kalorimetrin lämpötila ei muutu.
Lumi ja vesi sekoitetaan kalorimetrissä, joten oletetaan systeemi eristetyksi. Lämmin vesi luovuttaa energiaa, jonka lumi vastaanottaa. Energia menee lumen sulamiseen ja sulamisveden lämmittämiseen.
MAOL-taulukoiden mukaan jään ominaissulamislämpö on 333 kJ/kg. Virheen suuruus on noin 4,4 %.
Virhettä tulee lumen massan ja lämpötilan mittauksessa, sillä lumi lämpenee ja sulaa nopeasti, kun se tuodaan sisään. Myös kalorimetrin lämpötila muuttuu hieman.
Huom! Jos lumen lämpötila olisi pakkasen puolella, pitäisi myös lumen lämmittäminen huomioida yhtälössä.
Tällöin yhtälö olisi muodossa
Huomaa, että jään ja veden ominaislämpökapasiteetit ovat erisuuret! Jää ja vesi pitää täten käsitellä yhtälössä omina termeinään.
11 Energia olomuodon muutoksissa
By pauliinak
11 Energia olomuodon muutoksissa
FY03 Energia ja lämpö
- 121



