2.1/2.2 Atomi ja sen spektrin synty, monielektroniatomit
FY08 Aine, säteily ja kvantittuminen
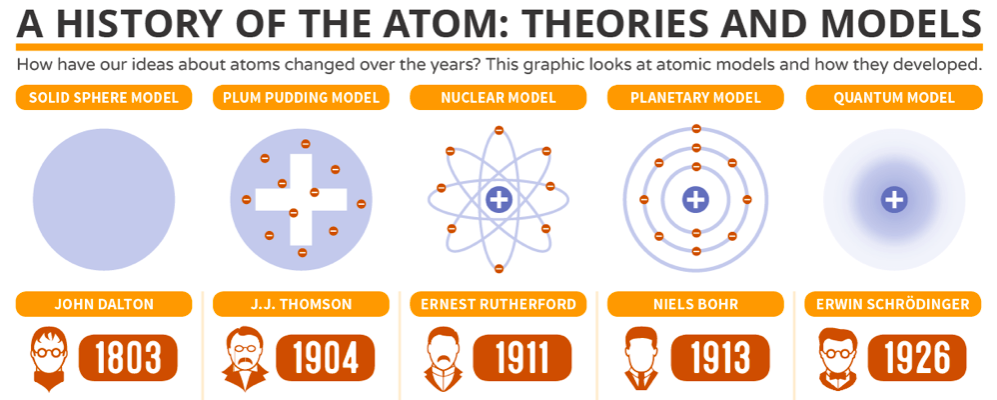
Kuva: CompoundChem
- Käsitys atomin rakenteesta kehittyi vauhdilla 1900-luvun alussa
- Uudet kokeelliset havainnot selitettiin erilaisilla malleilla
Atomimallin kehitys
Varhaiset atomimallit
- Demokritoksen atomimalli (Antiikin Kreikka n. 400 eaa.)
- Demokritos ajatteli aineen koostuvan pienistä jakamattomista osista
- Ei empiirisiä todisteita atomien puolesta
- Molekyylit koostuvat atomeista
- John Dalton havaitsi, että kemialliset yhdisteet koostuvat samoista alkuaineista
- Yhdisteessä alkuaineiden massojen suhde on aina sama
- Alkuaine koostuu siis atomeista


Kuva: CompoundChem

Kuvat: Wikipedia CC0
Joseph John Thomsonin atomimalli
- Thomson havaitsi anodin ja katodin välillä hiukkasten siirtymistä (katodisäteet)
- Hiukkaset nimettiin elektroneiksi (1897)
- Hiukkasilla oltava sähkövaraus, koska niiden rata muuttui magneettikentässä
- Hiukkasille laskettiin varauksen e ja massan m suhde e/m
- Elektronin massa on vain 1/2000 vedyn massasta

- Thomson päätteli löydettyjen hiukkasten olevan sähköisesti neutraalin atomin osa
- Elektronit sijaitsevat Thomsonin atomin sisällä kuin rusinat pullassa ("rusinapullamalli")
Kuva: CompoundChem
Ernest Rutherfordin atomimalli
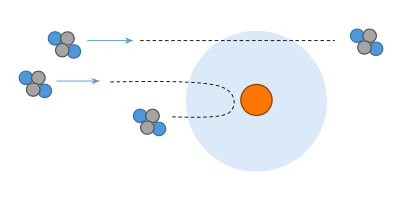
- Rutherfordin sirontakokeessa kultakalvoa pommitettiin heliumytimillä (alfahiukkanen)
- Suuri osa hiukkasista kulki kalvon läpi lähes suuntaansa muuttamatta
- Hyvin pieni osa sirosi takaisin

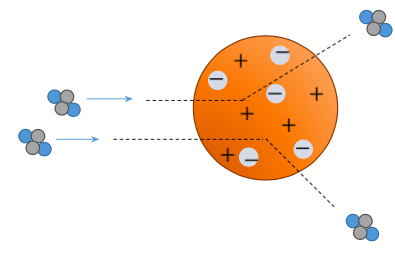
- Havainto ei tukenut Thomsonin atomimallia, josta hiukkasten pitäisi sirota satunnaisesti eri suuntiin
- Havainnot selitettiin mallilla, jossa lähes koko atomin massa on sen keskuksessa atomiytimessä
- Ytimen ympärillä oleva elektroniverho määrää atomin koon
Kuva: CompoundChem
Rutherfordin mallin puutteet
- Ytimen koostuminen protoneista ja neutroneista ymmärrettiin vasta vuonna 1932 (Rutherford & Chadwick)
- Mallin ongelma:
- Elektronien liike on kiihtyvää, joten niiden tulisi lähettää sähkömagneettista säteilyä
- Tällöin elektronit menettävät energiaa ja syöksyisivät lopulta ytimeen

Kuva: CompoundChem
Niels Bohrin atomimalli
- Niels Bohr yhdisti kvantittumisen idean Rutherfordin malliin
- Rutherfordin kokeen tulokset ja vedyn spektristä tehdyt havainnot
- Bohrin mallissa vain tietyt kiinteät elektronien radat ovat mahdollisia
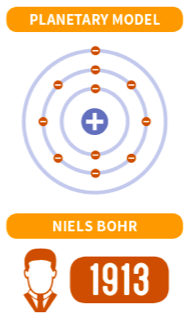
- Viisi oletusta vetyatomin rakenteesta:
- Vetyatomin elektroni kiertää ympyrärataa positiivisen ytimen ympärillä
- Elektroni pysyy radallaan Coulombin lain välisen vetovoiman ansiosta
- Elektronin rata voidaan määrittää klassisen mekaniikan liikeyhtälöstä
- Tietyt radat ovat pysyviä; kun atomilla on pysyvät radat, se ei säteile energiaa
- Kun atomin elektroni siirtyy radalta toiselle, absorboituu tai emittoituu säteilykvantti
Kuva: CompoundChem
Bohrin vetyatomimalli
- Vetyatomin pysyvien energiatilojen (elektronien eri ratojen) energiat saadaan yhtälöstä
- Energia 13,6 eV on luonnonvakioista johdettu energian arvo
- Termi n saa arvoja 1, 2, 3, ...
- Se ilmaisee vetyatomin perustilan tai viritystilan
- Perustilalla n = 1, 1. viritystilalla n = 2, 2. viritystilalla n = 3 jne.
- Kahden tilan välinen siirtymä joko vapauttaa tai vaatii energiaa
- Atomi vastaanottaa (absorboi) energian fotonilta tai emittoi fotonin
Energiatasokaavio
- Vetyatomin elektronin energia on kvantittunut
- Laskemalla elektronin pysyvät energiatilat, voidaan piirtää energiatasokaavio
jne.
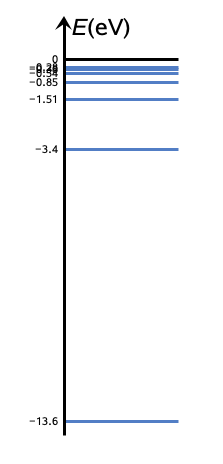
TI: Widget Aine ja säteily Energiatasokaavio
Huom! Elektronin energia on negatiivinen
Energialla 0 eV atomi ionisoituu eli elektroni irtoaa
Esimerkki 1
Virittyminen perustilasta (n = 1) toiseen viritystilaan (m = 3) vaatii energian
Lopputilanteesta m = 3 vähennetään alkutilanne n = 1!
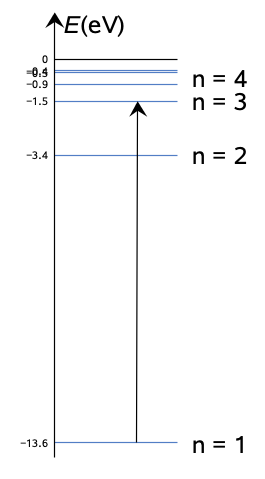
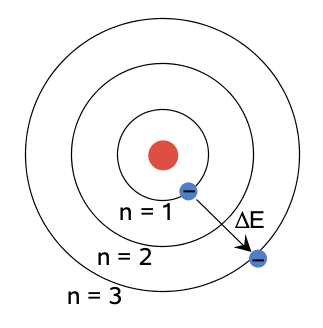
Energiatasokaavio:
Elektroni absorboi energialtaan 12,1 eV:n fotonin, jotta se voi siirtyä perustilalta toiselle viritystilalle.
Atomin virittyminen ja viritystilan purkautuminen
- Atomit tai molekyylit voivat absorboida tai emittoida energiaa (fotonin)
- Elektronin siirtyminen alemmalta energiatasolta ylemmälle vaatii energiaa (absorptio)
- Siirtyminen ylemmältä alemmalle orbitaalille vapauttaa energiaa (emissio)
- Vapautuvan energian määrästä riippuu, havaitaanko tämä röntgen-, UV-, VIS- vai IR-säteilynä
-
Esim. revontulissa happi ja typpi virittyvät, ja viritystilojen purkautuminen havaitaan näkyvän valon alueella punaisena ja vihreänä valona
- Typpi: 391 nm (violetti) ja 473 nm (sininen)
- Happi: 558 nm (vihreä) ja 630 nm (oranssi)
- Esim. röntgensäteilyä voi syntyä mm. kohtiomateriaalin elektronin siirtymistä
-
Esim. revontulissa happi ja typpi virittyvät, ja viritystilojen purkautuminen havaitaan näkyvän valon alueella punaisena ja vihreänä valona
Emittoituvan tai absorboituvan fotonin aallonpituus
- Fotonin energian täytyy olla yhtä suuri kuin elektronin kahden energiatilan erotus
- Toisaalta fotonin energia on
- Aallonpituudeksi saadaan
Vety:
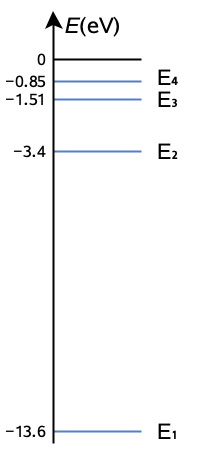
Esimerkki 2
Määritä lyhyin ja pisin mahdollinen fotonin aallonpituus, joita voi emittoitua vedyn 3. viritystilan purkautuessa.
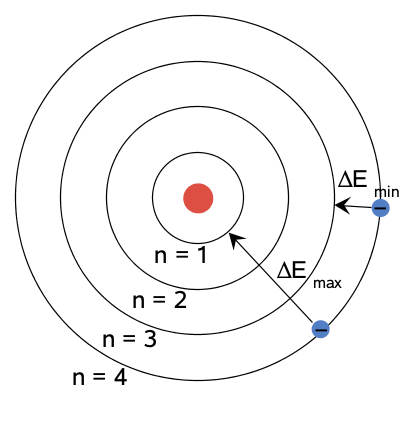
Lyhyin aallonpituus tarkoittaa fotonin suurinta energiaa, eli elektroni siirtyy 3. viritystilalta perustilalle (4 1).
Energia lasketaan vedyn energiatasojen erotuksena. Energiatilat saadaan yhtälöstä
Energioiden erotus on siis
Tätä energiaa vastaava aallonpituus on
UV-säteilyä
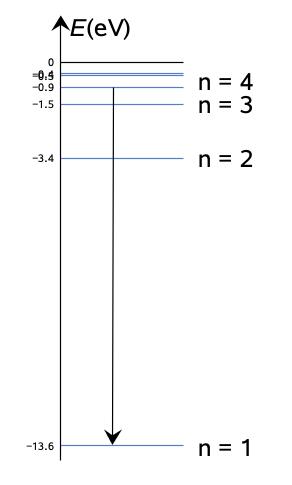
Pisin aallonpituus tarkoittaa fotonin pienintä energiaa, joka tulee viritystilojen erotuksesta. Korkeammat viritystilat ovat lähempänä toisiaan, joten elektroni siirtyy 3. viritystilalta toiselle (4 3).
Energiatilojen erotus on
Tätä energiaa vastaava aallonpituus on
IR-säteilyä
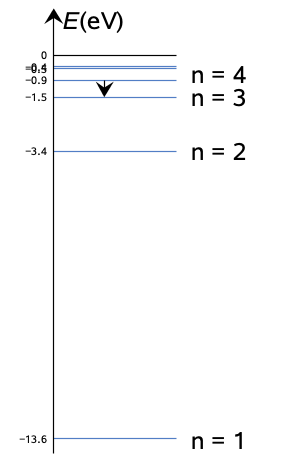
Tehtävä 216b
Revontulet syntyvät yläilmakehässä, kun Auringosta lähteneet suurienergiset hiukkaset vuorovaikuttavat ilmakehän atomien kanssa. Hiukkaset virittävät atomeja, ja viritystilan purkaantuessa syntyy valoa. Revontulien punainen (630,0 nm) ja vihreä (557,7 nm) ovat peräisin happiatomien ja hiukkasten vuorovaikutuksesta.
Mitkä ovat niiden energiatilojen väliset energiaerot, joissa revontulien punainen ja vihreä valo syntyy?

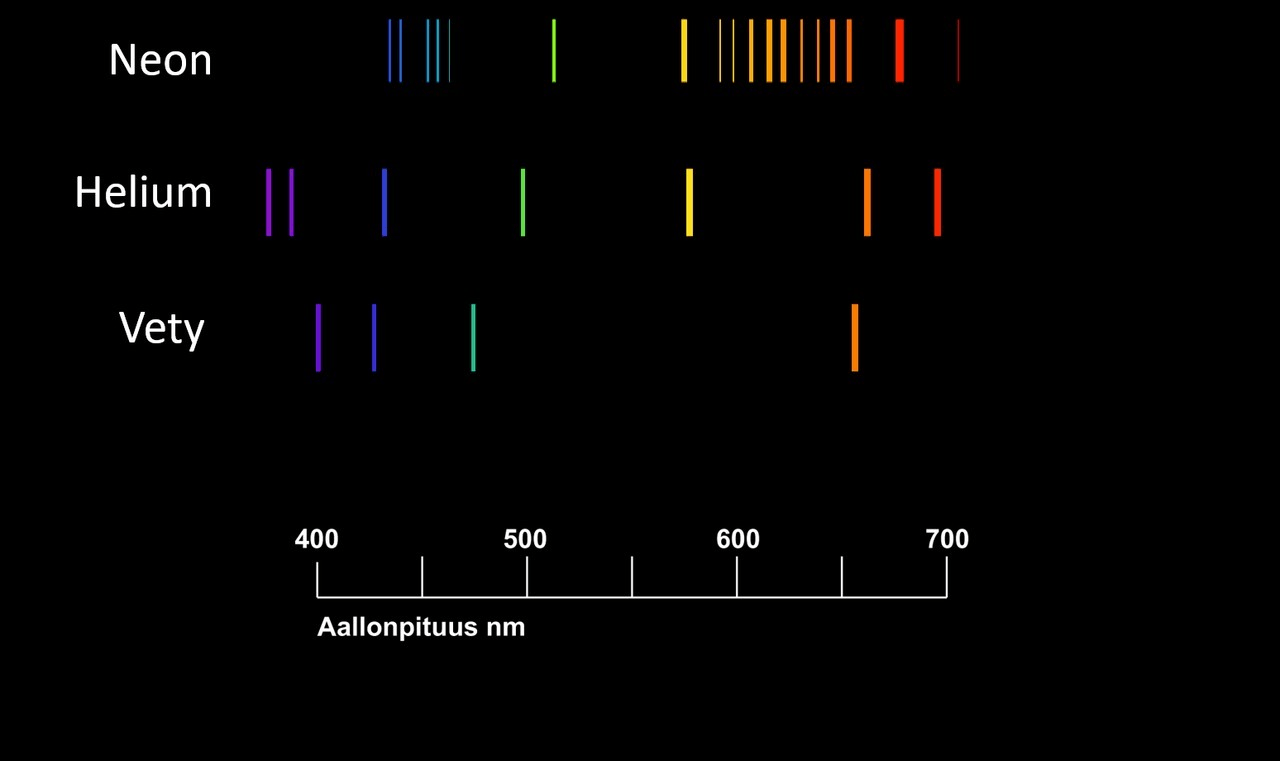
Absorptiospektrin synty
- Atomin tai molekyylin absorboituvat aallonpituudet muodostavat viivaspektrin
- Aine absorboi fotoneja vain tietyillä aallonpituuksilla
- Muunlaiset fotonit eivät vuorovaikuta aineen kanssa, vaan kulkevat sen läpi
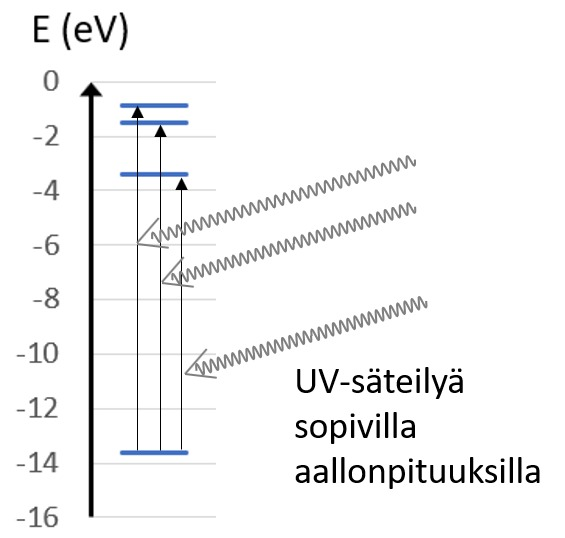
- Absorptio ilmenee absorptiospektrissä tummina viivoina, puuttuvina aallonpituuksina
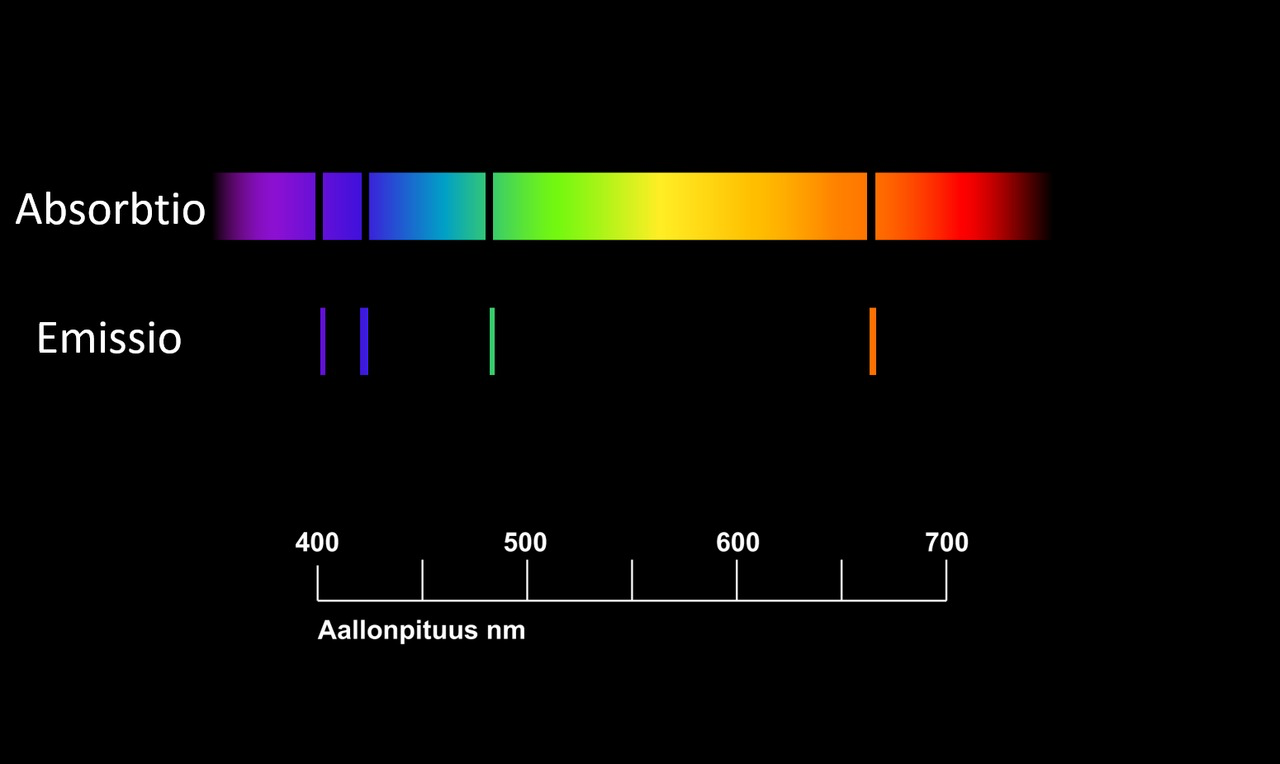
Kuva: Resonanssi 8 (e-Oppi)
Kuva: Resonanssi 8 (e-Oppi)
Emissiospektrin synty
- Atomin viritystilat purkautuvat nopeasti (~ 1 ns)
- Elektroni palaa korkeammalta viritystilalta alemmalle (tai suoraan perustilaan)
- Tällöin vapautuu energiaa (fotoneita)
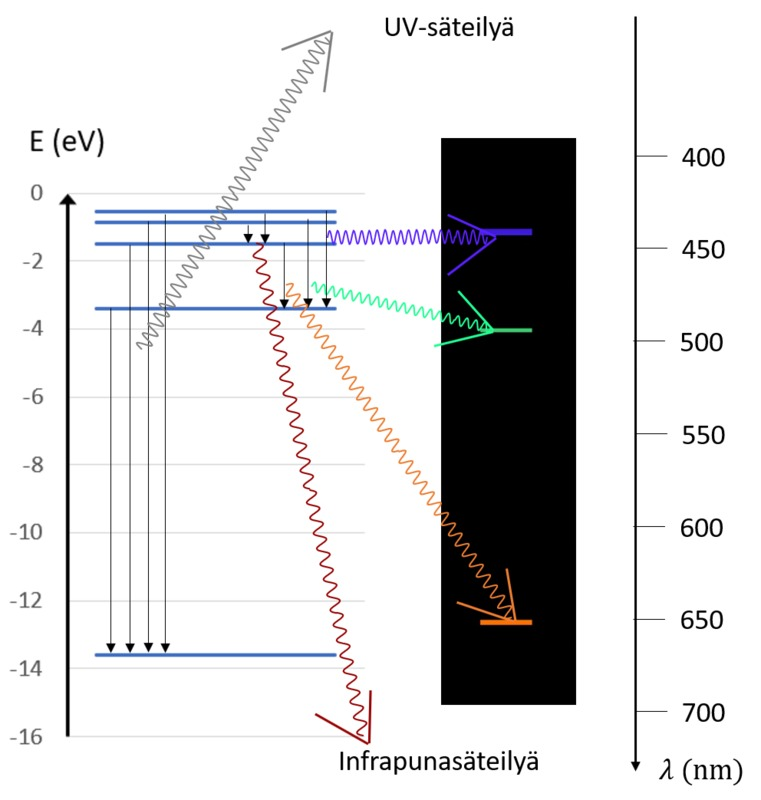
Pienempi energia suurempi aallonpituus
- Emittoituvat aallonpituudet muodostavat viivaspektrin
- Absorptio- ja emissiospektrit kytkeytyvät toisiinsa
- Kuuma alkuaine emittoi samoja aallonpituuksia, joita se absorboi

Liekkikokeet kemiassa!
Kuva: Resonanssi 8 (e-Oppi)
Kuva: Resonanssi 8 (e-Oppi)
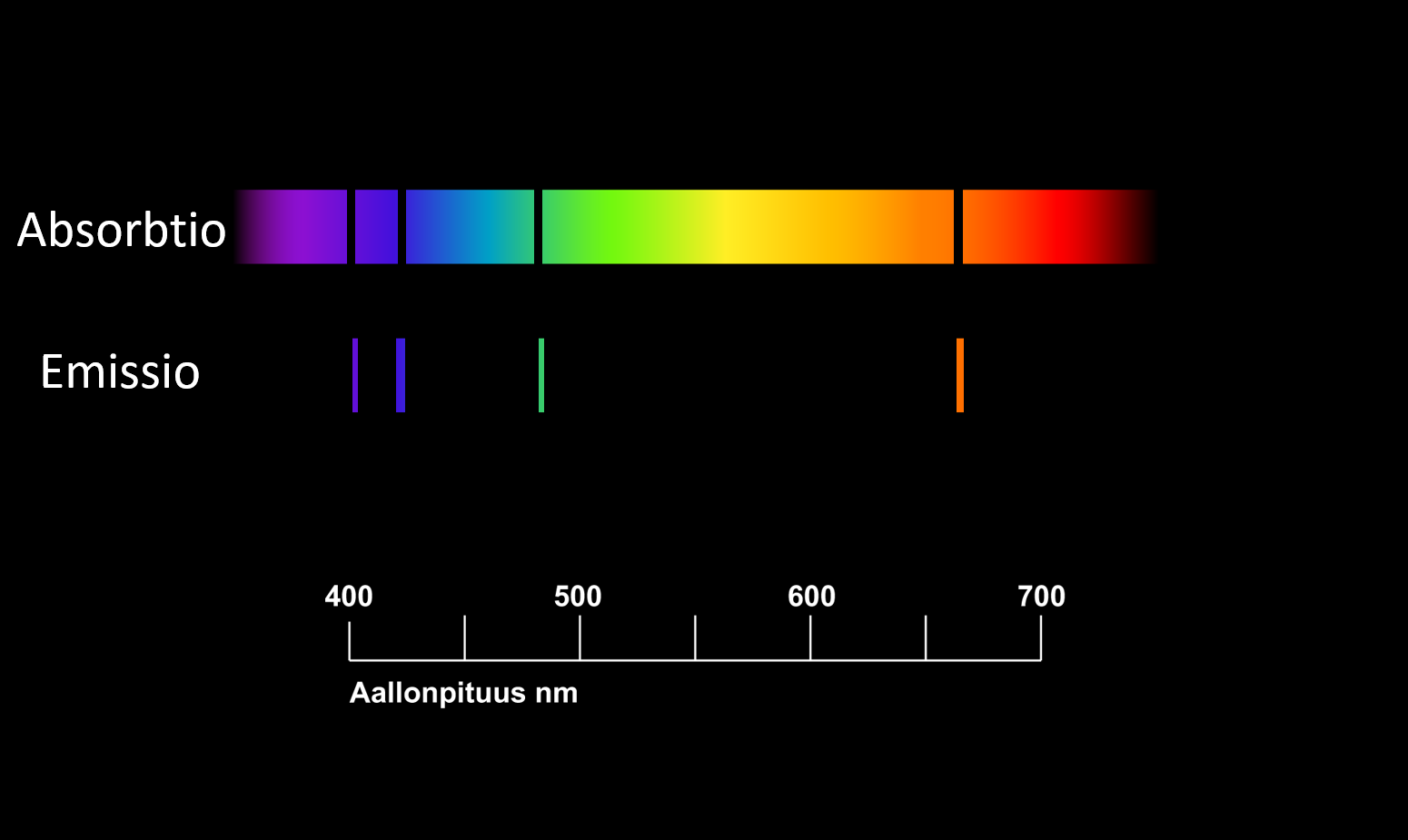
Säteilijän spektri esim. tietyn kaasun läpi
Tämän kaasun emissiospektri
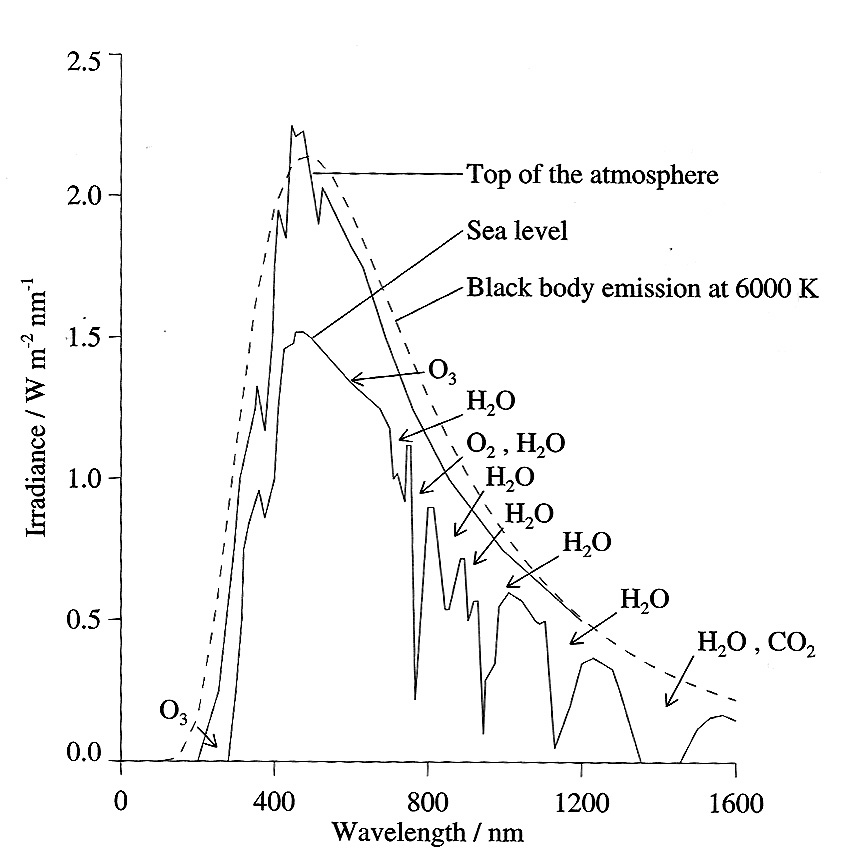
Teoreettinen arvo
UV: otsoni
IR: vesihöyry, hiilidioksidi
Merenpinnan tasolla
Ilmakehän vaikutus Auringon emissiospektriin
Ilmakehän ylärajalla
Kuva: Resonanssi 8 (e-Oppi)
Bohrin atomimallin puutteet
- Bohrin atomimalli selitti vain vedyn spektrin oikein
- Useampia elektroneja sisältävien atomien energiat ovat myös kvantittuneet, mutta niitä ei voi laskea vetyatomin tavoin
- Malli ei myöskään antanut pysyville tiloille fysikaalista selitystä
- Malli ei selittänyt spektriviivojen toisistaan poikkeavia intensiteettejä

Kuva: CompoundChem
Kvanttimekaaninen atomimalli
- Elektronin tilaa kuvataan neljällä kvanttiluvulla, jotka määräävät sen tilan
- Kvanttimekaanisessa atomimallissa elektroni ei ole tietyllä tasolla
- Sille löytyy alue, jossa se todennäköisimmin on (orbitaali)

- Monielektroniatomimallin täsmällisten tilojen laskeminen on hankalaa
- Voidaan tehdä hyviä arvioita atomien kvantittuneille energiatiloille ja elektronien esiintymistodennäköisyyksille
-
Paulin kieltosääntö antaa ehdon kvanttimekaaniselle atomimallille
- Saman atomin elektronit eivät voi olla samassa tilassa eli niillä ei voi olla täsmälleen samat kvanttiluvut
Kuva: CompoundChem
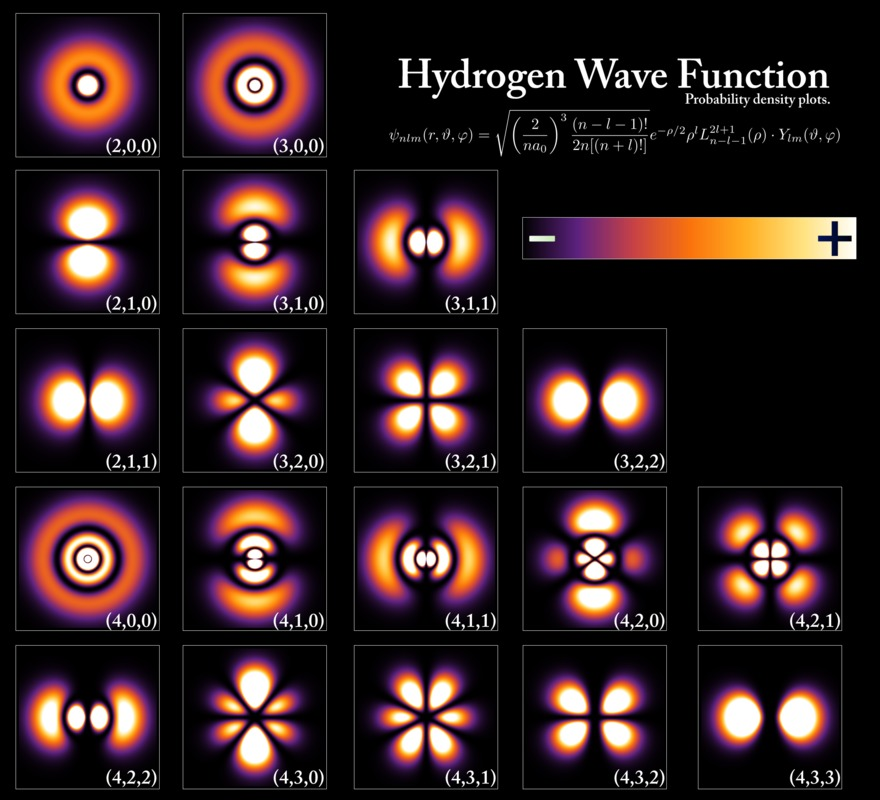
Elektronin sijainnin todennäköisyysjakaumia eri energiatiloilla
Vedyn aaltofunktio
Kuva: Wikimedia CC0
Monielektroniatomit
- Monielektroniatomien energiatilat ovat myös kvantittuneet
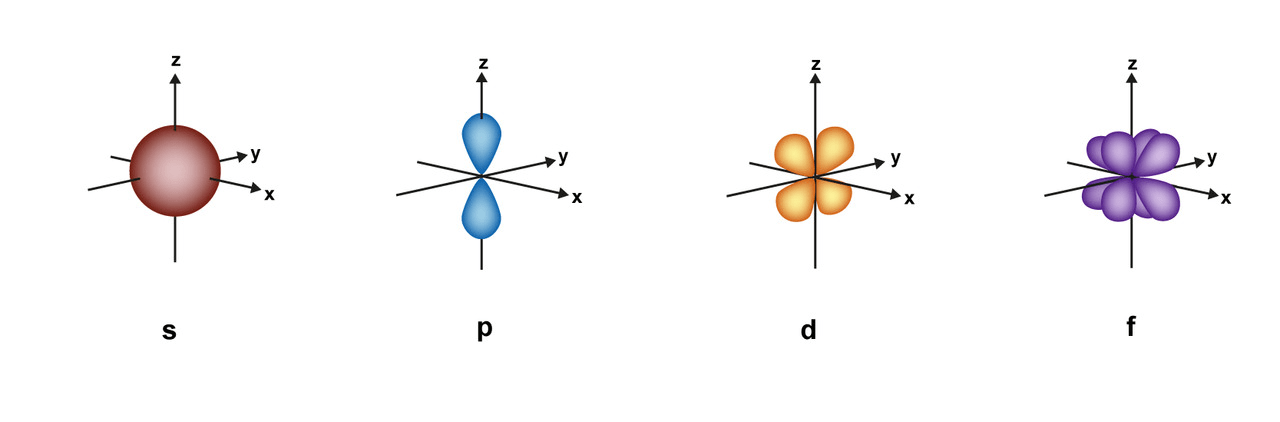
Kuvat: Resonanssi 8 (e-Oppi)
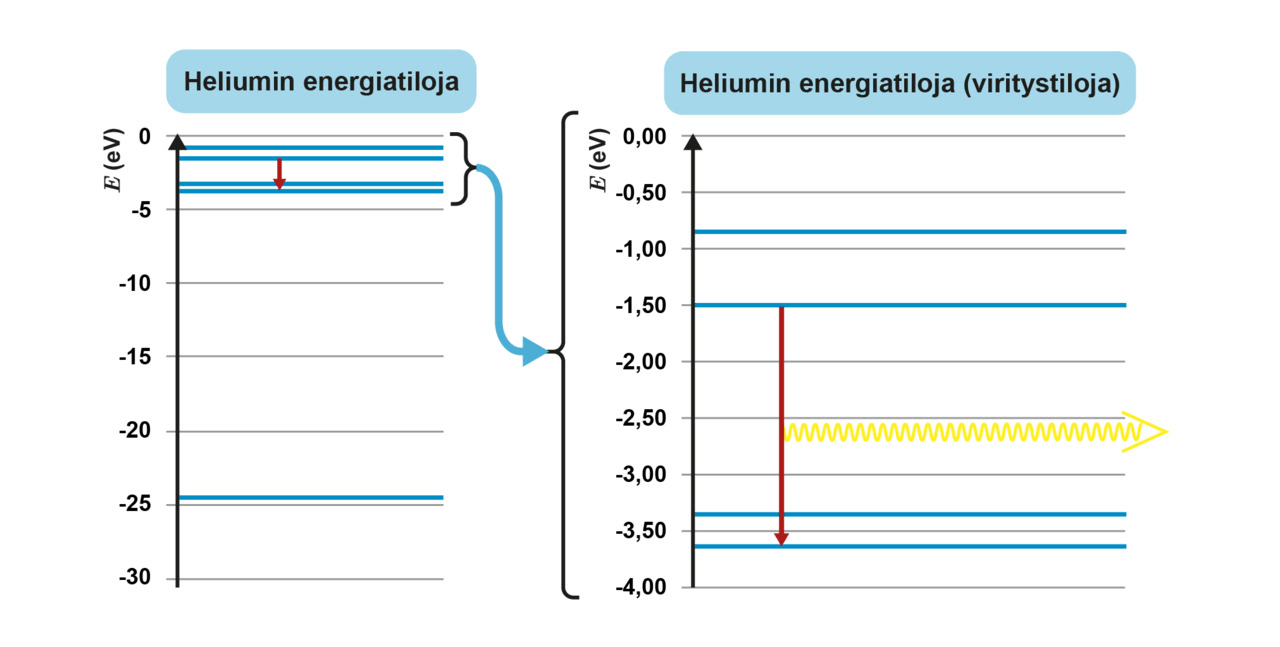
- Elektronit asettuvat elektronikuorille
- Pääkuoria ilmaistaan pääkvanttiluvulla 1, 2, 3, ... tai K, L, M, ...
- Pääkuoret jakautuvat eri muotoisiin alakuoriin, joita ilmaistaan sivukvanttiluvuilla s, p, d, f, ...
- Muut kvanttiluvut ovat magneettinen kvanttiluku ja spinkvanttiluku
Elektronien sijoittuminen orbitaaleille
- Minimienergiaperiaate
- Elektronit asettuvat orbitaaleille alimpiin mahdollisiin energiatiloihin
- Paulin kieltosääntö
- Kahdella elektronilla ei voi olla täysin sama energiatila: yhdelle orbitaalille mahtuu 2 elektronia, joilla eri spin
- Jokaisella elektronilla oma neljän kvanttiluvun yhdistelmä
- Hundin sääntö
- Elektronit sijoittuvat energialtaan samanarvoisille orbitaaleille samansuuntaisin spinein niin pitkälle kuin mahdollista
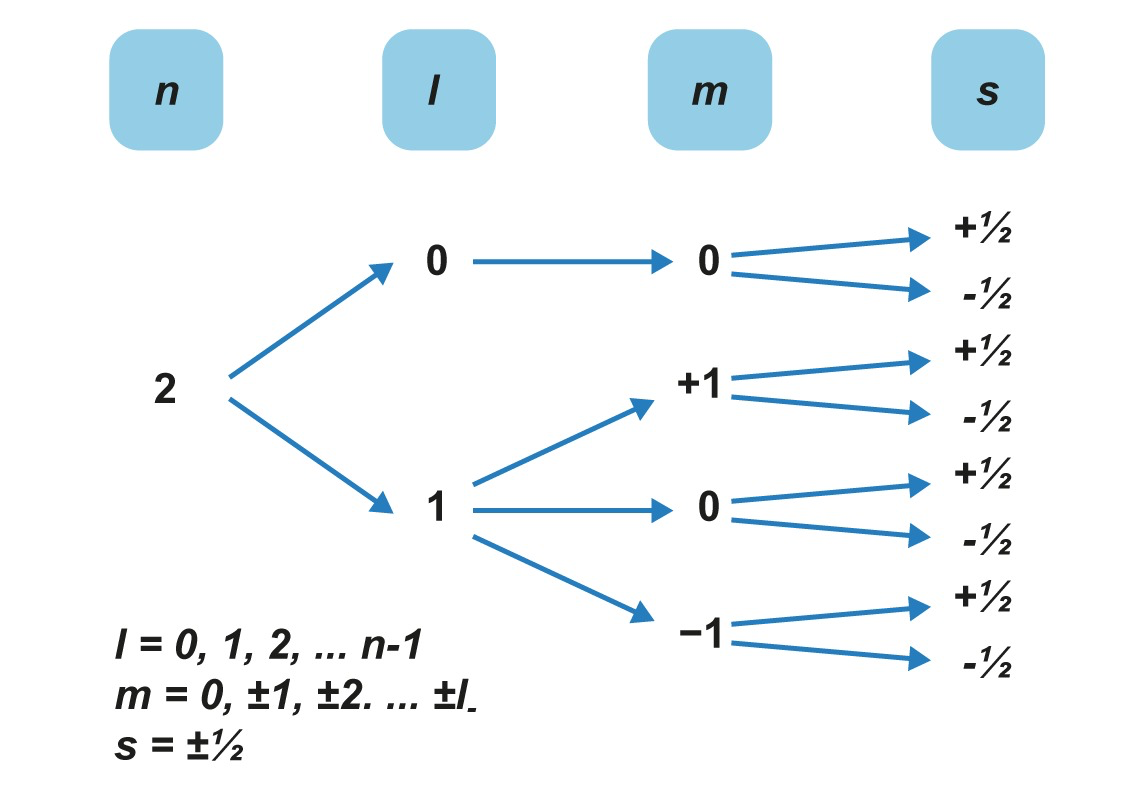
n = 2 8 yhdistelmää
Pääkvanttiluku
Sivukvanttiluku (aina pienempi kuin pääkvanttiluku)
Magneettikvanttiluku
Spinkvanttiluku
Pääkvanttiluku: elektronin energian suuruusluokka (~ sijainti)
Kuva: Resonanssi 8 (e-Oppi)
Sivukvanttiluku: avaruuden osa, jossa elektroni todennäköisimmin sijaitsee, orbitaalin muoto
Magneettinen kvanttiluku: elektronien energia magneetti-kentässä, orbitaalin asento
Spinkvanttiluku: erottelee yhdessä orbitaalissa olevat elektronit toisistaan ("elektronien pyöriminen")
Jaksollinen järjestelmä
- Kvanttimekaniikka selittää jaksollisen järjestelmän
- Muotoutuu sen mukaisesti, miten elektronit täyttävät energiatiloja
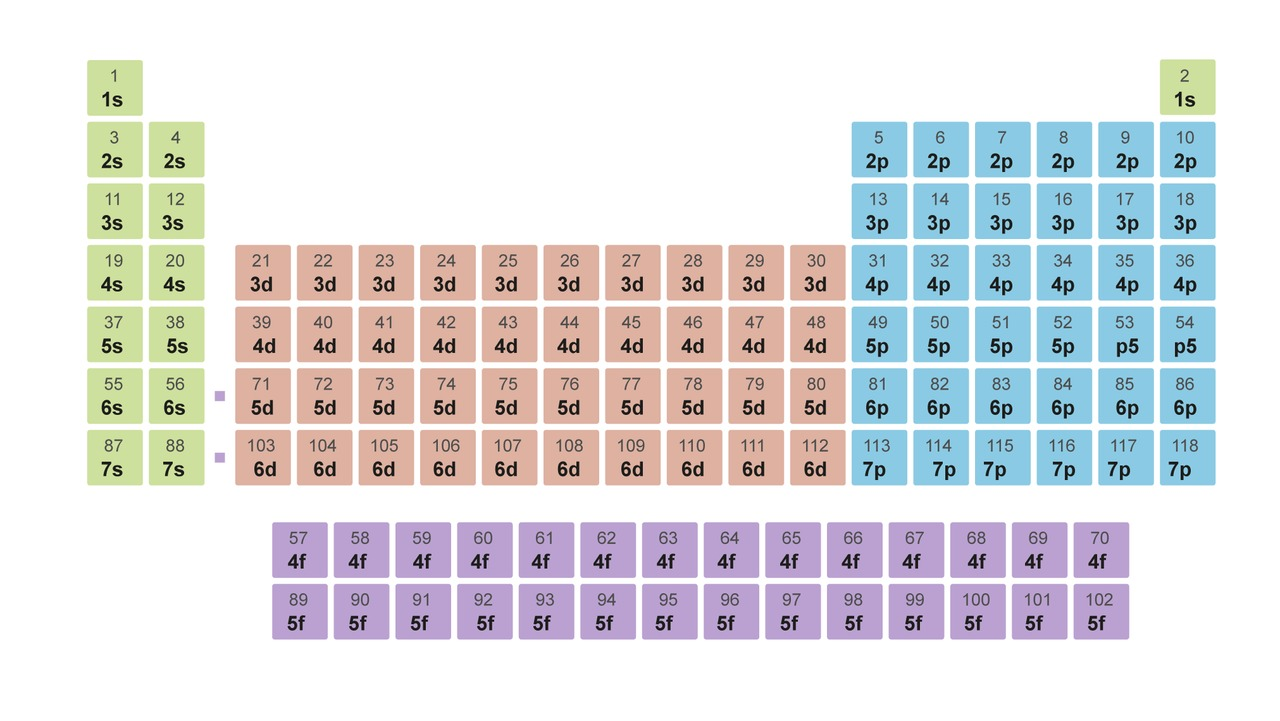
Kuva: Resonanssi 8 (e-Oppi)
2.1/2.2 Atomi ja sen spektrin synty, monielektroniatomit
By pauliinak
2.1/2.2 Atomi ja sen spektrin synty, monielektroniatomit
FY08 Aine, säteily ja kvantittuminen
- 792



