3.1 Atomiydin
FY08 Aine, säteily ja kvantittuminen
Atomin rakenne
- Atomin massa on keskittynyt sen ytimeen
- Ytimen hiukkasia (protonit ja neutronit) kutsutaan nukleoneiksi
- Ydintä ympäröi elektroniverho, joka määrää atomin koon
- Protoni ja neutroni muodostuvat kolmesta kvarkista
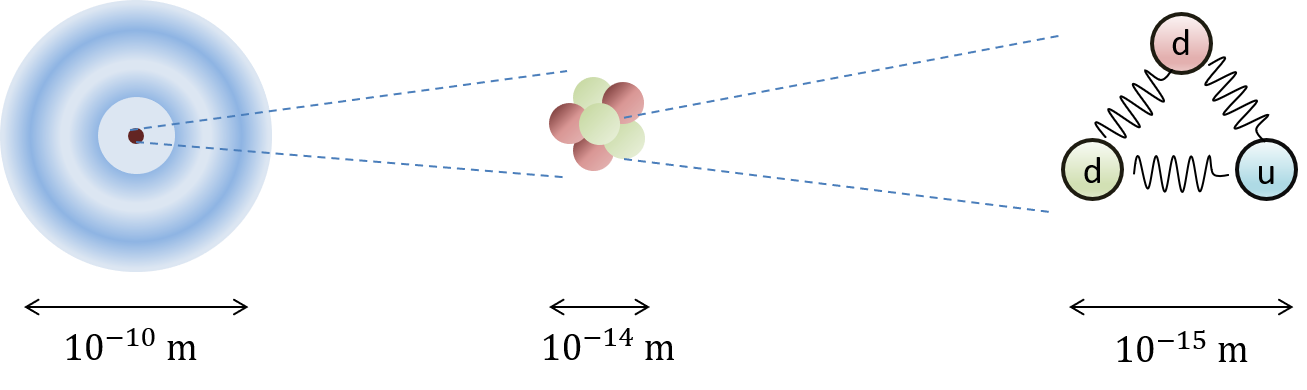
d-kvarkin varaus on –1/3 e, u-kvarkin +2/3 e.
Protonin varaus on +1 e, elektronin –1 e. Neutronilla ei ole varausta.
Kuva: Resonanssi 8 (e-Oppi)
Ytimen vuorovaikutuksista
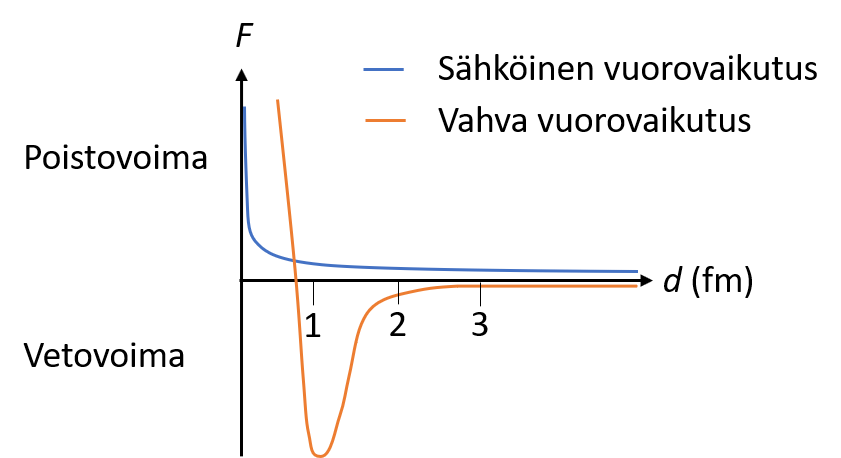
- Protonien välinen sähkömagneettinen vuorovaikutus (sähköinen voima) pyrkii työntämään protoneja erilleen
- Kvarkkien välinen vahva vuorovaikutus (ydinvoima) pitää ydintä koossa
- Kun nukleonit ovat riittävän lähellä toisiaan, ne voivat tuntea naapurihiukkasen vahvan vuorovaikutuksen
- Ydin pysyy koossa, kun ydinvoima (vetovoima) on voimakkaampi kuin sähköinen poistovoima
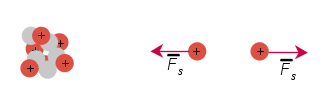
Protonien väliset voimat
Kuva: Resonanssi 8 (e-Oppi)
Ytimen tasapaino
- Pelkkien protonien välinen ydinvoima ei riitä pitämään niitä koossa
- Useamman protonin sisältävissä ytimissä on myös neutroneja
- Hyvin raskaissa ytimissä sähköinen poistovoima hyvin suuri (esim. uraaniytimessä 92 protonia)
- Ydinvoima pitää ytimen juuri ja juuri kasassa
- Kaikkein raskaimmissa ytimissä on enemmän neutroneja kuin protoneja
- Pieni "tönäisy" neutronilla voi hajottaa ytimen kahteen osaan, jolloin sähköinen voima sinkoaa osat erilleen
- Fissiossa vapautuva "ydinenergia" on sähköistä potentiaalienergiaa!
Atomien merkitseminen
- Atomiytimet eroavat toisistaan protonien ja neutronien lukumäärän kautta
- Merkintä usein lyhennetään, koska kemiallinen merkki kertoo protonien lukumäärän
X = alkuaineen kemiallinen merkki
A = massaluku eli protonien ja neutronien yhteismäärä
Z = järjestysluku eli protonien lukumäärä
Isotooppi
- Protonien lukumäärän pysyessä samana alkuaine ei muutu
- Samalla alkuaineella voi olla eri määrä neutroneita
- Saman alkuaineen atomit, joissa neutroneita on eri määrä, ovat alkuaineen isotooppeja
- Monesti alkuaineella on vain yksi pysyvä isotooppi
- Muut hajoavat radioaktiivisesti (itsestään tai avustettuna)
- Vedyllä on 2 erikoista isotooppia: deuterium ja tritium
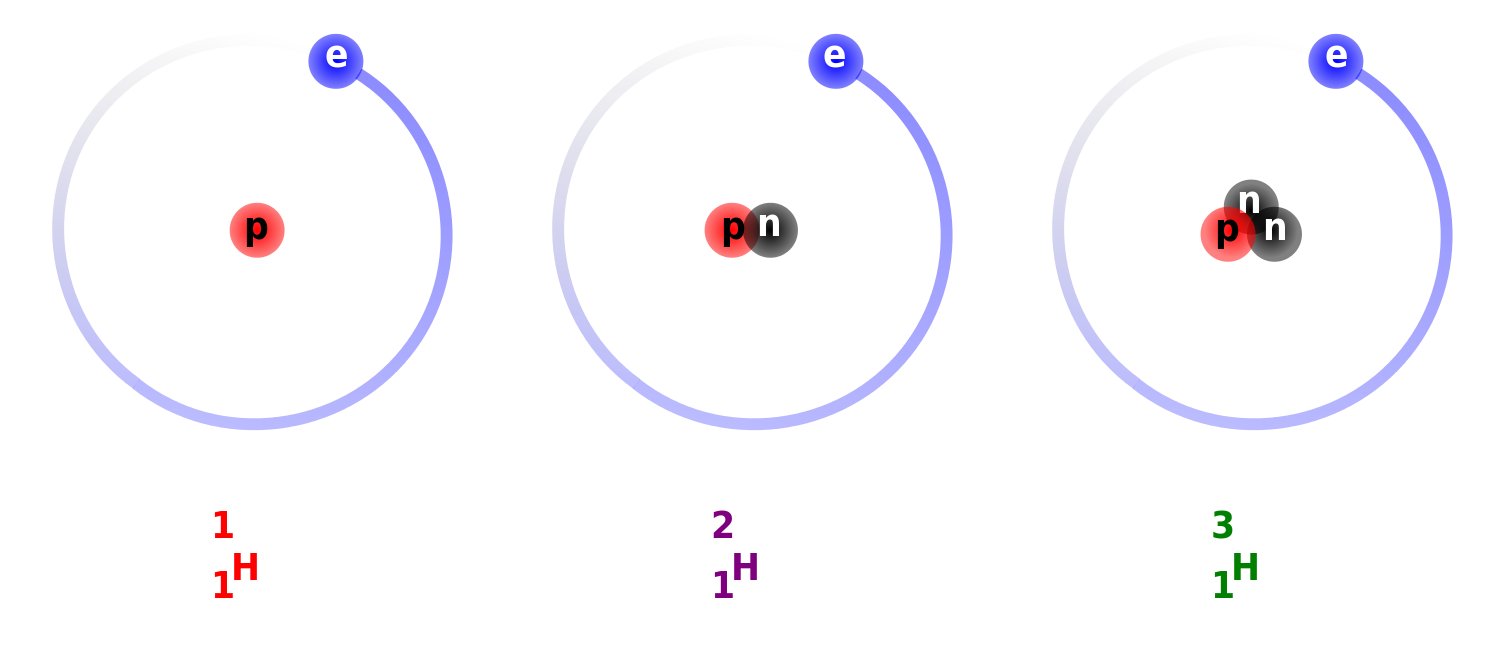
Kuva: Wikipedia
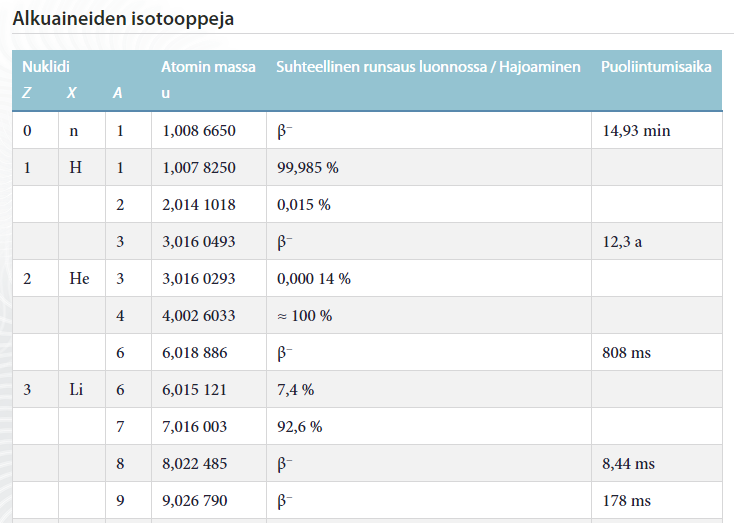
Luonnossa esiintyvä vety on lähes kaikki "tavallista" vetyä (99,985 %).
Vain pieni osa on deuteriumia (0,015 %).
Kuva: MAOL-taulukot (Otava)
Atomimassayksikkö
- Suurin osa atomin massasta on sen ytimessä
- Atomin massa on suunnilleen protonien ja neutronien yhteismäärä (massaluku) kerrottuna yksittäisen protonin tai neutronin massalla
- Atomimassayksikkö u (dalton) on massan lisäyksikkö
- Määritelmä: hiilen C-12 -isotoopin massa on tasan 12 u
- 12 grammaa hiili-12 -atomeja sisältää yhden moolin verran hiiliatomeja
- 12 grammassa hiiltä (1 mol) on Avogadron luvun verran atomeja
- Määritetään yksi atomimassayksikkö kilogrammoissa:
Lukuarvoja
-
Jaksollisessa järjestelmässä esiintyvät massaluvut ovat isotooppien massoista lasketut painotetut keskiarvot
- Esim. kuparin pysyvät isotoopit:
- Taulukkokirjan isotooppitaulukossa on kunkin atomin massa
- Atomiytimen massa = atomin massa – elektronien massat
Cu-63: massa 62,929 598 u, osuus 69,17 % ja Cu-65: massa 64,927 793 u, osuus 30,83 %
elektroni
protoni
neutroni
alfahiukkanen



Esimerkki 1
Laske kahden protonin ja kahden neutronin yhteenlaskettu massa. Vertaa tulosta alfahiukkasen eli heliumytimen massaan (kts. MAOL).
Kahden protonin ja kahden neutronin yhteenlaskettu massa on
Hiukkaset erikseen
Hiukkaset yhdessä
???

Massavaje
-
Atomiytimen massa on aina pienempi kuin ytimen muodostavien hiukkasten yhteenlaskettu massa
- Eroavuutta Δm kutsutaan massavajeeksi
- Suhteellisuusteorian mukaan massalla ja energialla on yhteys
-
Einsteinin yhtälö kertoo, että kun kappaleella on massaa, sillä on tietty määrä energiaa, vaikka se olisi levossa (massa on energian muoto)
- Käänteisesti: fotonin lepomassa on nolla, mutta sillä liike-energiaa
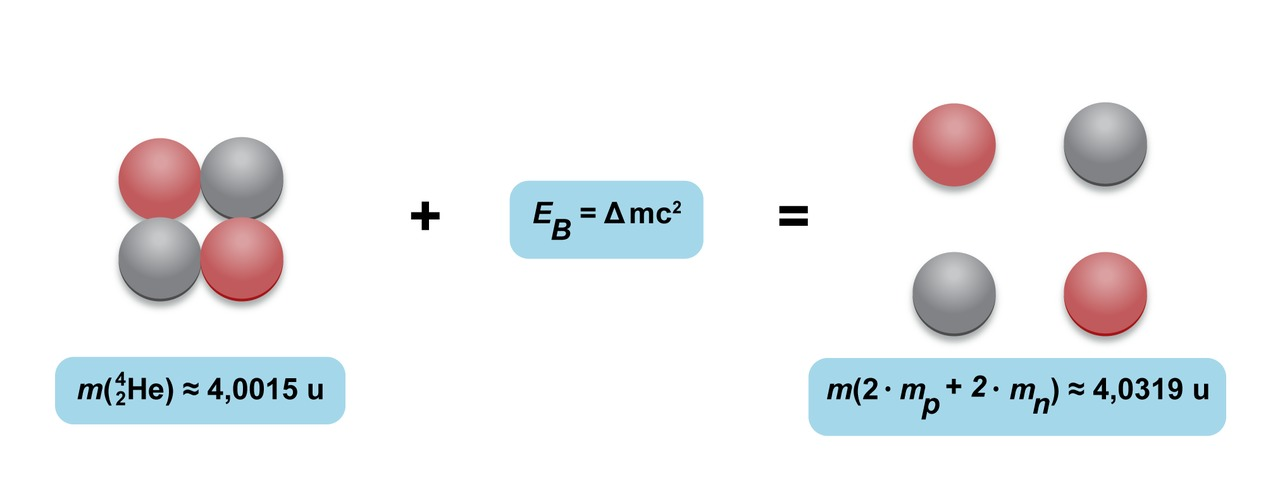
energiaa / massaa
Kuva: Resonanssi 8 (e-Oppi)
Miksi E = mc²?
- Paikallaan olevassa laivassa ammutaan tykillä vastakkaiseen laitaan
- Laiva liikkuu taaksepäin ja kuula liikkuu eteenpäin
- Koko systeemin massakeskipiste pysyy paikoillaan, sillä siihen ei vaikuta ulkoisia voimia

- Tykki korvataan laserpyssyllä
- Lasersäteellä on liikemäärä, joten laiva liikkuu jälleen taaksepäin
- Systeemin massakeskipisteen täytyy pysyä paikoillaan
- Laiva on siirtynyt, joten säteen mukana on siirtynyt massaa toiseen laitaan!

Esimerkki 2
a) Auringon säteilyn teho on . Kuinka paljon aurinko menettää massaa sekunnissa?
b) Opiskelija juoksee nopeudella 10 m/s. Kuinka suurta massaa kineettinen energia vastaa?
a) Tehon määritelmästä saadaan ratkaistua energia 1 s ajalta.
b) Ratkaistaan opiskelijan liike-energian suuruus ja tätä vastaava massan muutos.
vrt. Auringon massa:
Tätä vastaava massan muutos on Einsteinin yhtälön mukaan
Sidosenergia
- Kun kaksi protonia ja kaksi neutronia muodostavat heliumatomin ytimen (alfahiukkasen), ympäristöön vapautuu energiaa
- Vapautuneen energian suuruus voidaan laskea massavajeen avulla
- Massavaje Δm on vapaiden hiukkasten ja niiden muodostaman atomin massojen erotus
- Sidosenergia EB on ytimen hajottamiseen vaadittu energia (tai ytimen muodostuessa vapautuva energia)
hiukkaset erillään
hiukkaset yhdessä
Esimerkki 3
Laske -isotoopin sidosenergia.
taulukkoarvot:
Massaluku A = 56
Järjestysnumero Z = 26
Neutronien määrä N = 56 – 26 = 30
Lasketaan ensin ytimen massavaje.
Nyt voidaan laskea sidosenergia.
Atomimassayksikkö ja energia
- Yhtä atomimassayksikköä 1 u vastaava energia on
- Muutetaan energian yksikkö joule J elektronivolteiksi eV:
- Näin äskeinen Fe-56 -sidosenergia voidaan laskea myös
vrt.
Huom! Valonnopeuden lukuarvoa ei sijoiteta!
Sidososuus
-
Sidosenergian määrä kasvaa, kun aineen massaluku A kasvaa
- Atomiytimessä ytimen rakenneosien välisten sidosten määrä kasvaa
- Sidososuudella tarkoitetaan sidosenergian määrää nukleonia (eli protonia tai neutronia) kohden
- Sidososuus tarkoittaa keskimääräistä energiaa, jota ytimeen pitäisi tuoda, jotta sieltä saataisiin irrotettua yksi nukleoni
- Sidososuus on pienempi esimerkiksi -ytimellä kuin ytimillä ja
ENERGIAA
(hypoteettinen reaktio, luonnollisessa fissiossa osa neutroneista vapautuu)
Eri ydinten sidososuudet
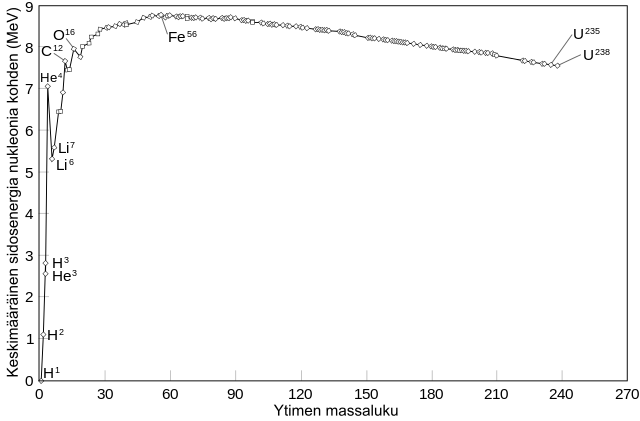
Ydinmuutokset pyrkivät tapahtumaan kohti rautaa.
Fissio
Fuusio
Suurin sidososuus on raudalla (n. 8,7 MeV).
Tiukasti sitoutuneet ytimet
Löyhästi sitoutuneet ytimet
Kuva: Resonanssi 8 (e-Oppi)
3.1 Atomiydin
By pauliinak
3.1 Atomiydin
FY08 Aine, säteily ja kvantittuminen
- 672



