Aineen ja säteilyn kertaus (FY08)
FY10 Kertausta abiturienteille
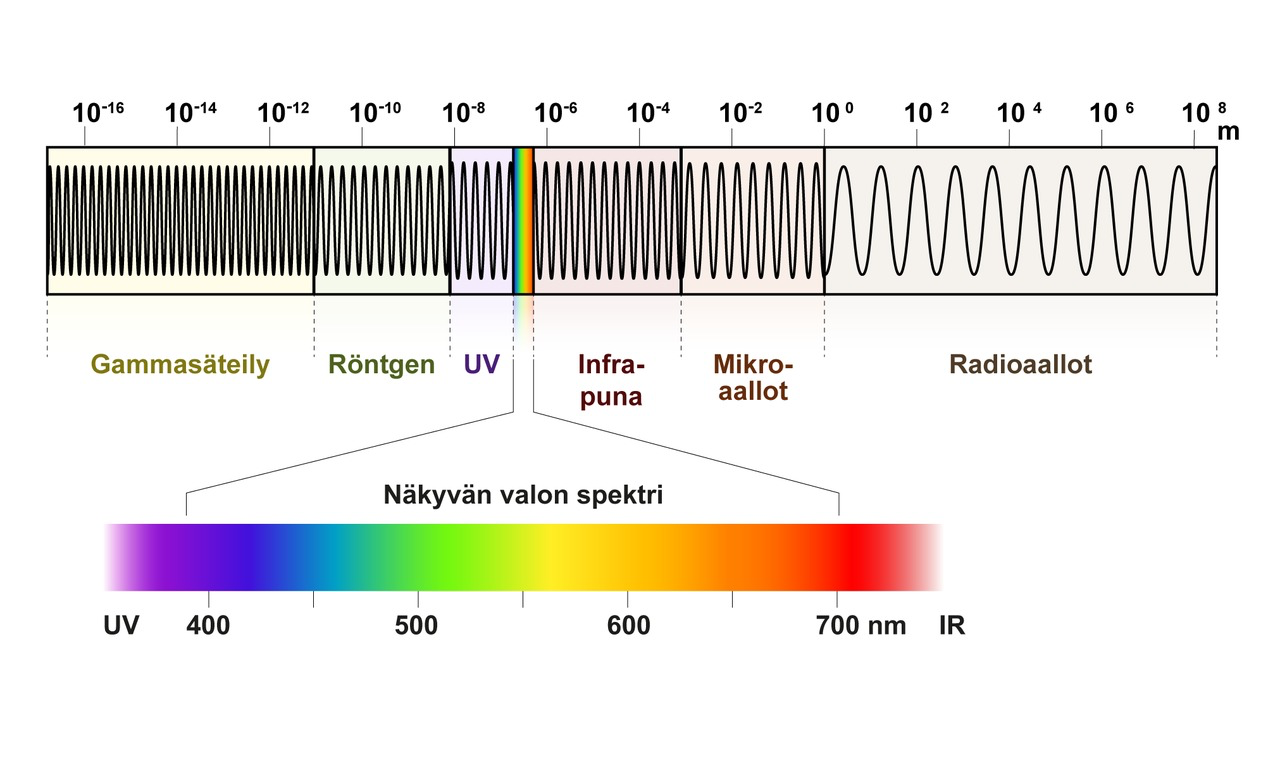
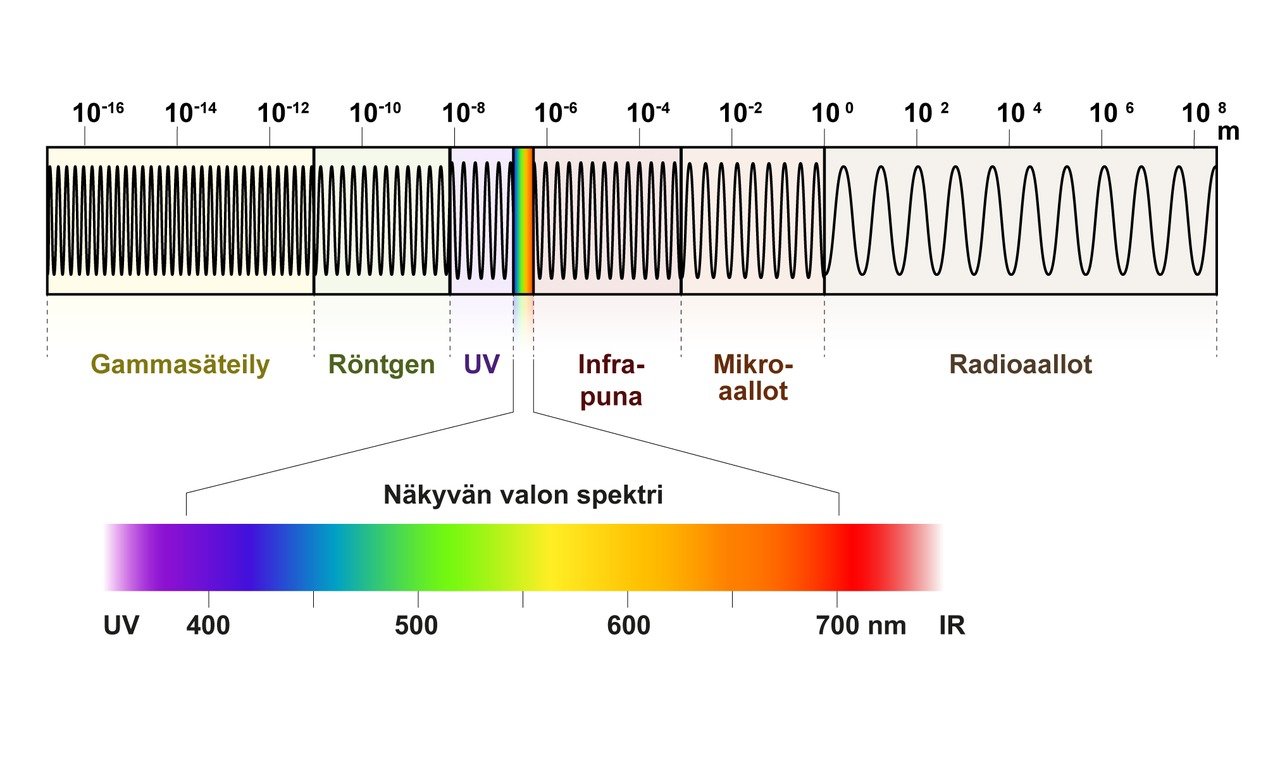
Sähkömagneettinen säteily ja spektri
- Spektri on aaltoliikkeen aallonpituus- tai taajuusjakauma
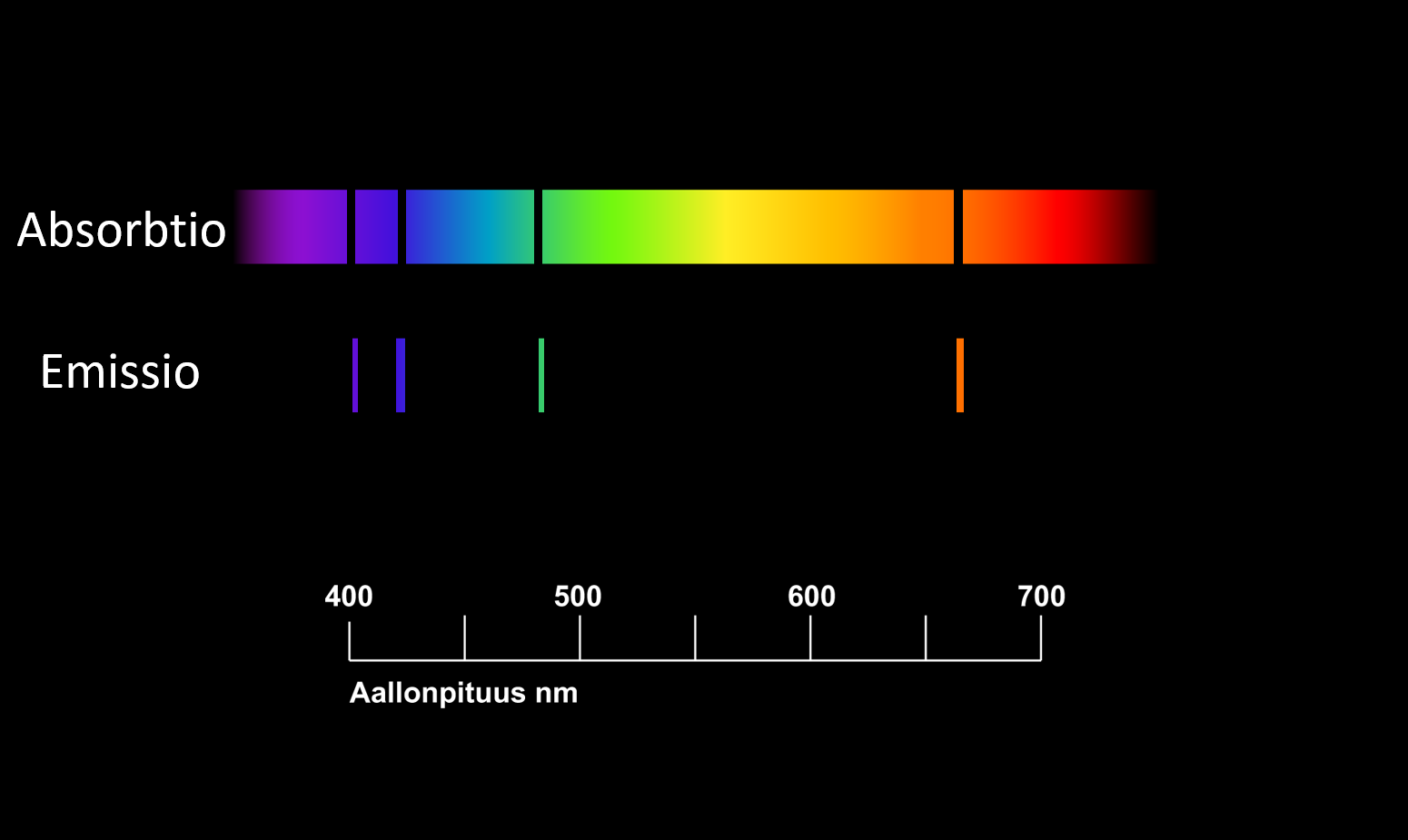
- Emissiospektri on säteilijän lähettämä aallonpituusjakauma
- Kun säteily on kulkenut väliaineen läpi, nähdään absorptiospektri
Aaltoliikkeen perusyhtälö
Valon nopeus tyhjiössä
Emissio ja absorptio
- Aine voi emittoida eli lähettää säteilyä
- Absorptiossa aine vastaanottaa eli absorboi säteilyä
- Emissio ja absorptio ovat mikroskooppisia ilmiöitä
- Aiemmin on puhuttu heijastumisesta, joka on makroskooppinen ilmiö

Emissio
Absorptio
Mustan kappaleen säteily
-
Kaikki kappaleet säteilevät energiaa ympärilleen
- Varatut hiukkaset kiihtyvässä liikkeessä lähettävät SM-säteilyä
-
Ideaalinen malli säteilijälle on ns. musta kappale
- Musta kappale ei heijasta tai sirota säteilyä
- Mustan kappaleen spektri on jatkuva ja sen muoto voidaan määrittää teoreettisesti
- Spektrin intensiteettimaksimin kohta riippuu säteilijän lämpötilasta
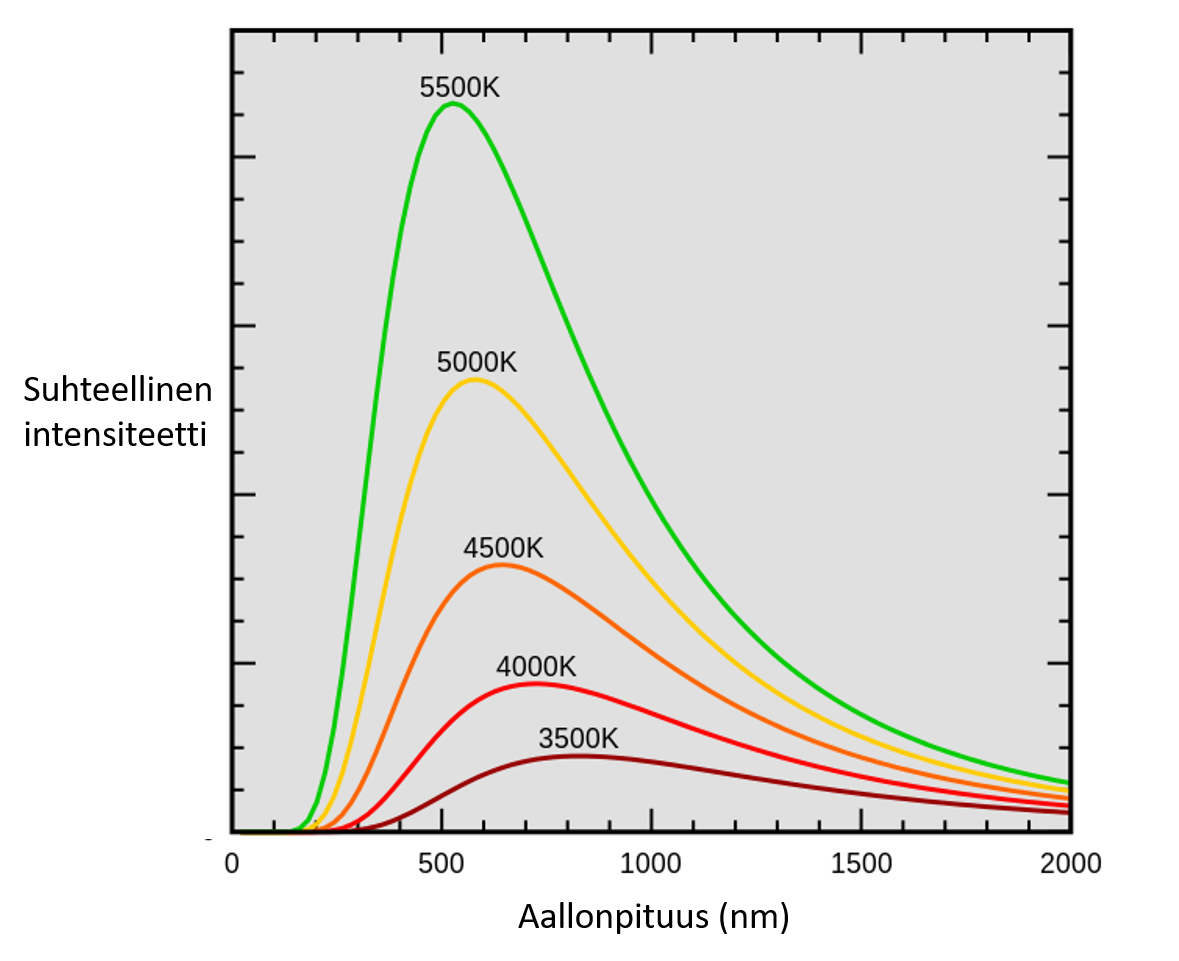
Mitä suurempi lämpötila, sitä pienemmän aallonpituuden kohdalla intensiteettimaksimi on
Wienin siirtymälaki
- Mustan kappaleen säteilyn intensiteettimaksimin aallonpituus ja lämpötila T riippuvat toisistaan

k on vakio:
Viivamaiset emissiospektrit
-
Spektroskopiassa tutkitaan jonkin kohteen lähettämää säteilyä
- Saadaan tietoa säteilijän koostumuksesta
- Viivaspektri muodostuu, kun valoa emittoituu vain tietyillä aallonpituuksilla
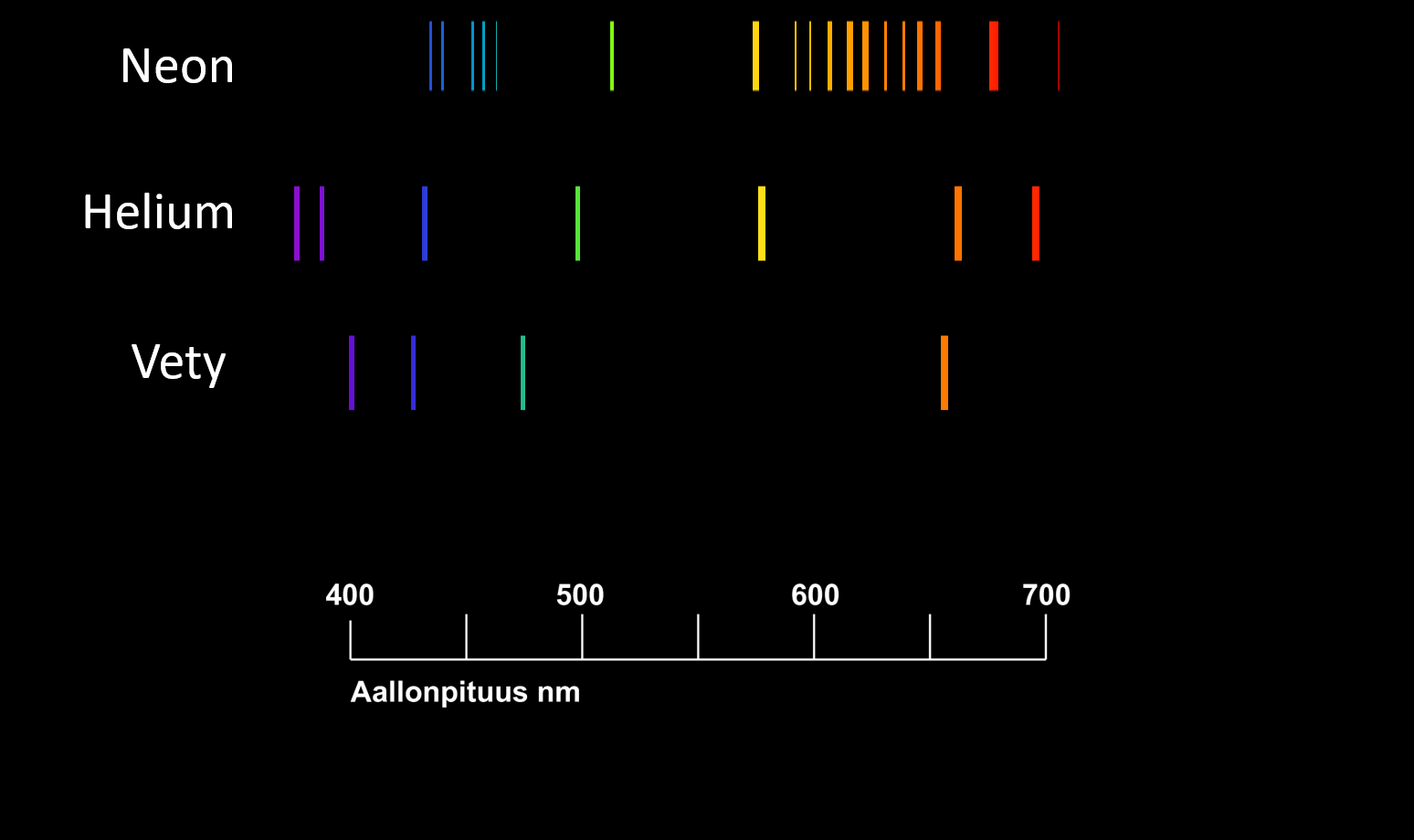
Liekkikokeet kemiassa!
Absorptiospektri
- Auringon valo on esimerkki jatkuvasta spektristä
- Spektristä kuitenkin puuttuu tiettyjä aallonpituuksia
- Alkuaineet absorboivat itselleen ominaisia aallonpituuksia
- Absorptio- ja emissiospektrit kytkeytyvät toisiinsa
- Kuuma alkuaine emittoi aallonpituuksia, joita sama aine absorboi
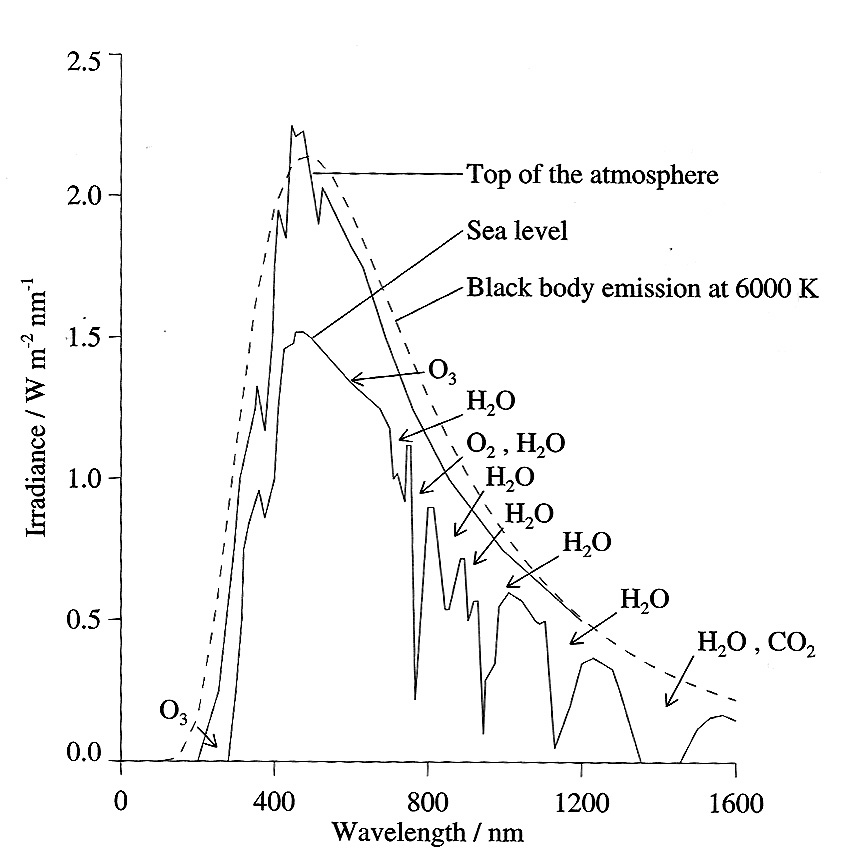
Teoreettinen arvo
UV: otsoni
IR: vesihöyry, hiilidioksidi
Merenpinnan taso
Kvantittuminen
- Mustan kappaleen säteily oli selittämätön ilmiö vuoteen 1900 asti
- Max Planck perusteli spektrin teoreettisesti ns. kvanttihypoteesin avulla
- Säteilyn energia siirtyy "paketteina" (kvantteina)
- Säteilyenergiaa vastaanotetaan ja luovutetaan kvantteina, joiden energia on
Fotoni
- Planckin hypoteesin myötä säteilyä alettiin mallintaa hiukkasmaisena
-
Säteilyn voidaan ajatella koostuvan hiukkasista, joita kutsutaan fotoneiksi
- Mitä korkeampi taajuus (tai mitä lyhyempi aallonpituus) säteilyllä on, sitä enemmän sillä on energiaa
Kvantin energia:
Aaltoliikkeen perusyhtälö:
Valosähköinen ilmiö
- Sähkömagneettisen säteilyn absorboituessa aineeseen säteily luovuttaa siihen energiaa
-
Valosähköilmiössä säteilyn energia irrottaa elektroneja ("valosähköä") metallin pinnasta
- Elektronit eivät irtoa näkyvän valon vaikutuksesta
- UV-valolla on tarpeeksi energiaa se voi irrottaa elektroneja ja purkaa varauksen (videolla)
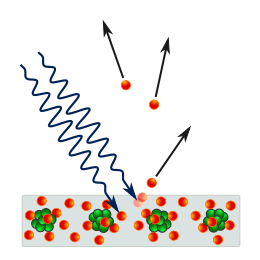
Kuva: Wikipedia, CC BY-SA 4.0
Valosähköilmiön tutkiminen
- Valo irrottaa elektroneja metallin pinnasta
- Elektronit lähtevät liikkeelle ja niille jää liike-energia
- Säädetään pysäytysjännite sellaiseksi, että elektronit eivät pääse kulkemaan toiselle metallilevylle piirissä ei kulje sähkövirtaa
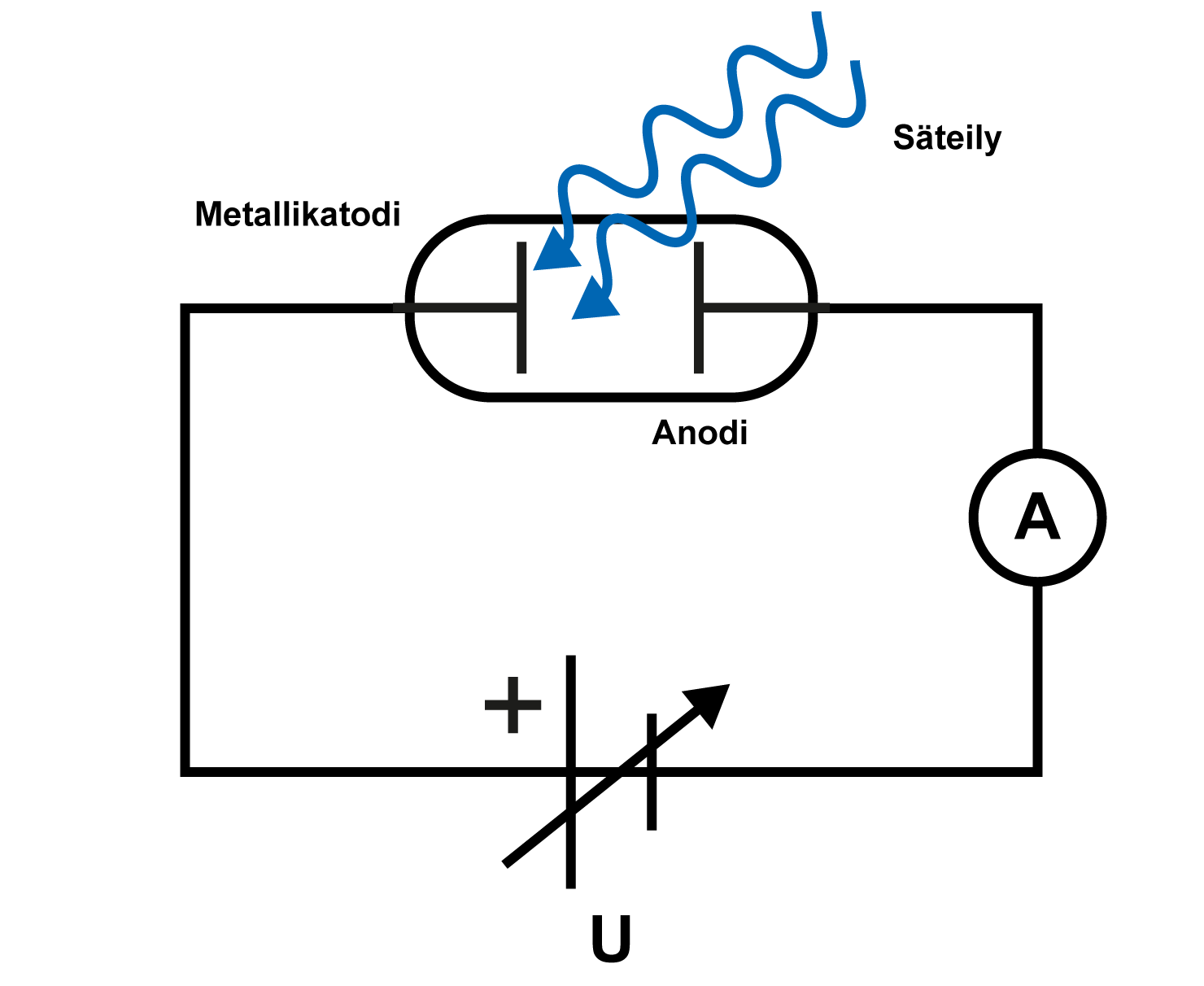
Kahden metallilevyn välillä on säädettävä jännite
Ohjataan lyhytaaltoista valoa toiselle metallilevylle
Valosähköisen ilmiön mallintaminen
- Voidaan tarkastella sekä kvanttihypoteesin että energian säilymislain näkökulmasta
- Säteily luovuttaa metallille energiaa yksittäisinä kvantteina
- Säteilykvantin absorboituessa metalliin sen energia siirtyy kokonaisuudessaan yhdelle elektronille
- Rajataajuus, jolla elektroneja alkaa irrota, on eri metalleilla eri suuruinen
- Jos taajuus on tätä suurempi, osa kvanttien energiasta muuttuu elektronien liike-energiaksi
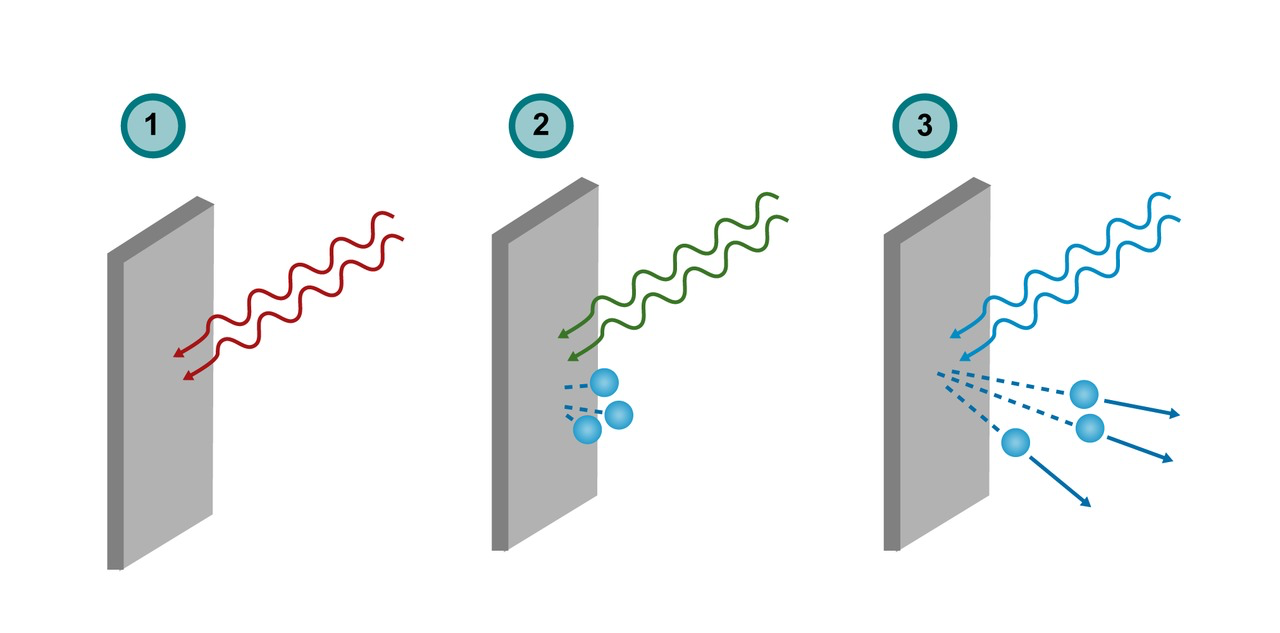
Matalataajuuksinen säteily ei irrota elektroneja
Rajataajuudella elektroneja irtoaa
Suurella taajuudella irtoaa elektroneja, joilla on liike-energiaa
Energia valosähköilmiössä
- Kun jännite pystyy juuri ja juuri pysäyttämään irronneet elektronit, on elektronien liike-energia yhtä suuri kuin sähkökentän tekemä työ
- Osa säteilyn energiasta (hf) kuluu elektronien irrotukseen ( ), loppu jää elektronien liike-energiaksi
- Rajataajuudella kvanttien energia on yhtä suuri kuin metallille ominainen irrotustyö
Valosähköilmiö graafisesti
- Piirretään (f, )-kuvaaja
- Planckin vakio saadaan määrittämällä suoran kulmakerroin
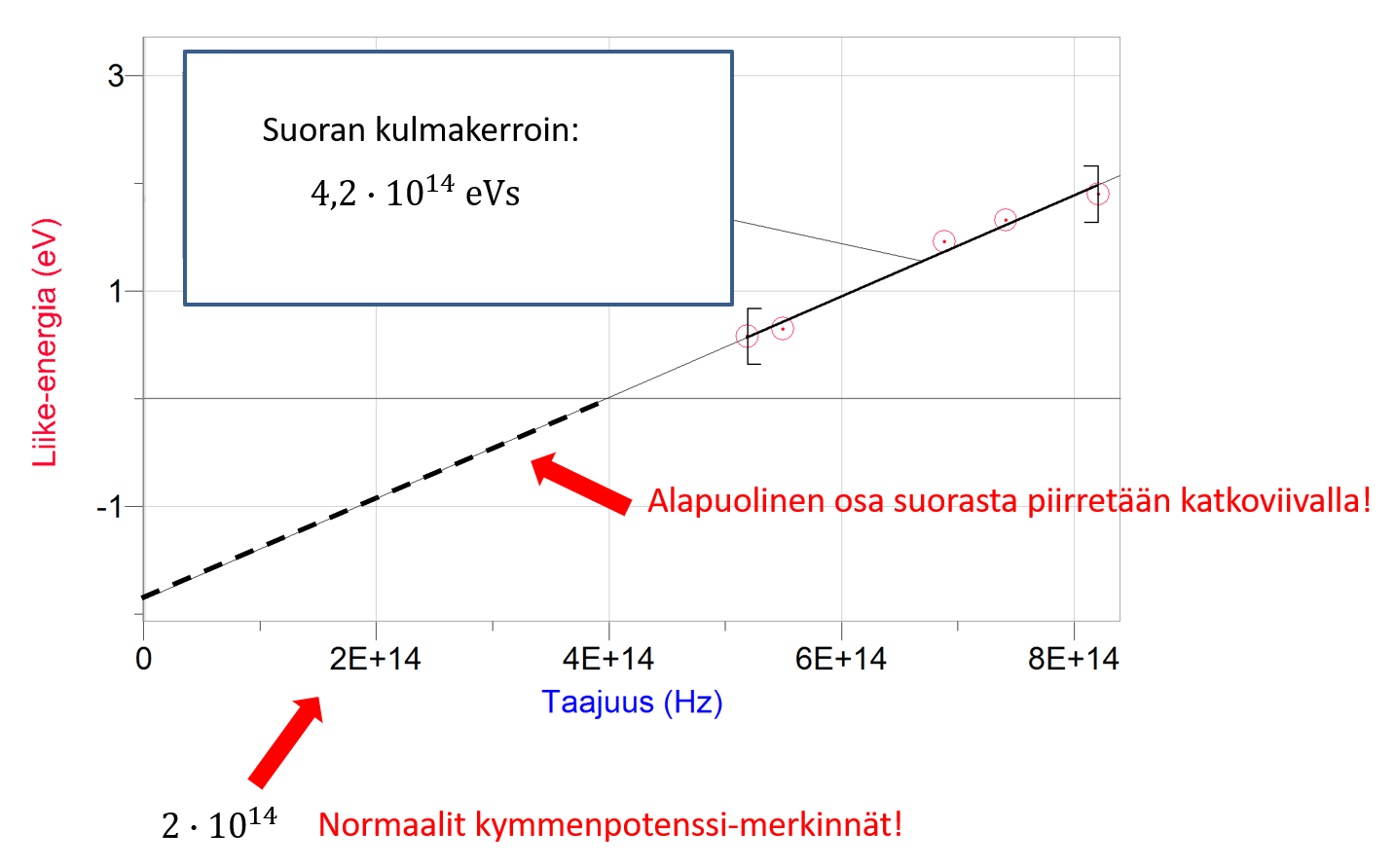
Kulmakerroin
y-akselin leikkauspiste
Energian yksiköt ja kvantit
-
Energian perusyksikkö joule (J) on varsin suuri yksikkö säteilykvanttien energioihin nähden
- Siispä on käytännöllisempää käyttää energian yksikkönä elektronivolttia (eV)
- Elektronivoltti on energia, jonka elektroni saa kulkiessaan yhden voltin kiihdyttävän jännitteen yli
- Kvantin energia lasketaan joko elektronivoltteina tai jouleina
- Planckin vakion yksikkö valitaan halutun energian yksikön mukaisesti
- Jouleja tarvitaan, kun halutaan ratkaista elektronin nopeus
Aaltohiukkasdualismi
- Klassisen käsityksen mukaan säteily jaetaan hiukkasiin ja aaltoihin
- Hiukkassäteilyä on esim. elektronisuihku ja aaltoliikettä sähkömagneettinen säteily
- Havaintojen pohjalta käsitys hiukkasista ja aalloista muuttui


Kaksoisrakokoe valolle (diffraktio):
Kaksoisrakokoe elektroneille:
Kaksoisrakokoe
- Aallot voivat tietyissä tilanteissa käyttäytyä kuin hiukkaset ja hiukkaset käyttäytyä kuin aallot
- Aalto-ominaisuus:
- Elektronit käyttäytyvät kuten valo kulkiessaan kaksoisraosta
- Varjostimelle muodostuu aaltomainen kuvio
- Hiukkasominaisuus:
- Elektronia voidaan pitää hiukkasena, koska varjostimella havaitaan yksittäisten elektronien jättämiä jälkiä
- Energia siirtyy fotonien välityksellä
- Voidaan määrittää liike-energia ja liikemäärä p
- Yksittäiset vuorovaikutustapahtumat: hiukkasominaisuudet
- Vuorovaikutustapahtumia suuri määrä: aalto-ominaisuudet
Comptonin sironta
- Ilmiö paljastaa fotonien hiukkasluonteen
- Fotoni törmää kimmoisasti elektroniin
- Osa fotonin energiasta muuttuu elektronin liike-energiaksi
- Samalla syntyy uusi pienempienerginen fotoni
- Fotonien liikemääräksi on voitu mitata
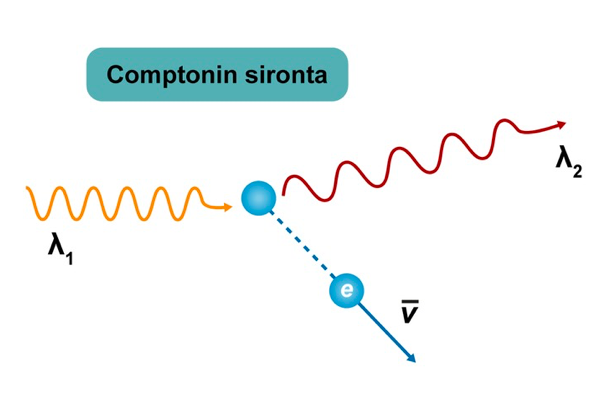
Fotonin ja elektronin törmäyksessä energia ja liikemäärä säilyvät.
Fotonia tarkastellaan Comptonin sironnassa kuin hiukkasta.
de Broglien lait
- Sähkömagneettisen säteilyn lajeilla on sekä aallon että hiukkasen ominaisuuksia
- Aallon ominaisuuksia ovat aallonpituus ja taajuus
- Hiukkasen ominaisuuksia ovat liike-energia ja liikemäärä
- Aallon ja hiukkasten ominaisuudet liitetään toisiinsa de Broglien lakien avulla
- Jos hiukkasilla on massa, liikemäärä ja liike-energiat ovat
- Nopeus on tällöin merkittävästi pienempi kuin valonnopeus
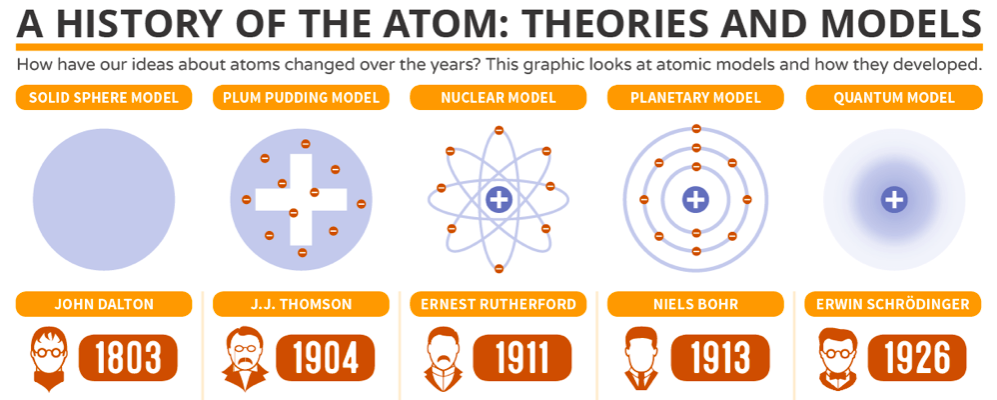
- Käsitys atomin rakenteesta kehittyi vauhdilla 1900-luvun alussa
- Uudet kokeelliset havainnot selitettiin erilaisilla malleilla
Atomimallin kehitys
Niels Bohrin atomimalli
- Niels Bohr yhdisti kvantittumisen idean Rutherfordin malliin
- Bohrin mallissa vain tietyt kiinteät elektronien radat ovat mahdollisia
- Bohr yhdisti Rutherfordin kokeen tulokset ja vedyn spektristä tehdyt havainnot
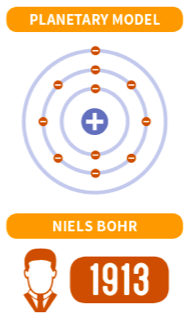
- Viisi oletusta vetyatomin rakenteesta:
- Vetyatomin elektroni kiertää ympyrärataa positiivisen ytimen ympärillä
- Elektroni pysyy radallaan Coulombin lain välisen vetovoiman ansiosta
- Elektronin rata voidaan määrittää klassisen mekaniikan liikeyhtälöstä
- Tietyt radat ovat pysyviä; kun atomilla on pysyvät radat, se ei säteile energiaa
- Kun atomin elektroni siirtyy radalta toiselle, absorboituu tai emittoituu säteilykvantti
Bohrin vetyatomimalli
- Vetyatomin pysyvien energiatilojen (elektronien eri ratojen) energiat saadaan yhtälöstä
- Energia 13,6 eV on luonnonvakioista johdettu energian arvo
- Termi n saa arvoja 1, 2, 3, ...
- Se ilmaisee vetyatomin perustilan tai viritystilan
- Perustilalla n = 1, 1. viritystilalla n = 2, 2. viritystilalla n = 3 jne.
- Kahden tilan välinen siirtymä joko vapauttaa tai vaatii energiaa
- Atomi vastaanottaa (absorboi) energian fotonilta tai emittoi fotonin
Bohrin atomimallin puutteet
- Bohrin atomimalli selitti vain vedyn spektrin oikein
- Useampia elektroneja sisältävien atomien energiat ovat myös kvantittuneet, mutta niitä ei voi laskea vetyatomin tavoin
- Malli ei myöskään antanut pysyville tiloille fysikaalista selitystä
- Malli ei selittänyt spektriviivojen toisistaan poikkeavia intensiteettejä

Kvanttimekaaninen atomimalli
- Elektronin tilaa kuvataan neljällä kvanttiluvulla, jotka määräävät sen tilan
- Kvanttimekaanisessa atomimallissa elektroni ei ole tietyllä tasolla
- Sille löytyy alue, jossa se todennäköisimmin on (orbitaali)

- Monielektroniatomimallin täsmällisten tilojen laskeminen on hankalaa
- Voidaan tehdä hyviä arvioita monielektroniatomien kvantittuneille energiatiloille ja elektronien esiintymistodennäköisyyksille
-
Paulin kieltosääntö antaa ehdon kvanttimekaaniselle atomimallille
- Saman atomin elektronit eivät voi olla samassa tilassa eli niillä ei voi olla täsmälleen samat kvanttiluvut
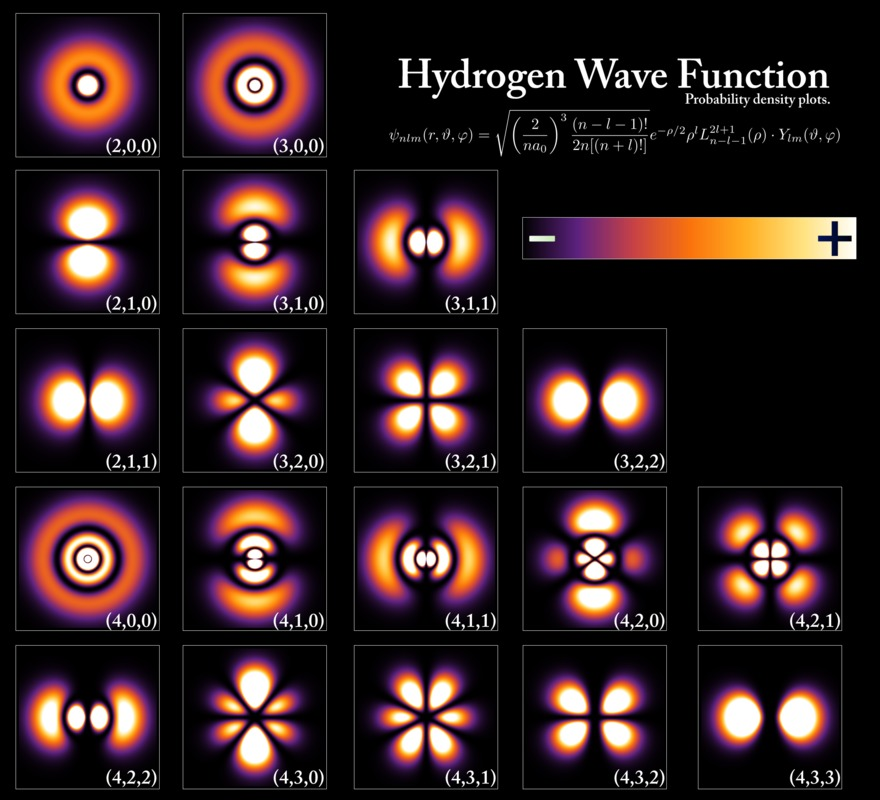
Elektronin sijainnin todennäköisyysjakaumia eri energiatiloilla ja vedyn aaltofunktio
Elektronien sijoittuminen orbitaaleille
- Minimienergiaperiaate
- Elektronit asettuvat orbitaaleille alimpiin mahdollisiin energiatiloihin
- Paulin kieltosääntö
- Kahdella elektronilla ei voi olla täysin sama energiatila: yhdelle orbitaalille mahtuu 2 elektronia, joilla eri spin
- Jokaisella elektronilla oma neljän kvanttiluvun yhdistelmä
- Hundin sääntö
- Elektronit sijoittuvat energialtaan samanarvoisille orbitaaleille samansuuntaisin spinein niin pitkälle kuin mahdollista
Atomin virittyminen ja viritystilan purkautuminen
- Atomit tai molekyylit voivat absorboida energiaa tai emittoida fotonin
- Siirtyminen alemmalta energiatasolta ylemmälle vaatii energiaa (absorptio)
- Siirtyminen ylemmältä alemmalle orbitaalille vapauttaa energiaa (emissio)
- Vapautuvan energian määrästä riippuu, havaitaanko tämä röntgen-, UV-, VIS- vai IR-säteilynä
-
Esim. revontulissa happi ja typpi virittyvät, ja viritystilojen purkautuminen havaitaan näkyvän valon alueella punaisena ja vihreänä valona
- Typpi: 391 nm (violetti) ja 473 nm (sininen)
- Happi: 558 nm (vihreä) ja 630 nm (oranssi)
- Esim. röntgensäteilyä voi syntyä mm. kohtiomateriaalin elektronin siirtymistä
-
Esim. revontulissa happi ja typpi virittyvät, ja viritystilojen purkautuminen havaitaan näkyvän valon alueella punaisena ja vihreänä valona
Emittoituvan tai absorboituvan fotonin aallonpituus
- Fotonin energian täytyy olla yhtä suuri kuin elektronin kahden energiatilan erotus
- Toisaalta fotonin energia on
- Aallonpituudeksi saadaan
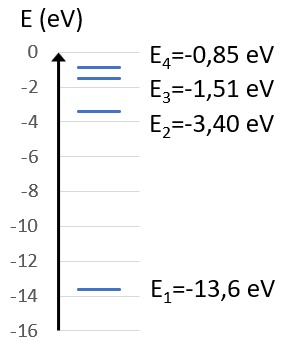
Vety:
Luminesenssi
- Fotoni virittää atomin
- Viritystila purkautuu asteittain
- Siirryttäessä tilalta toiselle emittoituu fotoni
- Fluoresenssissa viritystila purkautuu nopeasti (nanosekuntien kuluessa), fosforenssissa viiveellä
- Luminesenssia käytetään esim.
- Loisteputkissa (elohopean emittoima UV-säteily muutetaan putken sisäpinnan fluoresoivalla pinnoitteella näkyväksi valoksi)
- Hätäpoistumisteiden opasteissa, kellotaulujen viisareissa
- Lääketieteessä leikkausten kuvantamistekniikkana
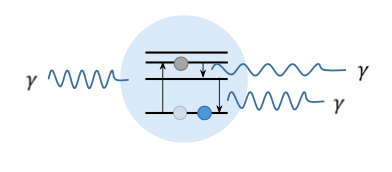
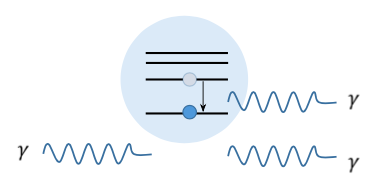
Stimuloitu emissio eli laser
- Elektroneja on viritetty samaan viritystilaan
- Viritystilan purkautuessa syntyy fotoneja
- Virittyneen atomin "ohittava" fotonin purkaa viritystilan
- Syntyvän uuden fotonin vaihe, energia ja aallonpituus ovat samoja kuin viritystilan purkaneella fotonilla
- Fotonit heijastuvat peilien avulla putkessa ja yhä uusia viritystiloja purkaantuu
- Syntynyt säteily lasketaan läpi yhdestä aukosta, joka on lasersäde (laser eli Light Amplification by the Stimulated Emission of Radiation)
- Laser on monokromaattista (vain yhtä aallonpituutta) sekä koherenttia (samassa vaiheessa) valoa
Atomin rakenne
- Atomin massa on keskittynyt sen ytimeen
- Ytimen hiukkasia (protonit ja neutronit) kutsutaan nukleoneiksi
- Ydintä ympäröi elektroniverho
- Protoni ja neutroni muodostuvat kolmesta kvarkista
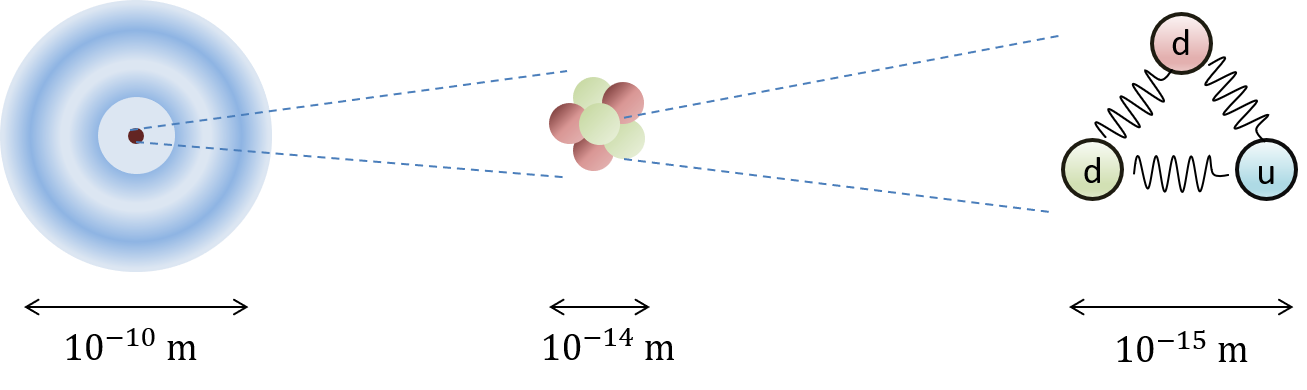
d-kvarkin varaus on -1/3 e, u-kvarkin +2/3 e.
Protonin varaus on +1 e, elektronin -1 e. Neutronilla ei ole varausta.
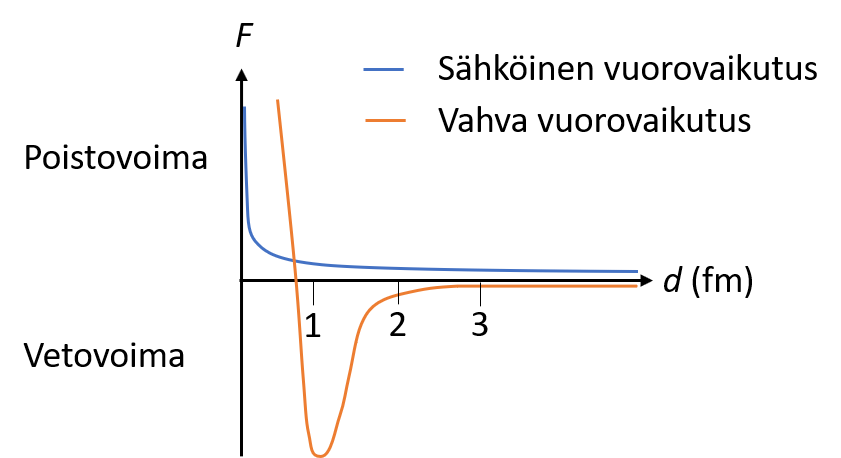
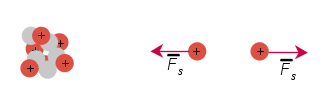
Ytimen vuorovaikutuksista
- Protonien välinen sähkömagneettinen vuorovaikutus pyrkii työntämään protoneja erilleen
- Kvarkkien välinen vahva vuorovaikutus pitää ydintä koossa (ydinvoima)
- Kun ydinhiukkaset ovat riittävän lähellä toisiaan, ne voivat tuntea naapurihiukkasen vahvan vuorovaikutuksen
- Ydin pysyy koossa, kun ydinvoima (vetovoima) on voimakkaampi kuin sähköinen poistovoima
Atomien merkitseminen
- Atomiytimet eroavat toisistaan protonien ja neutronien lukumäärän kautta
- Merkintä usein lyhennetään, koska kemiallinen merkki kertoo protonien lukumäärän
X = alkuaineen kemiallinen merkki
A = massaluku eli protonien ja neutronien yhteismäärä
Z = järjestysluku eli protonien lukumäärä
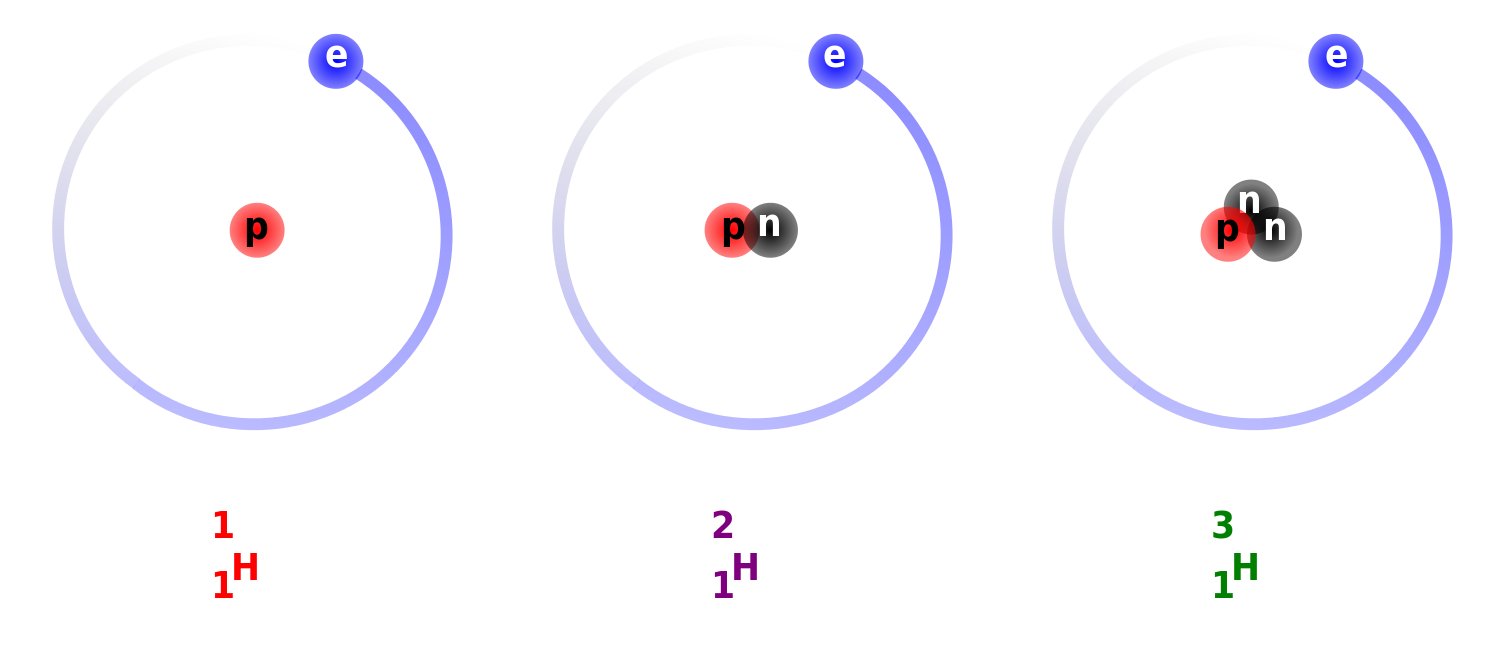
Isotooppi
- Protonien lukumäärän pysyessä samana alkuaine ei muutu
- Samalla alkuaineella voi olla eri määrä neutroneita
- Tällaiset saman alkuaineen atomit, joissa neutroneita on eri määrä, ovat alkuaineen isotooppeja
- Monesti alkuaineella on vain yksi isotooppi, joka on pysyvä
- Muut hajoavat radioaktiivisesti
- Vedyn erikoiset isotoopit: deuterium ja tritium
Atomimassayksikkö
- Suurin osa atomin massasta on sen ytimessä
- Atomin massa on suunnilleen protonien ja neutronien yhteismäärä (massaluku) kerrottuna yksittäisen protonin tai neutronin massalla
- Atomimassayksikkö u on massan lisäyksikkö
- Määritelmän mukaan hiilen C-12 -isotoopin massa on tasan 12 u
- 12 grammaa hiili-12 -atomeja sisältää yhden moolin verran hiiliatomeja
- 12 grammassa hiiltä on siis Avogadron luvun verran hiiliatomeja
- Määritetään yksi atomimassayksikkö kilogrammoissa:
Massavaje
-
Atomiytimen massa on aina pienempi kuin ytimen muodostavien hiukkasten yhteenlaskettu massa
- Eroavuutta kutsutaan massavajeeksi
- Suhteellisuusteorian mukaan massalla ja energialla on yhteys
- Yhtälö kertoo, että kun kappaleella on massaa, sillä on tietty määrä energiaa, vaikka se olisi levossa
- Käänteisesti; vaikka fotonin lepomassa on nolla, on sillä liike-energiaa
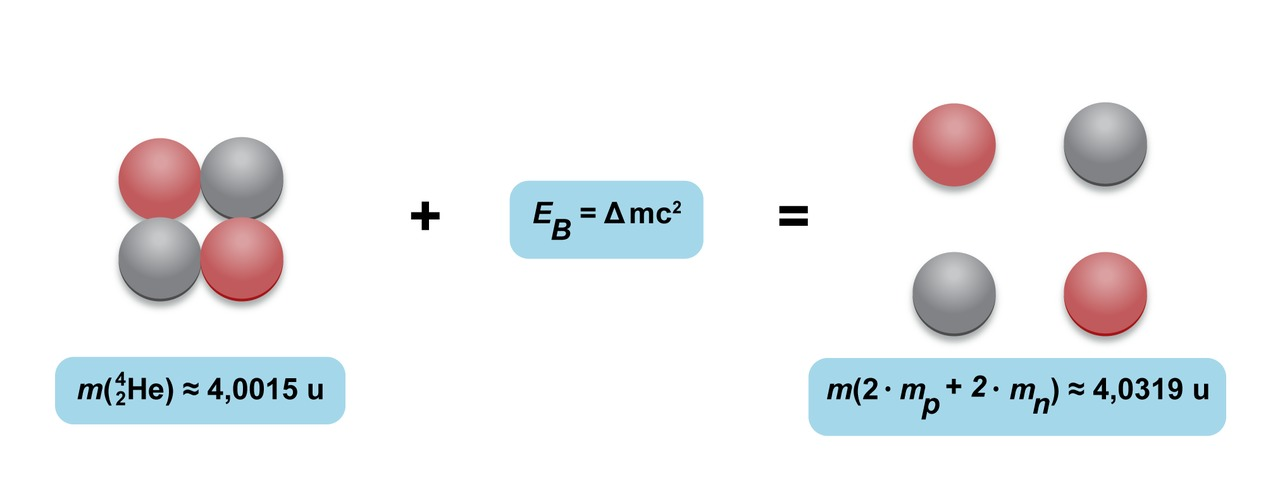
Sidosenergia
- Kun kahdesta protonista ja kahdesta neutronista muodostuu heliumatomin ydin (alfahiukkanen), ympäristöön vapautuu energiaa
- Energian suuruus voidaan laskea massavajeen avulla
- Sidosenergia on ytimen hajottamiseen vaadittu energia (tai ytimen muodostuessa vapautuva energia)
- Massavaje on vapaiden hiukkasten ja niiden muodostaman atomin massojen erotus
Atomimassayksikkö ja energia
- Yhtä atomimassayksikköä 1 u vastaava energia on
- Kun muutetaan energian yksikkö joule J elektronivolteiksi eV, saadaan
- Näin esim. Fe-56 -sidosenergia voidaan laskea
Sidososuus
-
Sidosenergian määrä kasvaa, kun aineen massaluku A kasvaa
- Atomiytimessä ytimen rakenneosien välisten sidosten määrä kasvaa
- Sidososuudella tarkoitetaan sidosenergian määrää nukleonia (eli protonia tai neutronia) kohden
- Sidosenergia tarkoittaa keskimääräistä energiaa, jota ytimeen pitäisi tuoda, jotta sieltä saataisiin irrotettua yksi nukleoni
- Sidososuus on pienempi esimerkiksi -ytimellä kuin ytimillä ja
ENERGIAA
(hypoteettinen reaktio, luonnollisessa fissiossa osa neutroneista vapautuu)
Eri ydinten sidososuudet
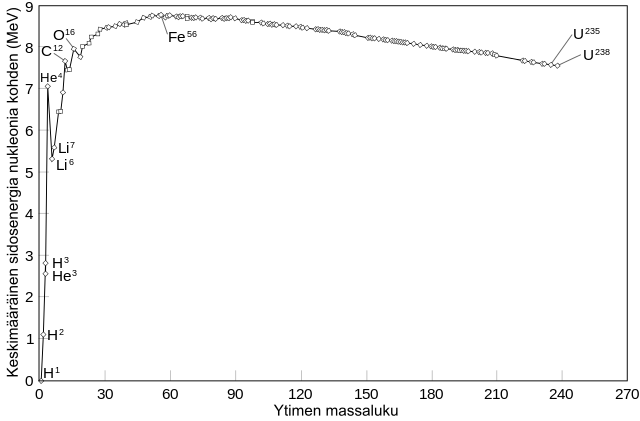
Suurin sidososuus on raudalla. Ydinmuutokset pyrkivät tapahtumaan kohti rautaa.
Fissio
Fuusio
Radioaktiivisuus
- Suurin osa isotoopeista on radioaktiivisia eli ne hajoavat itsestään
- Hajoamisessa vapautuu energiaa
- Hiukkasten liike-energiana
- Sähkömagneettisena säteilynä
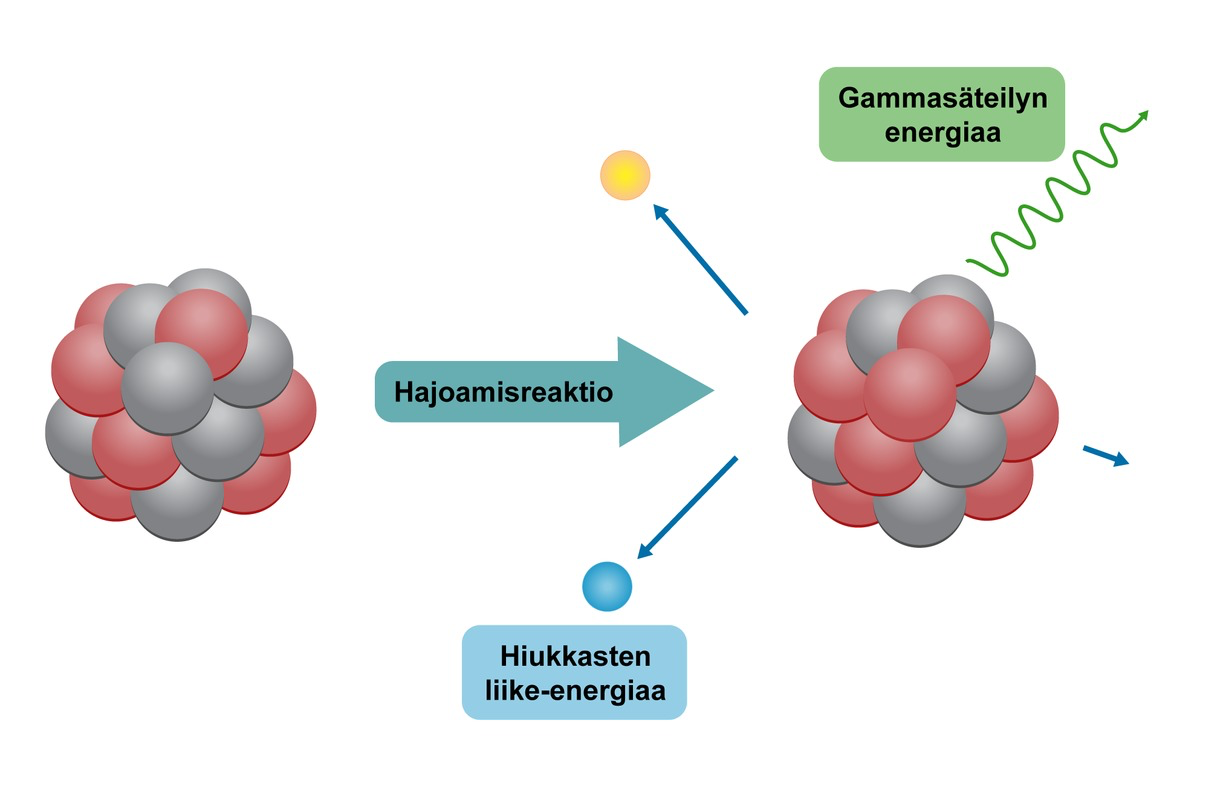
Radioaktiivinen hajoaminen
- Hiukkassäteily:
- α- ja β-hajoamisessa syntyy liikkuvia hiukkasia
- Suurin osa isotoopeista on α- tai β-aktiivisia
- Radioaktiiviset ytimet lähettävät myös gammasäteilyä ytimen viritystilan purkautuessa
- Ydinsäteily (syntynyt ytimesta: α, β, γ, n) ionisoi atomeja
- Kemialliset ominaisuudet muuttuvat
- Voi seurata haitallisia biologisia muutoksia elävissä kudoksissa

Tyypilliset hajoamistavat
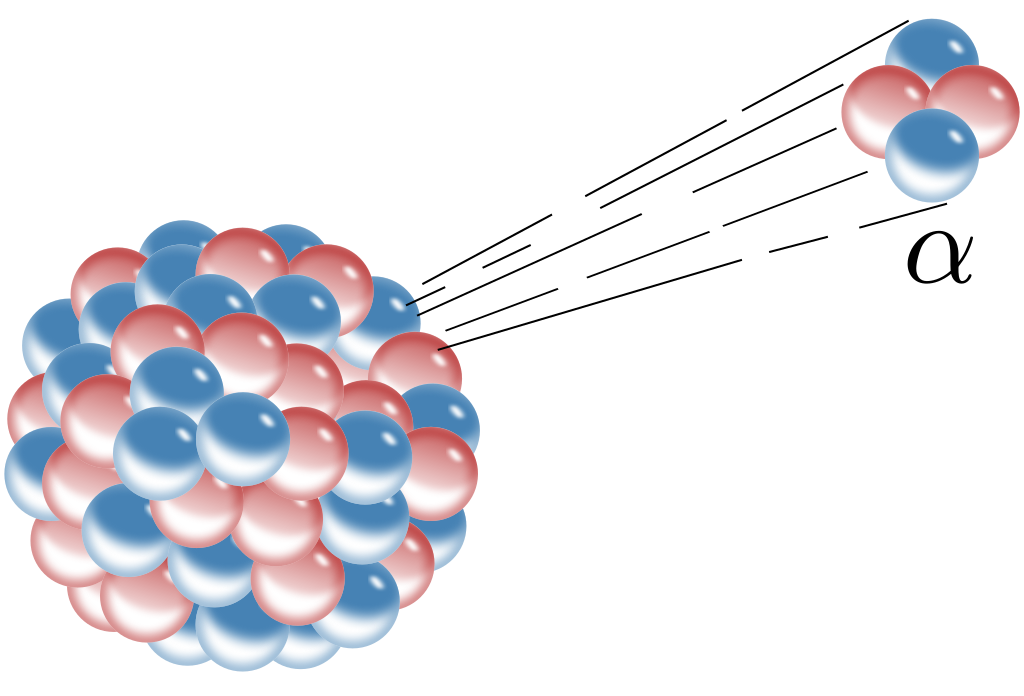
- Alfahajoaminen
- Ytimestä lähtee heliumatomin ytimiä (suuri sidosenergia)
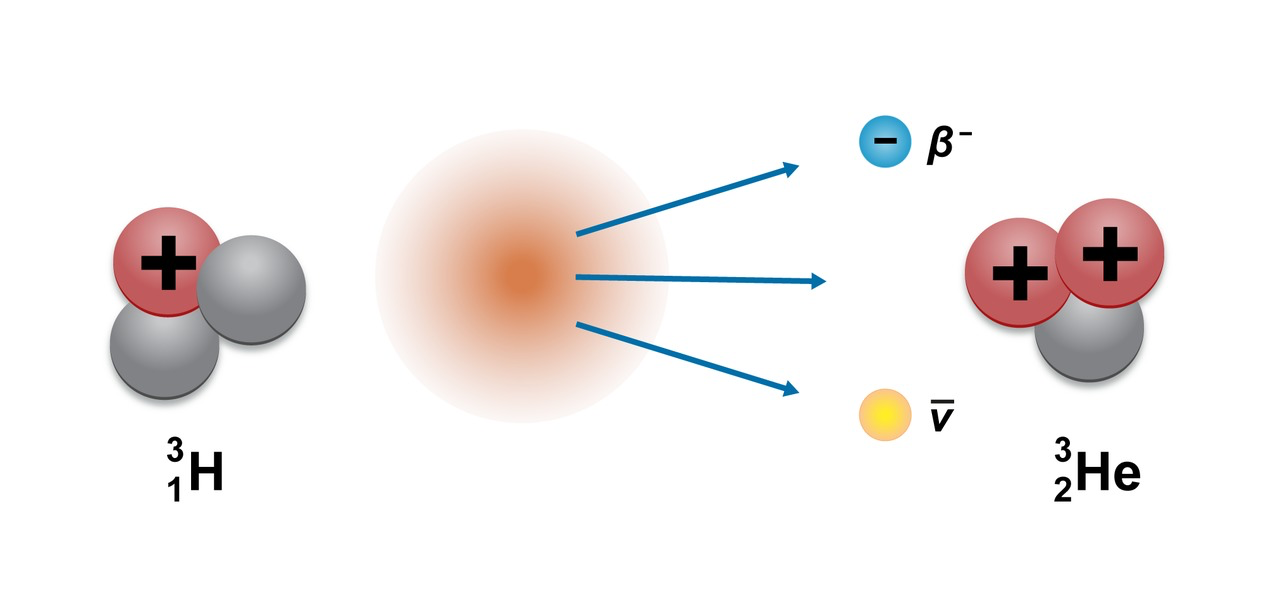
- Beetahajoaminen
- β- : Neutroni muuttuu protoniksi, samalla vapautuu elektroni ja antineutriino
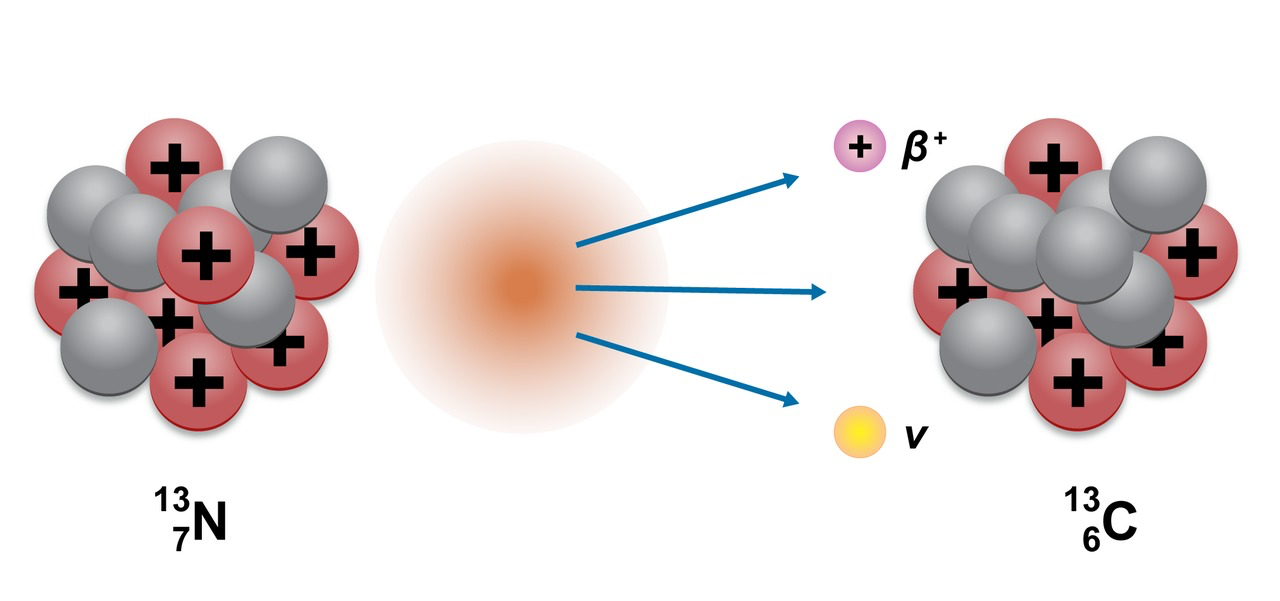
- β+ : Protoni muuttuu neutroniksi, samalla vapautuu positroni ja neutriino
- Gammasäteily
- Radioaktiivisten ytimien viritystila purkautuu
Hajoamisenergia
- Hajoamisessa vapautunut energia Q syntyy massan muutoksesta
- Hajoamistapahtuma esitetään reaktioyhtälön kautta
+
Alfahajoaminen
- Hajoamisessa atomi siirtyy sidosenergialtaan kohti edullisempaa tilaa
- Ytimestä lähtee heliumatomin ytimiä, koska niillä on suuri sidosenergia
- Se on "edullisempaa" kuin protonin tai neutronin poistuminen
- Hajoamisessa syntyneen tytärytimen massaluku pienenee neljällä ja järjestysluku kahdella
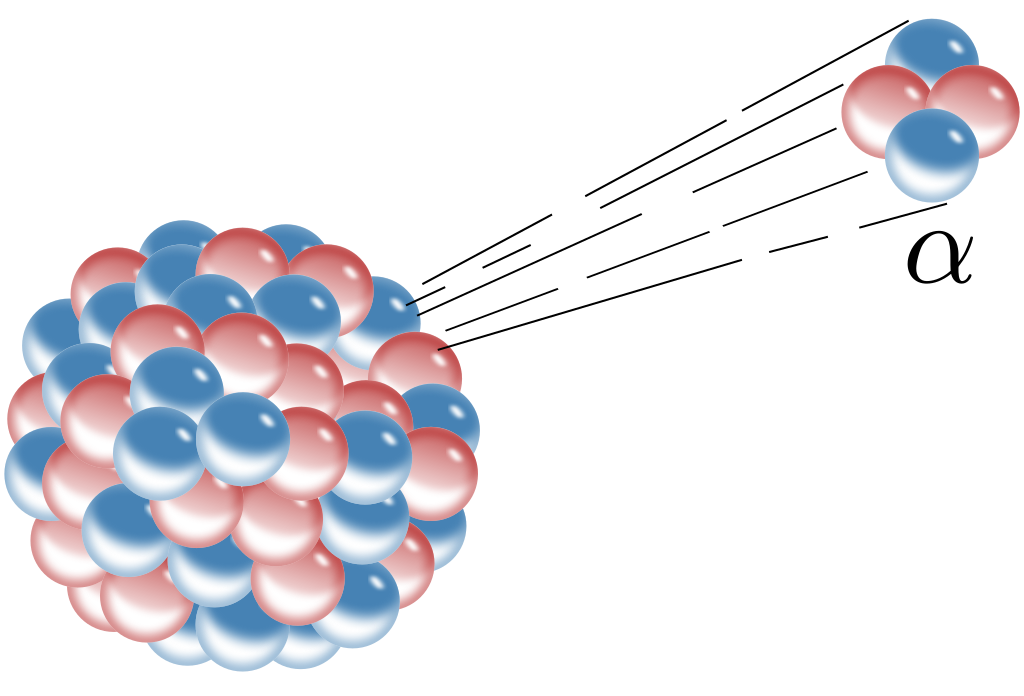
Lähtöydin
Syntyneet ytimet
Alfahajoaminen
- Alfasäteily kulkee ilmassa senttimetrejä
- Pysähtyy paperiin
- Luovuttaa energiansa pienelle alueelle
- On elimistöön joutuessaan vaarallista (esim. radon)
- Hajoamisessa vapautuva energia muuttuu hiukkasten liike-energiaksi sekä jättää tytäratomin virittyneeseen tilaan
- Viritystilan purkautuessa vapautuu gammakvantti eli gammasäteilyä
- Jos oletetaan, että ytimen virittymistä ei tapahdu ja atomi on paikallaan hajotessaan, voidaan määrittää hiukkasten saamat nopeudet
- Reaktiossa säilyy energian lisäksi myös liikemäärä
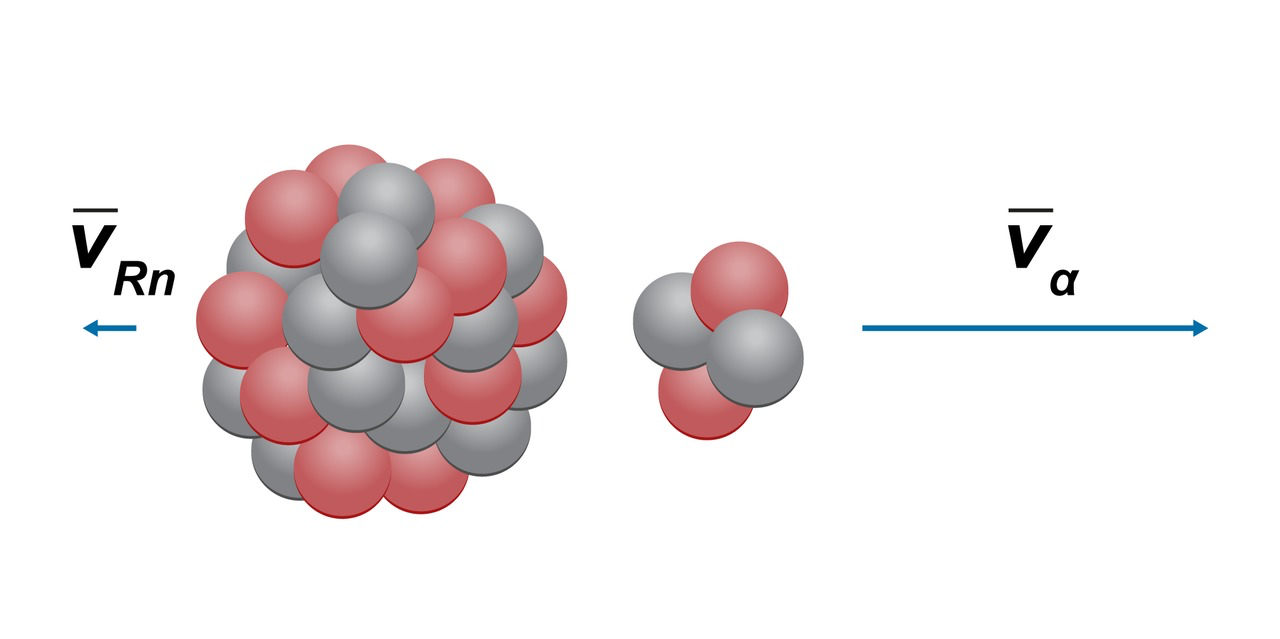
Beetahajoaminen
- Heikon vuorovaikutuksen seurauksena kvarkki voi muuttua toiseksi kvarkiksi
- Atomiytimessä neutroni voi muuttua protoniksi tai protoni neutroniksi
- β- -hajoaminen: neutroni muuttuu protoniksi, elektroniksi ja antineutriinoksi
- β+ -hajoaminen: protoni muuttuu neutroniksi, positroniksi ja neutriinoksi
Beetahajoaminen
- Beetahajoamisissa massaluku ei muutu
- Myös beetahajoamisessa ydin voi jäädä virittyneeseen tilaan
- Syntyy gammasäteilyä
- Beetasäteily kantaa pidemmälle kuin alfasäteily, mutta ionisoi heikommin
- Pysähtyy muovilevyyn
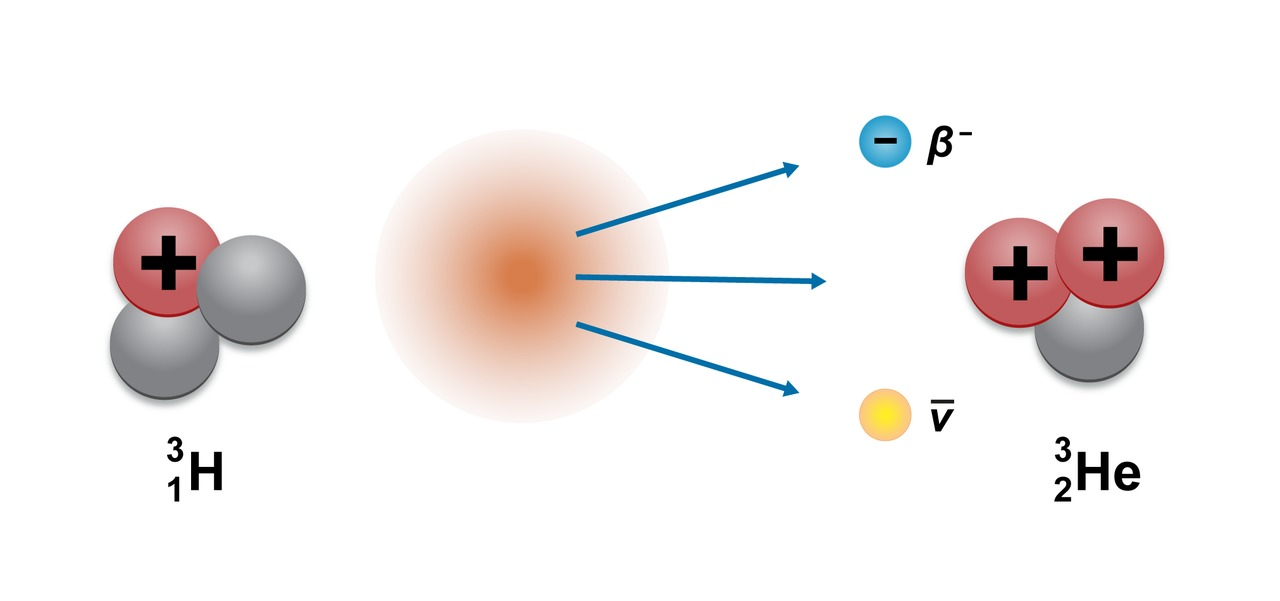
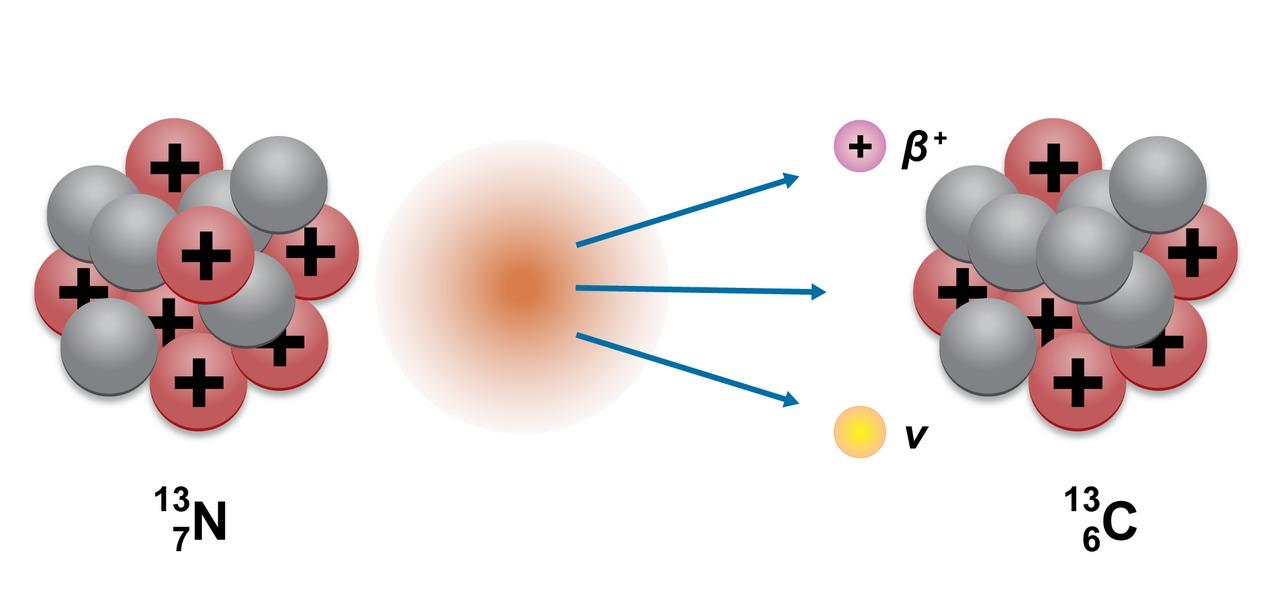
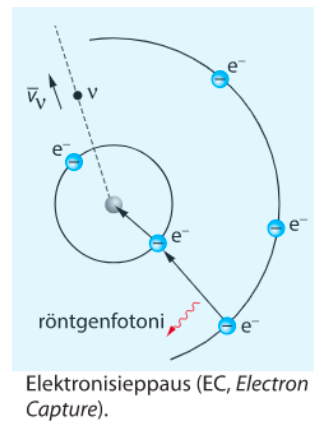
Elektronisieppaus
- Ydin sieppaa alimmalta elektronikuorelta elektronin, joka muodostaa ytimessä olevan protonin kanssa neutronin
- Neutroni jää atomin ytimeen ja vapautuu neutriino ja röntgen- tai gammasäteilyä
- Elektronisieppaus tapahtuu sitä todennäköisimmin mitä suuremmaksi atomi järjestysluku kasvaa
- Tällöin ytimen sähkökenttä voimistuu
Spontaani fissio
- Spontaanissa fissiossa raskas ydin hajoaa kahdeksi keskiraskaaksi ytimeksi
- Luonnossa mm. U-238 hajoaa spontaanilla fissiolla
- Keinotekoisesti valmistetuilla spontaani fissio on yleisempää
Neutronisäteily
Neutronisäteily
- Koostuu vapaista neutroneista
- Voi syntyä esim. spontaanin fission kautta ja fuusioreaktioissa
- Fuusioituvissa ytimissä täytyy olla yhteensä enemmän neutroneja kuin on tarpeen syntyvän uuden ytimen kannalta
- Vapaat neutronit hajoavat heikon vuorovaikutuksen seurauksena protoniksi, elektroniksi ja antineutriinoksi
Hajoamisreaktiot kootusti
Alfahajoaminen
Beeta- -hajoaminen
Beeta+ -hajoaminen
Elektronisieppaus
Ei taulukko-
kirjassa!
Aktiivisuus
- Radioaktiivisen aineen atomit hajoavat satunnaisesti
- Kullakin radioaktiivisella isotoopilla on ominainen todennäköisyys, jolla se hajoaa
- Ei voida ennustaa yksittäistä ytimen hajoamista
-
Aktiivisuus kuvaa radioaktiivisen aineen hajoamisnopeutta
- Se ilmoittaa hajoamisten lukumäärän yhdessä sekunnissa
- Hajoamisvakio kuvaa ytimen hajoamisen todennäköisyyttä aikayksikössä
- Suuri todennäköisyys hajoamiselle suuri lyhytikäinen isotooppi
Hajoamislaki
Hajoavien ytimien lukumäärä
Aktiivisuus
Puoliintumisaika
- Puoliintumisajan kuluessa puolet alkuperäisistä ytimistä on hajonnut
- Kun ytimien määrä puolittuu, puolittuu myös aktiivisuus
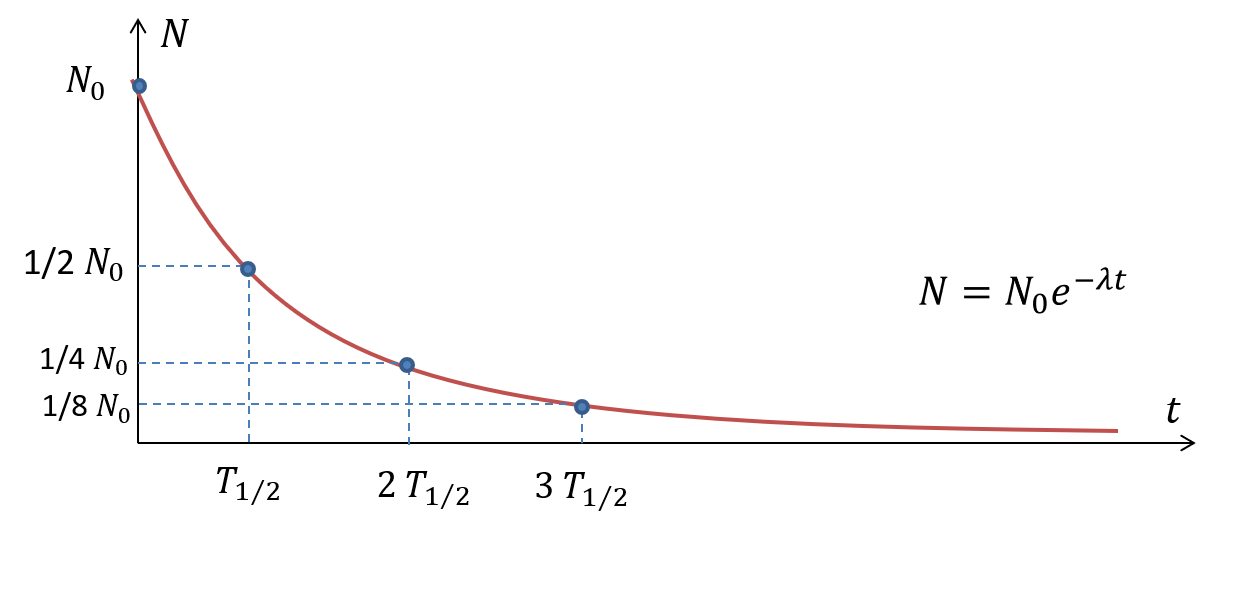
1 puoliintumis-aika
2 puoliintumis-aikaa
3 puoliintumis-aikaa
puolet ytimistä jäljellä
neljäsosa ytimistä jäljellä
kahdeksasosa ytimistä jäljellä
Fissio ja fuusio
- Ydinenergiaa voi vapautua kahdessa ydinreaktiossa: fuusiossa ja fissiossa
-
Fissiossa yksi raskas ydin halkeaa kahdeksi radioaktiiviseksi ytimeksi, jolloin vapautuu myös neutroneita
- Syntyneiden ytimien yhteenlaskettu sidosenergia suurempi kuin alkuperäisen ytimen (massaa muuntuu energiaksi)
-
Fuusiossa kaksi toisiinsa törmäävää kevyttä ydintä yhdistyvät
- Energia syntyy ytimen hiukkasten (protonien ja neutronien) sidosenergian vapautuessa
- Kaikkien tähtien energia on fuusioenergiaa
- Yksittäinen fissioreaktio vapauttaa 10–15 kertaa enemmän energiaa kuin yksittäinen fuusioreaktio
- Fissiossa vapautuu enemmän energiaa tapahtumaa kohden
- Fuusiossa vapautuu enemmän energiaa nukleonia kohden
- Fuusio on tehokkaampi ydinreaktio
Ydinvoimala ja fissioreaktorit
- Ydinvoimala on lämpövoimalan kaltainen voimalaitos (suuri vedenkeitin)
- Lämpö saadaan kontrolloiduista atomiytimien hajoamisketjusta, ketjureaktiosta
- Ydinpolttoaineena käytetään uraania
- Uraania rikastetaan eli U-235 -isotoopin suhteellista määrää lisätään
- Uraaninapit kootaan sauvoiksi, joiden käyttöikä on muutama vuosi
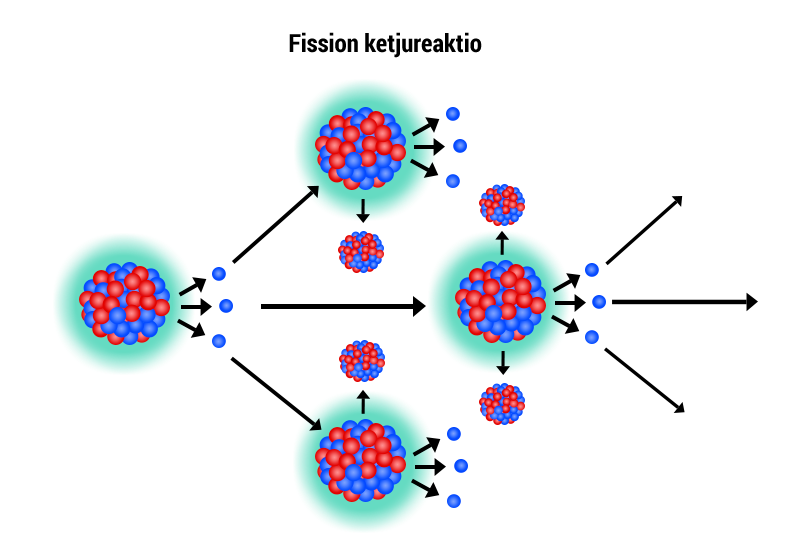
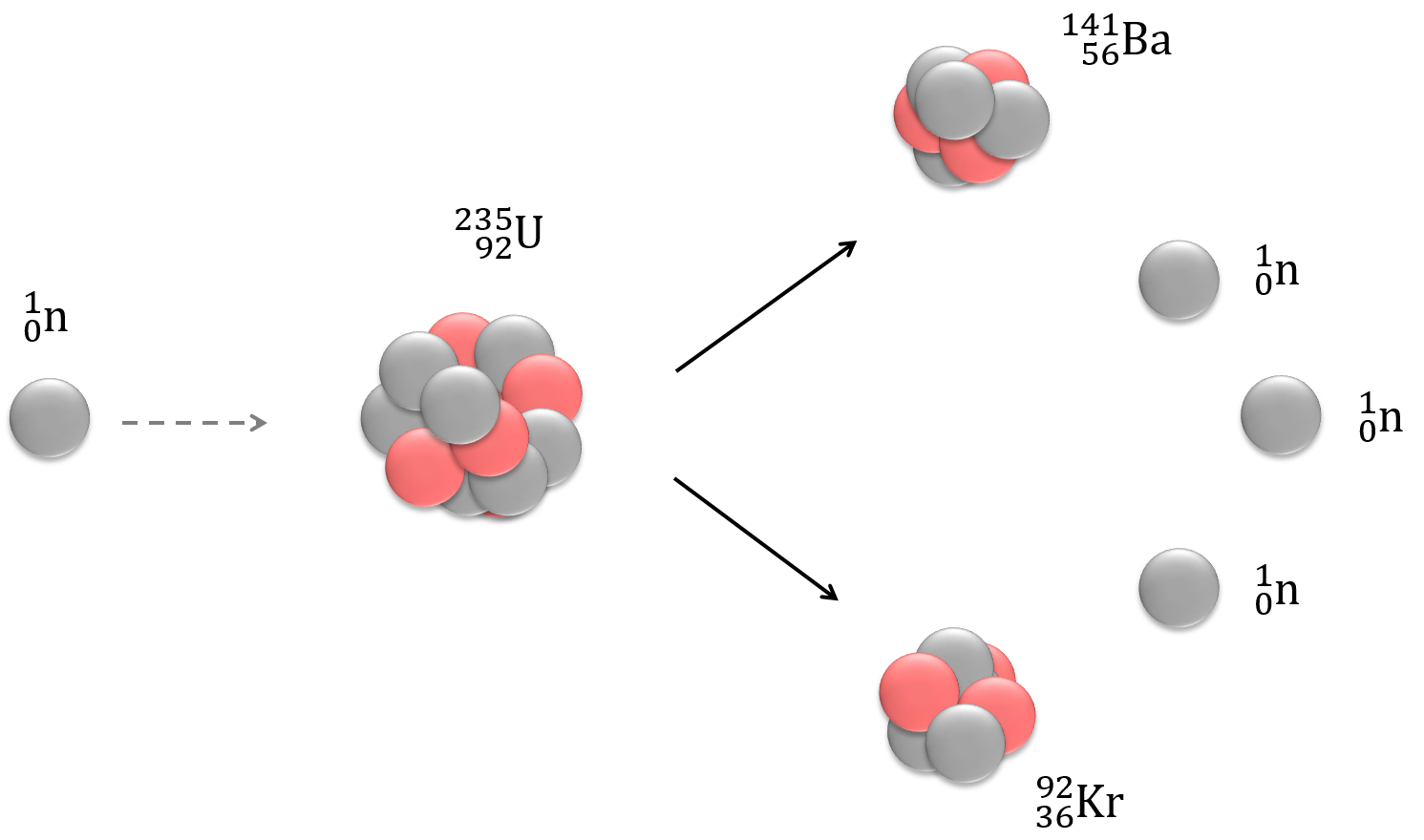
+ ENERGIAA
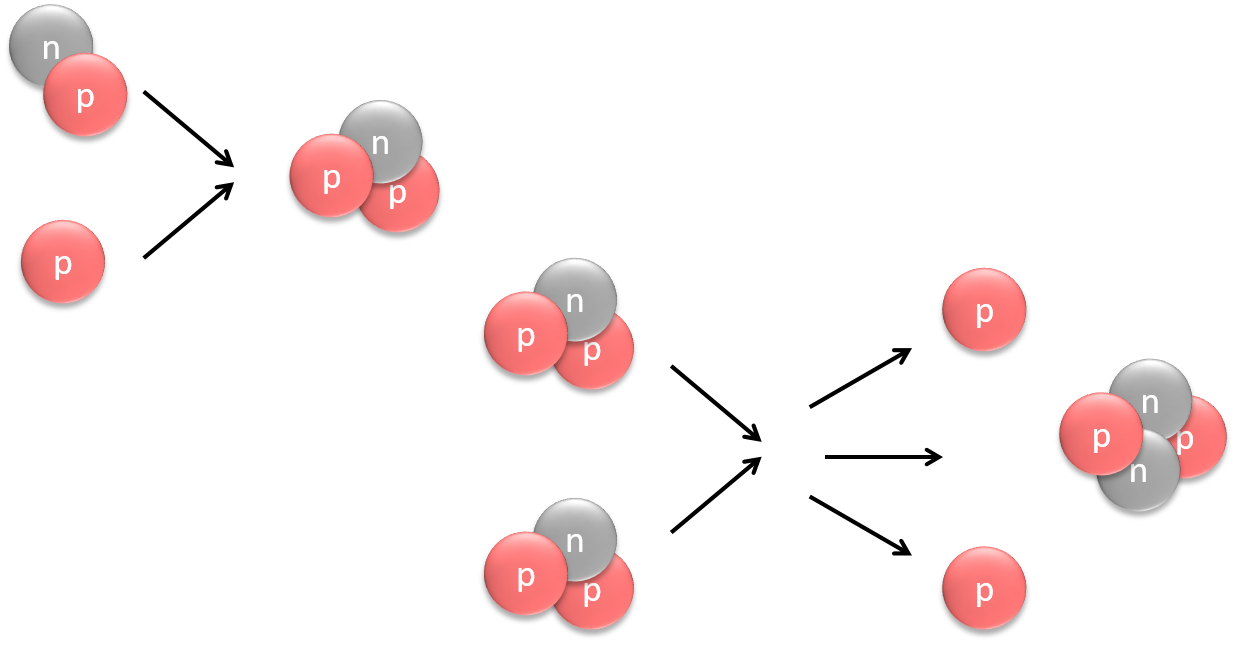
Fuusiovoima
- Ydinfuusiossa ytimet yhtyvät toistensa kanssa
- Aurinko tuottaa energiansa fuusioimalla vetyä heliumiksi
- Keskeinen elämän edellytys maapallolla
- Fuusiolla on ollut keskeinen merkitys maailmankaikkeuden vetyä raskaampien alkuaineiden synnyssä
- Ranskaan on rakenteilla maailmanlaajuisessa yhteishankkeessa fuusiovoiman koelaitos (ITER)
- Tarkoitus valmistua vuoteen 2035 mennessä?
Fuusiovoiman hyödyt ja haasteet
- Fuusioreaktiossa käytettäviä aineita on helposti saatavilla
- Runsas energiantuotto ainekiloa kohti
- Reaktiossa syntyvä helium ei ole radioaktiivista
- Reaktioaineista tritium on radioaktiivista, mutta sen puoliintumisaika on vain 12,3 vuotta
- Reaktioaineita ei tarvitse kuljettaa voimalaan, vaan ne voidaan valmistaa paikan päällä
-
Fuusiovoimalan suurimpana haasteena on korkean lämpötilan tuottaminen (100 miljoonaa astetta)
- Vasta näin kuumassa reaktio kuluttaa vähemmän energiaa kuin siitä saadaan
- Kuumuutta ja neutronisäteilyä kestävät materiaalit, jäähdytys
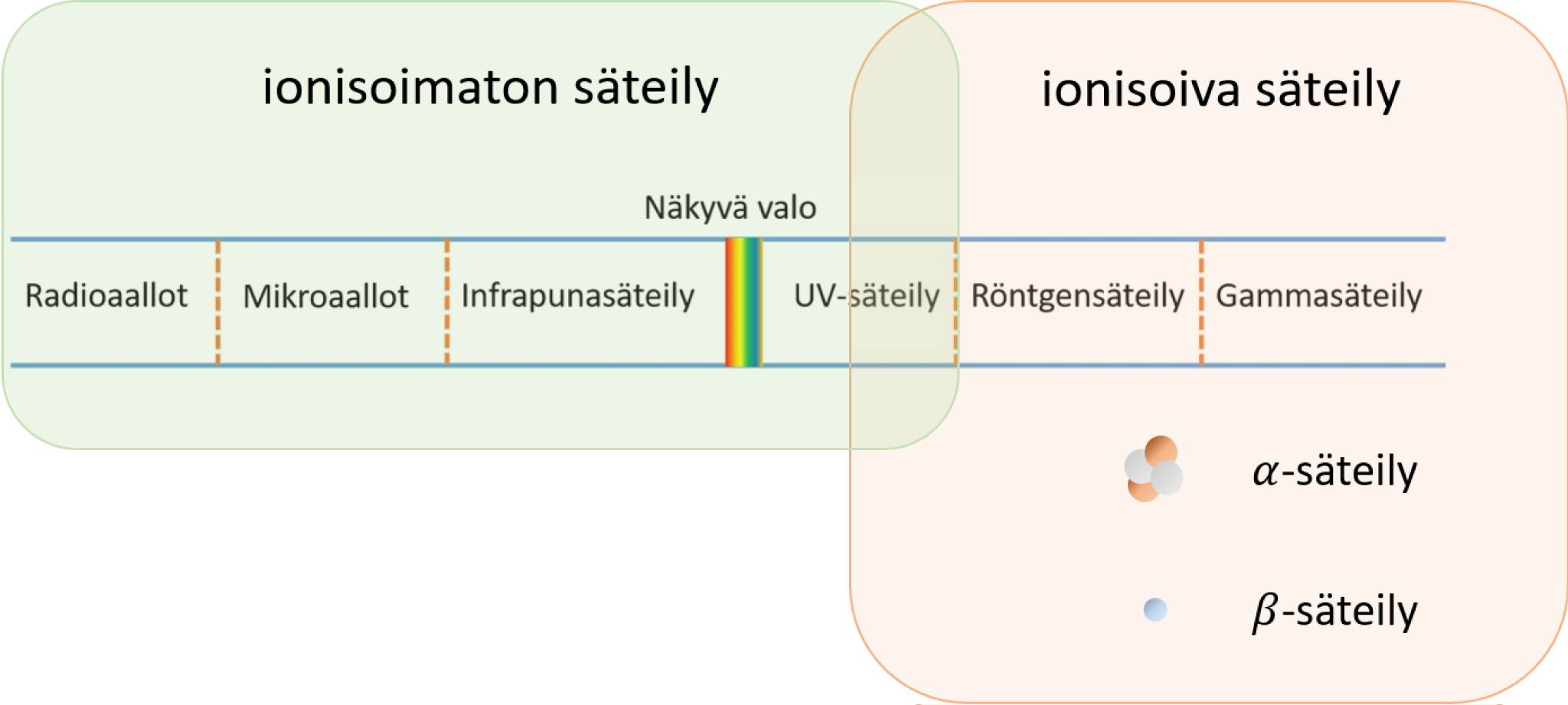
Ionisoiva säteily
- Ionisoivalla säteilyllä on riittävästi energiaa irroittamaan atomeista elektroneja tai rikkomaan aineen molekyylejä
- Muuttaa aineiden kemiallisia ominaisuuksia ja voi aiheuttaa häiriöitä solujen toiminnassa
- Sähkömagneettisesta säteilystä röntgen- ja gammasäteily (sekä osa UV-säteilystä) on ionisoivaa
Gammasäteily
- Hyvin lyhytaaltoista sähkömagneettista säteilyä
- Suuri taajuus, suuri energia
- Radioaktiivisten ydinten lähettämää säteilyä
Atomiytimen virittyminen
- Radioaktiivisessa hajoamisessa atomiydin voi jäädä virittyneeseen tilaan
- Kaikki hajoamisessa vapautuva energia ei välttämättä siirry hajoamistuotteiden liike-energiaksi
- Osa energiasta voi varastoitua ytimeen
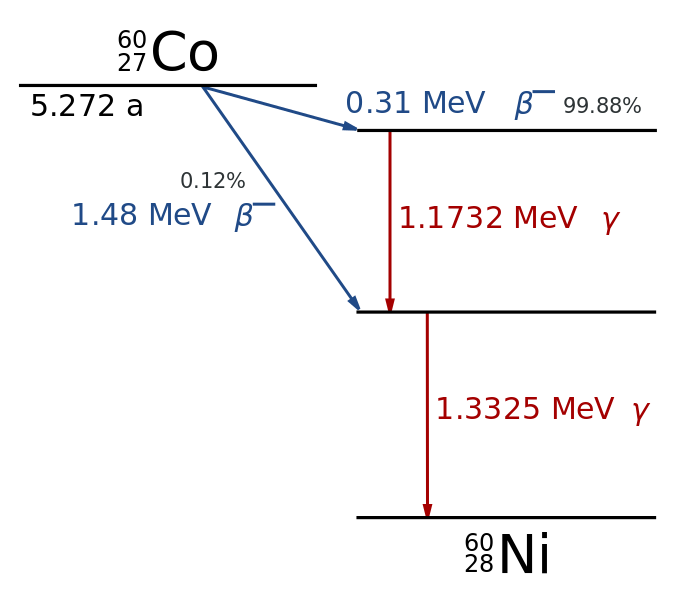
-
Ytimen viritystila purkautuu usein välittömästi
- Ytimen energiatilojen väliset erot ovat suuria (~ MeV)
- Tilan purkautuessa vapautuu gammasäteilyä
Vuorovaikutus aineen kanssa
- Gammasäteily vuorovaikuttaa aineen kanssa kolmella tavalla
- Valosähköinen ilmiö
- Comptonin sironta
- Parinmuodostus
- Vuorovaikutustapahtuman esiintymis-määrä riippuu ytimen järjestysluvusta ja gammasäteilyn energiasta
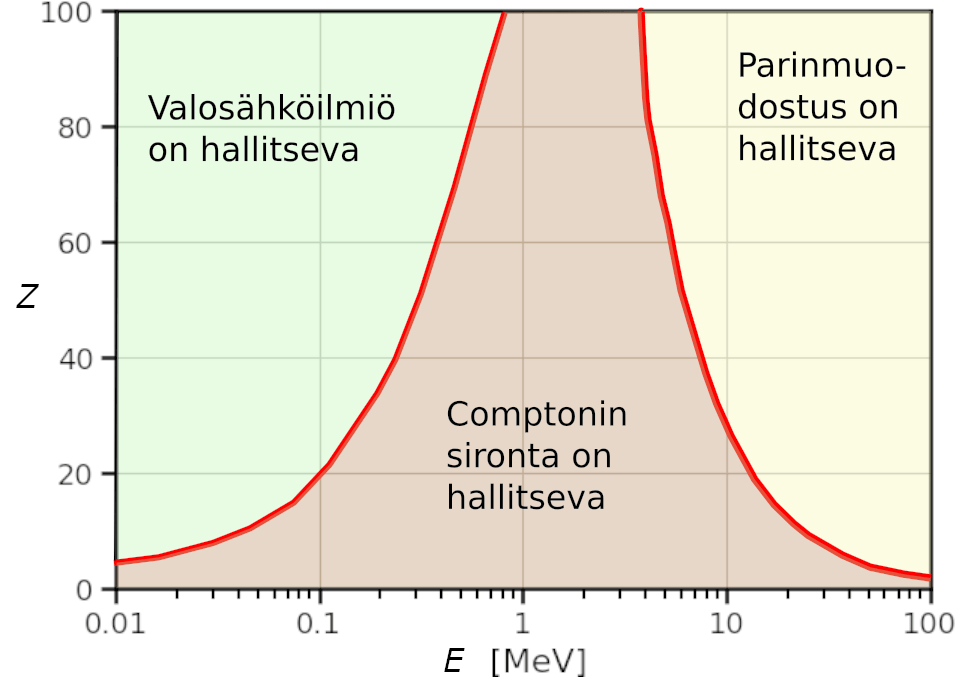
Kuva: YTL
- Parinmuodostuksessa fotoni vuorovaikuttaa atomiytimen kanssa ja muuttuu hiukkaseksi ja sen antihiukkaseksi
- Fotonin energia muuttuu hiukkasten massaksi ja liike-energiaksi
- Reaktio voi tapahtua vain, jos fotonin energia on suurempi kuin syntyvien hiukkasten lepoenergioiden summa
Gammasäteilyn vaimeneminen
- Gammasäteily vuorovaikuttaa pääasiassa elektronien kanssa
- Vaimenee parhaiten kulkiessaan raskaiden alkuaineiden läpi
- Kun gammasäteilyä tulee aineeseen, fotonit vuorovaikuttavat aineen kanssa absorboituen siihen
- Vuorovaikutustapahtumien kautta aineen läpäisseen säteilyn intensiteetti on heikentynyt
- Heikkeneminen on eksponentiaalista
- Riippuu väliaineesta ja säteilyn energiasta
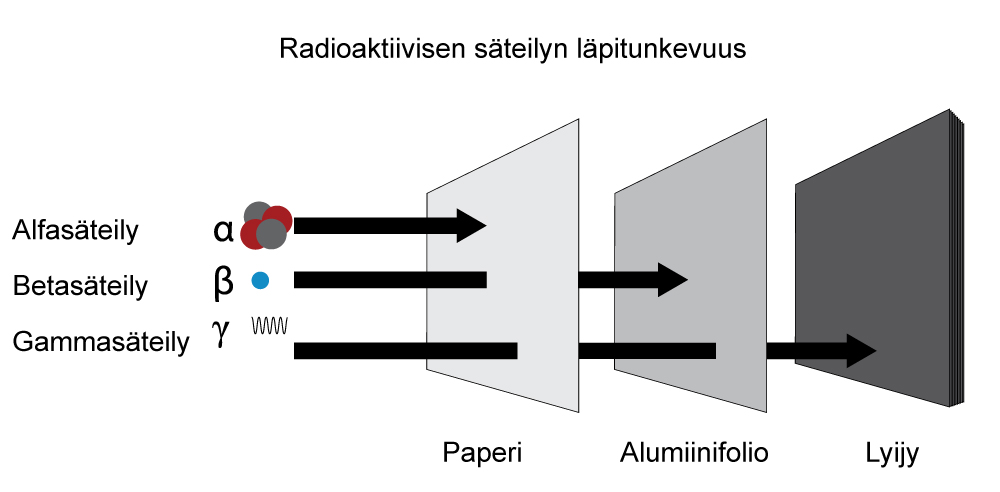
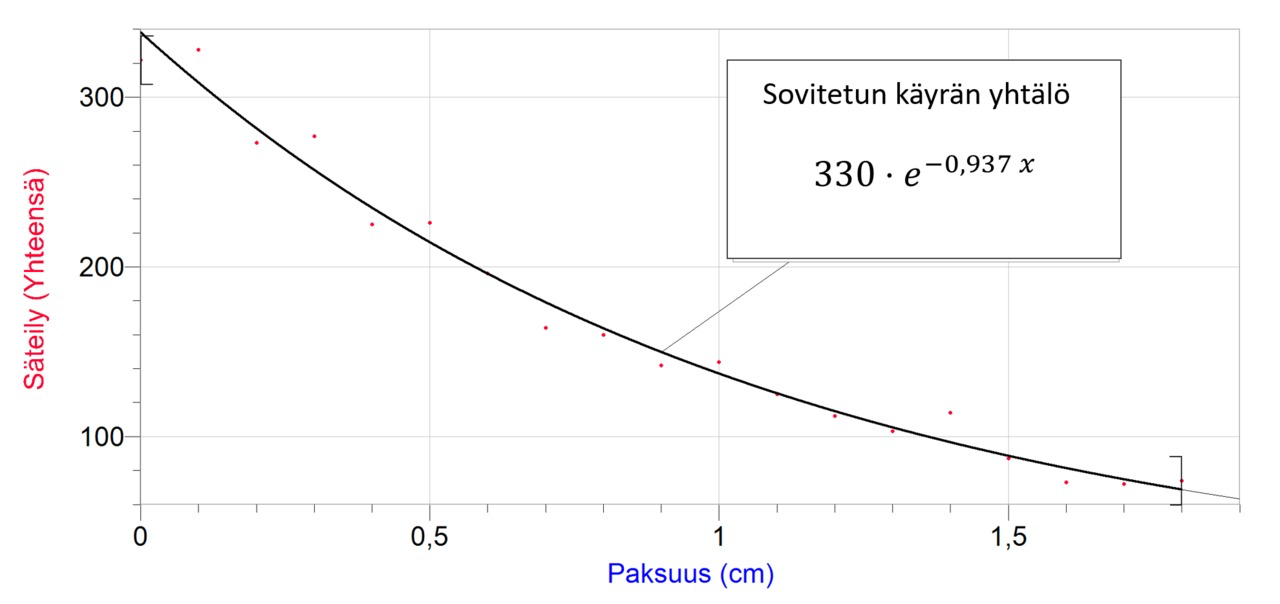
Gammasäteilyn vaimeneminen väliaineessa
Tarkista, että piirrät kuvaajaan oikean sovituksen!
Röntgensäteily
- Lyhytaaltoista sähkömagneettista säteilyä
- Aallonpituuden suuruusluokka noin
- Syntyy jarrutussäteilynä tai ominaissäteilynä
- Käytetään mm. lääketieteellisessä kuvantamisessa, tähtitieteessä ja aineen rakenteen tutkimisessa

Kuva: Wikipedia
Röntgensäteilyn synty
- Elektronit törmäävät metallikohtioon, jossa niiden liike hidastuu äkillisesti
- Kun elektronien liike-energian muutos on ollut riittävän suuri, syntyy lyhytaaltoista röntgensäteilyä
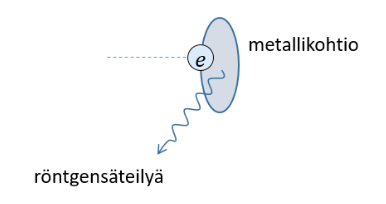
Röntgensäteilyn tuottaminen
- Mitä suurempi jännite, sitä lyhytaaltoisempaa säteilyä saadaan aikaan
- Kiihdytysjännitteet voivat olla suuruusluokkaa 100 kV
Röntgensäteilyn spektri
- Röntgenputken spektrissä havaitaan jatkuva osa sekä säteilypiikkejä
- Aallonpituuden alarajalta alkava jatkuva osa on jarrutussäteilyä
- Piikit ovat ominaissäteilyä
- Syntyy, kun elektronit irrottavat anodimetallin atomeista elektroneja
- Metalliatomin ylemmiltä tiloilta siirtyy elektroneja alemmille tiloille paikaten syntyneitä aukkoja atomi emittoi fotonin
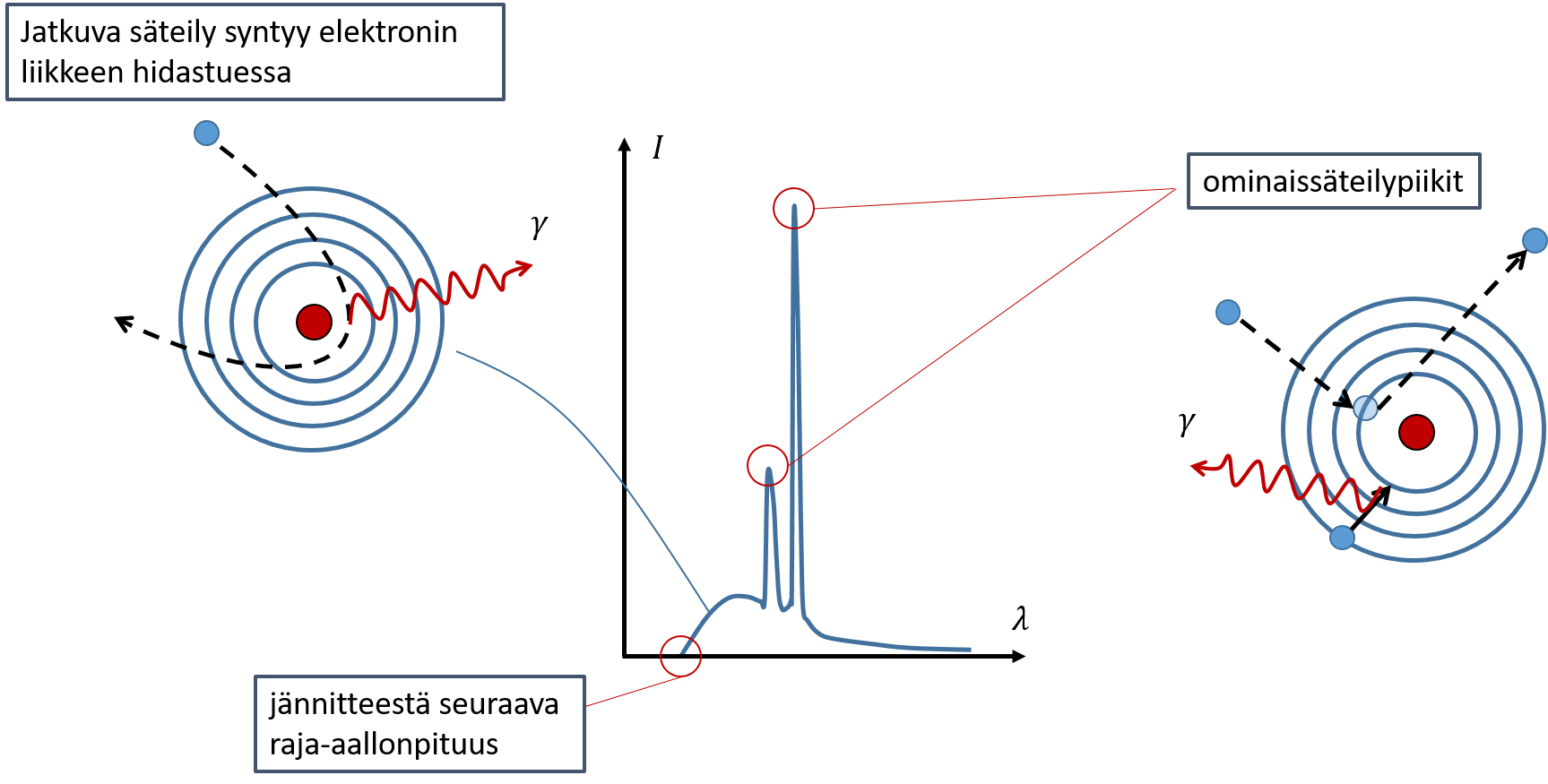

vrt. vetyatomi
Jarrutus-säteily
Ominais-säteily
Röntgensäteilyn spektri
- Spektrin aallonpituuden pienin arvo riippuu kiihdytysjännitteestä
- Mitä suurempi kiihdytysjännite, sitä lyhytaaltoisempaa säteilyä voidaan tuottaa
- Röntgensäteilyn spektri on jatkuva, koska kaikkien elektronien liike-energia ei muutu täysin säteilykvantiksi eli fotoniksi
- Iso osa muuttuu lämmöksi

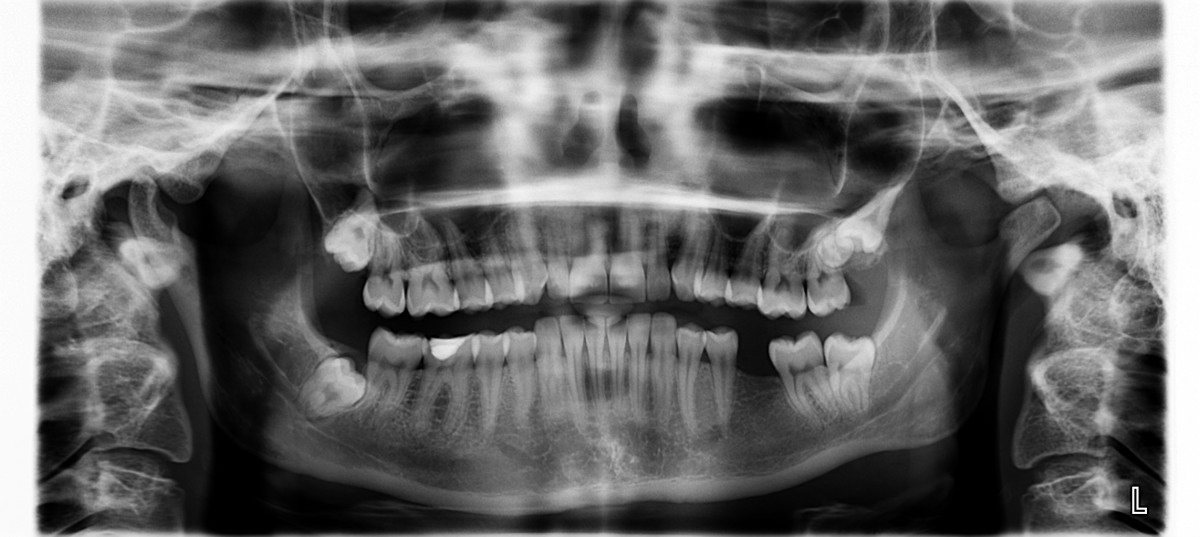
Röntgensäteily lääketieteessä
- Röntgensäteilyä käytetään lääketieteen kuvausmenetelmänä
- Perustuu eri aineiden kykyyn absorboida röntgensäteilyä
- Säteily läpäisee paremmin kudosta kuin luuta
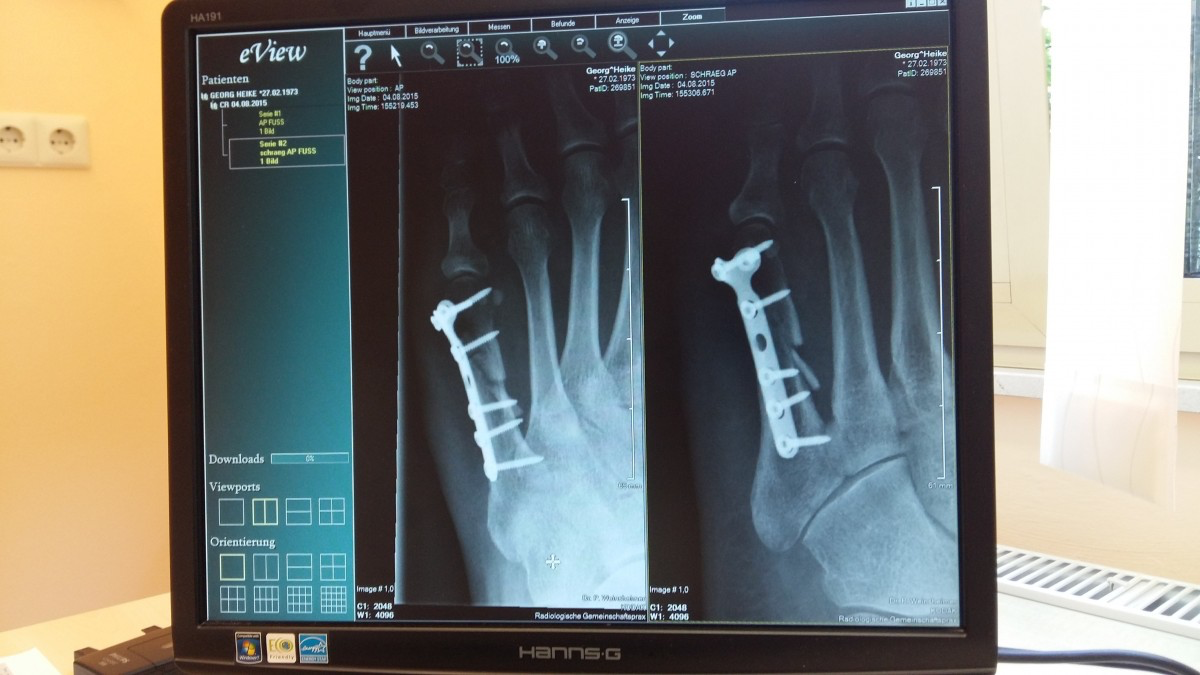
Kuvat: Pxhere / CC0
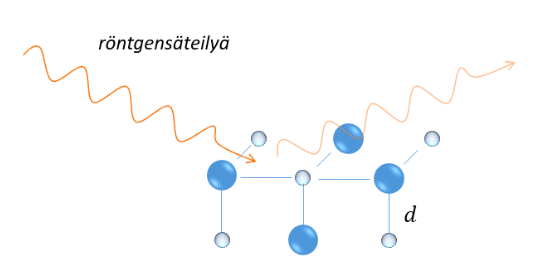
Röntgendiffraktio
- Aaltoliikkeelle tapahtuu diffraktio, kun se kulkee kapean raon läpi
- Raon kokoluokka on sama kuin aaltoliikkeen aallonpituus
- Aineiden rakenneosat ovat jäsentyneet säännöllisiksi hiloiksi
- Rakenneosasten välimatka on samaa suuruusluokkaa kuin röntgensäteiden aallonpituus
- Kun röngensäteet osuvat aineen pintaan, tapahtuu diffraktio
Säteilysuureita
-
Absorboitunut annos, yksikkö gray (Gy)
- Ilmoittaa säteilyn luovuttaman energian kilogrammaa kohti
-
Ekvivalenttiannos, yksikkö sievert (Sv)
- Absorboitunut annos kerrottuna säteilyn painotuskertoimella
- Huomioi, millaisesta säteilylajista on kyse
- Kertoo kudokseen tai elimeen kohdistuneen säteilyn biologisen vaikutuksen
-
Efektiivinen annos, yksikkö sievert (Sv)
- Ekvivalenttiannosten kudosten painokertoimilla painotettu summa
- Ilmoittaa kehoon kohdistuneen säteilyn määrän
Säteily ympäristössä
- Ihminen altistuu säteilylle koko ajan
- Suurin osa säteilystä tulee maaperän radonista
- Säteilyä tulee myös avaruudesta
- Lääketieteessä käytetään isotooppikuvauksissa -aktiivisia ytimiä merkkiaineina (Tc-199, F-18, I-123)
- Tyypillinen säteilytyyppi on kuvantamisessa käytetty röntgensäteily
- Ihmisen oma radioaktiivisuus: K-40 (luusto), Cs-137 ja Sr-90 (ruoan mukana, Tšernobyl)
- Sisäisellä säteilyllä tarkoitetaan elimistöön joutunutta säteilyä
- Säteily kulkeutuu elimistöön hengityksen tai ruoan mukana
Säteily ympäristössä
- Säteilyturvakeskus (STUK) valvoo Suomessa esiintyvää säteilyä ja vastaa kaikkiin säteilyyn liittyviin kysymyksiin
- Muuta käyttöä:
- Teollisuudessa käytetään apuna säteilyn vaimenemista kappaleita tutkittaessa
- Palovaroittimen toiminta: Am-241 alfa-lähde
- Säteilyltä voidaan suojautua:
- Vähentämällä oleskeluaikaa säteilylähteen läheisyydessä
- Lisäämällä etäisyyttä
- Käyttämällä suojia
- Varomalla kontaminaatiota
- (Jodin käyttö lääkkeenä säteilyonnettomuuden yhteydessä, jodin kertyminen kilpirauhaseen)
Aineen ja säteilyn kertaus (FY08)
By pauliinak
Aineen ja säteilyn kertaus (FY08)
FY10 Kertausta ylioppilaskokeeseen
- 445



