Lämpöopin kertaus (FY03)
FY10 Kertausta abiturienteille
Keskeiset käsitteet
- Termodynaamiset systeemit
- Makro- ja mikrotaso
- Lämpölaajeneminen
- Pituus
- Tilavuus
- Paine
- Mekaaninen paine
- Ilmanpaine
- Nesteen paine
- Tilansuureet
- Tilanmuutokset suljetussa systeemissä
- Ideaalikaasu
- Lämpöenergia lämpötilan muutoksessa
- Olomuodon muutokset
- Faasikaavio
- Sisäenergia ja Joulen koe
- Termodynamiikan pääsäännöt
- Kaasun tekemä työ
- Lämpövoimakone
- Kasvihuoneilmiö ja sen voimistuminen
Keskeiset suureyhtälöt
Pituuden lämpölaajeneminen
Tilavuuden lämpölaajeneminen
Mekaaninen paine
Hydrostaattinen paine
Kokonaispaine
Suljetun kaasusysteemin tilanyhtälö
Ideaalikaasun tilanyhtälö
Keskeiset suureyhtälöt
Kappaleeseen / kappaleesta siirtyvä lämpö
Aineen sulaessa tai jähmettyessä siirtyvä lämpö
Aineen höyrystyessä tai tiivistyessä siirtyvä lämpö
Termodynamiikan 1. pääsääntö
Kaasun tekemä työ (vakiopaineessa)
Termodynaaminen systeemi
- Termodynaaminen systeemi on ympäristöstä rajattu kokonaisuus ainetta
- Systeemejä on kolmea tyyppiä
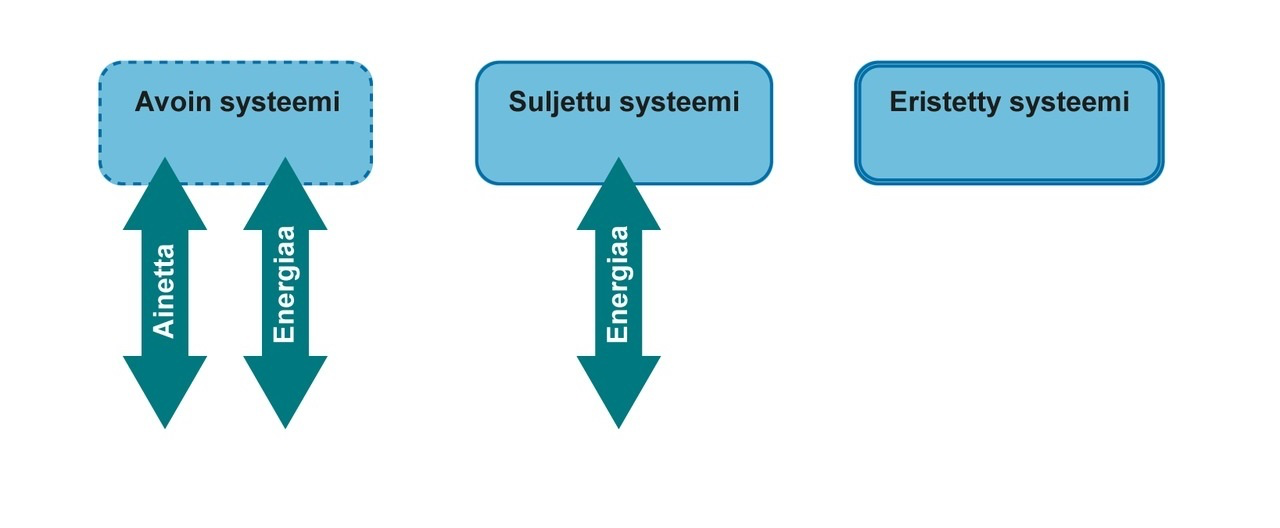
Lämpötilaerot tasoittuvat
Ideaalin systeemin lämpötila ei muutu
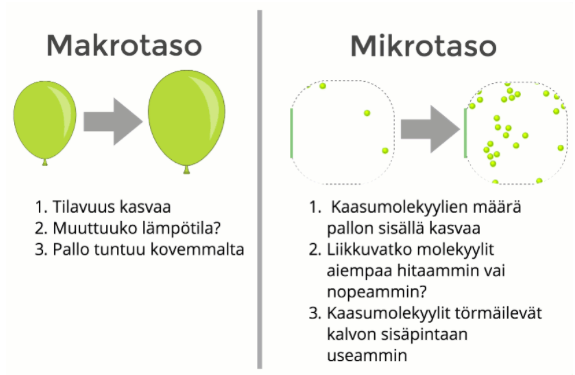
Mikro- ja makrotaso
- Systeemejä voidaan tarkastella kahdella eri tasolla
- Mikrotaso: aineen rakenneosaset (atomit tai molekyylit)
- Makrotaso: systeemi kokonaisuutena
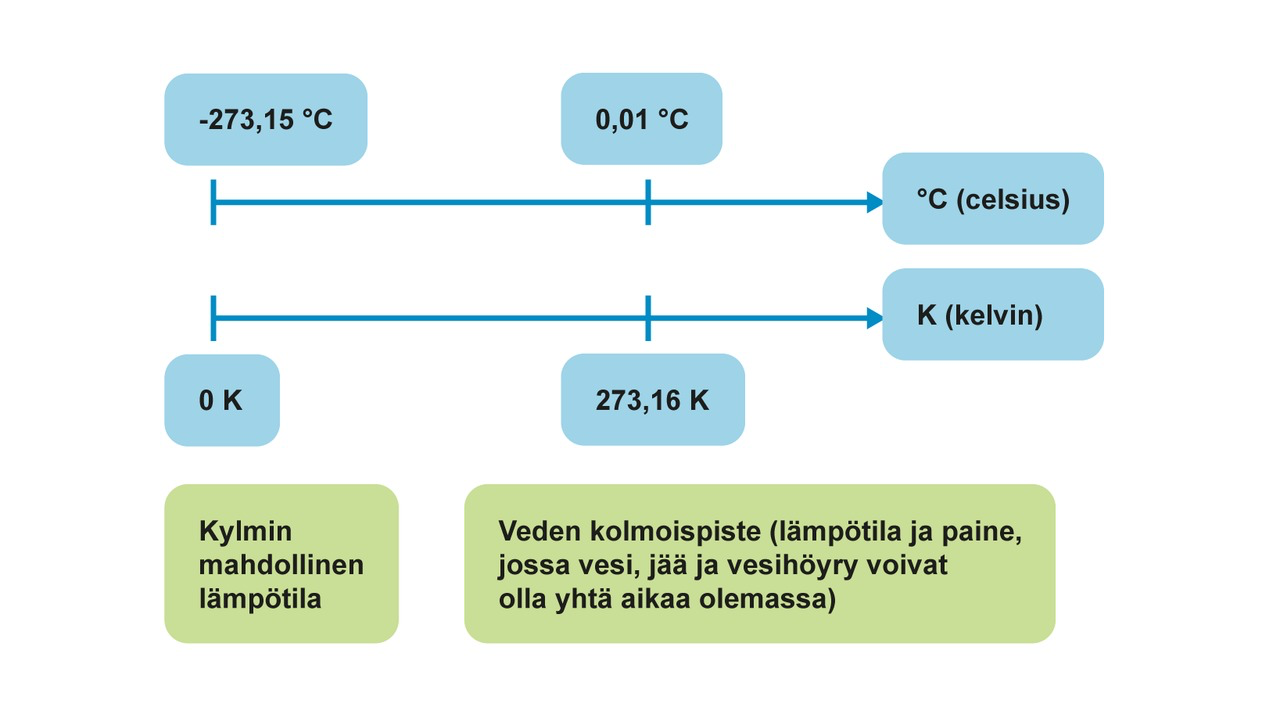
Lämpötila
- Lämpötila T on arkielämässä tuttu suure
- Ihminen kykenee aistimaan kappaleiden lämpötilaeroja
- Lämpötilan yksiköitä ovat celsius, kelvin, fahrenheit
Lämpöliike
- Lämpenemiseen tarvitaan energiaa, kun taas jäähtymisessä vapautuu energiaa
- Aineen rakenneosaset liikkuvat
- Lämpötilan noustessa aineeseen sitoutuu energiaa, joka varastoituu atomien liike-energiana
- Energian lisäys kasvattaa atomien liikettä (satunnaisesti)
-
Lämpöliike on erilaista kiinteässä aineessa kuin nesteessä ja kaasuissa
- Kiinteissä aineissa atomit värähtelevät tasapainoasemansa ympärillä
- Kaasuissa ja nesteissä rakenneosaset pääsevät kulkemaan vapaasti
Lämpöenergia
- Lämpötilaerot pyrkivät luonnostaan tasoittumaan
- Systeemit pyrkivät kohti termodynaamista tasapainoa
- Kuumasta kappaleesta siirtyy energiaa kylmempään, jolloin kuuman kappaleen lämpötila laskee ja kylmemmän nousee
- Siirtyvää lämpöenergiaa kutsutaan lämmöksi ja merkitään tunnuksella Q
- Lämmönsiirtymistapoja on kolme: johtuminen, konvektio ja säteily
- Myös olomuodon muutoksissa aine luovuttaa tai vastaanottaa lämpöä
Johtuminen
- Lämpö siirtyy aineen sisällä ilman, että aine liikkuu
- Kappaleiden koskettaessa kuumemman kappaleen hiukkaset törmäilevät rajapinnalla viileämmän kappaleen hiukkasiin
- Törmäyksessä hiukkasten liike samankaltaistuu, jolloin lämpötilaerot tasoittuvat
- Materiaalit voidaan jakaa lämmönjohteisiin ja lämmöneristeisiin sen mukaan, miten hyvin ne johtavat lämpöä


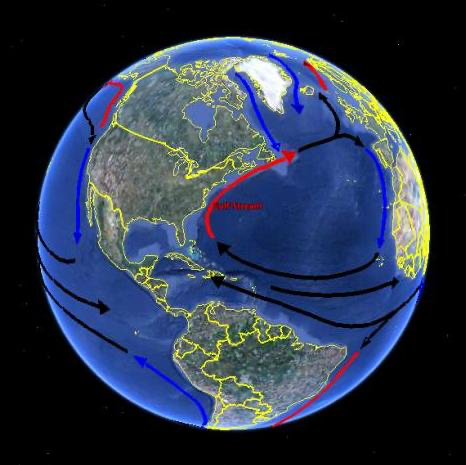
Kuljettuminen (konvektio)
- Lämpö siirtyy aineen mukana
- Kuljettumisesta käytetään myös nimitystä konvektio (tai advektio)
- Lämpötilaerojen (tiheyserojen) tasaantuminen pystysuunnassa (konvektio)
- Lämpötilaerojen tasaantuminen vaakasuunnassa (advektio)


Säteily
- Lämpö voi siirtyä kuumasta kappaleesta kylmään ilman kosketusta säteilemällä
- Kaikki kappaleet lähettävät ympäristöönsä lämpösäteilyä (infrapunasäteilyä) ja vastaanottavat samalla muiden kappaleiden säteilyä
- Lämpösäteily on valon kaltaista sähkömagneettista säteilyä (pidempi aallonpituus)



Energia lämpötilan muutoksissa
- Kappaleen lämpökapasiteetti riippuu sen massasta ja materiaalista, josta se koostuu
- Aineen kykyä varastoida lämpöä kutsutaan nimellä ominaislämpökapasiteetti c
- m-massaisen kappaleen lämmetessä lämpötilan ΔT verran siirtyy siihen lämpö
- Kappaleen jäähtyessä luovuttaa se vastaavan määrän energiaa
- Vesi sitoo energiaa hyvin eli sen ominaislämpökapasiteetti on varsin suuri
Aineen olomuodot ja niiden muutokset
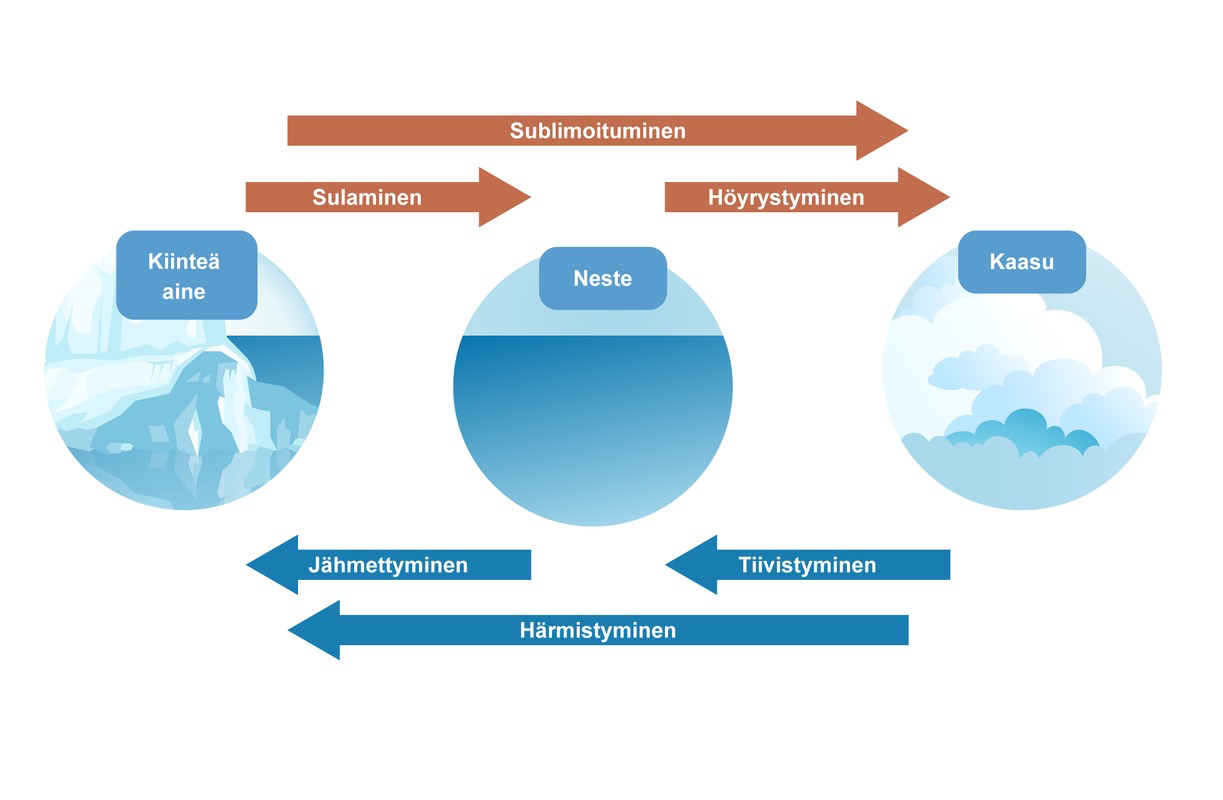
Aine vastaanottaa energiaa
Aine luovuttaa energiaa
Olomuodon muutokset
- Aineeseen siirtyvä energia aiheuttaa joko aineen lämpenemistä tai olomuodon muutoksen
- Olomuodon muutoksissa aine vastaanottaa tai luovuttaa energiaa
- Sulamiseen tai höyrystymiseen vaadittu energia riippuu aineesta
- Olomuodon muutoksen aikana aineen lämpötila ei muutu
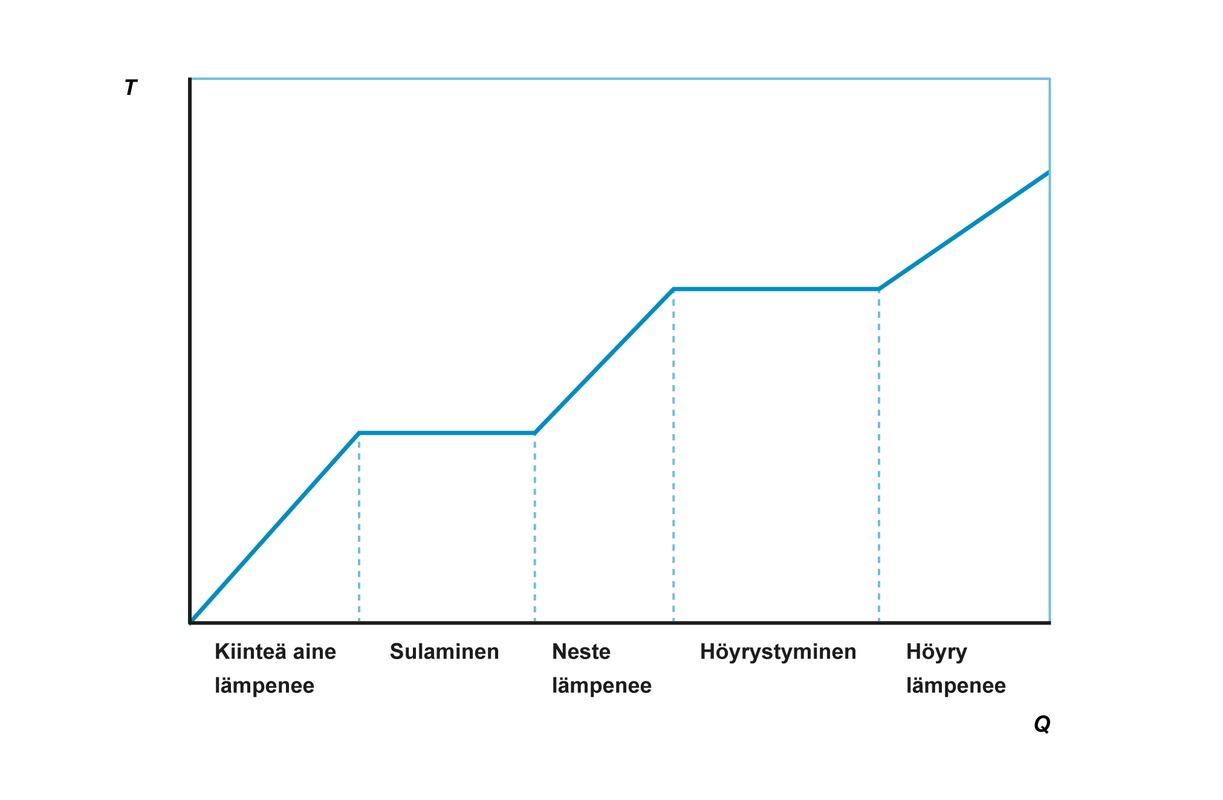
- Olomuodon muutoksen aikana energia kuluu kemiallisten sidosten muuttamiseen (latentti lämpö)
Energia olomuodon muutoksissa
- Sulaessaan aine vastaanottaa ympäristöltään lämmön
- Jähmettyessään aine luovuttaa ympäristöön vastaavan lämmön
- Höyrystyessään aine vastaanottaa ympäristöltään lämmön
- Tiivistyessään aine luovuttaa ympäristöön vastaavan lämmön
Lämpölaskujen periaatteita
- Eristettyä systeemiä voidaan kuvata yhtälöllä
- Siirtyvää lämpöä laskettaessa lämpötilan muutos lasketaan alkulämpötilan ja loppulämpötilan erotuksena
-
Suuremmasta lämpötilan arvosta vähennetään pienempi, jolloin lämpötilan muutos on aina positiivinen
- Siirtyvät lämmöt ovat näin ollen aina suuruudeltaan positiivisia
-
Laskuissa käytetään lämpötilan yksikkönä joko celsius- tai kelvinasteita
- Lämpötilan muutos on yhtä suuri molemmissa asteikoissa
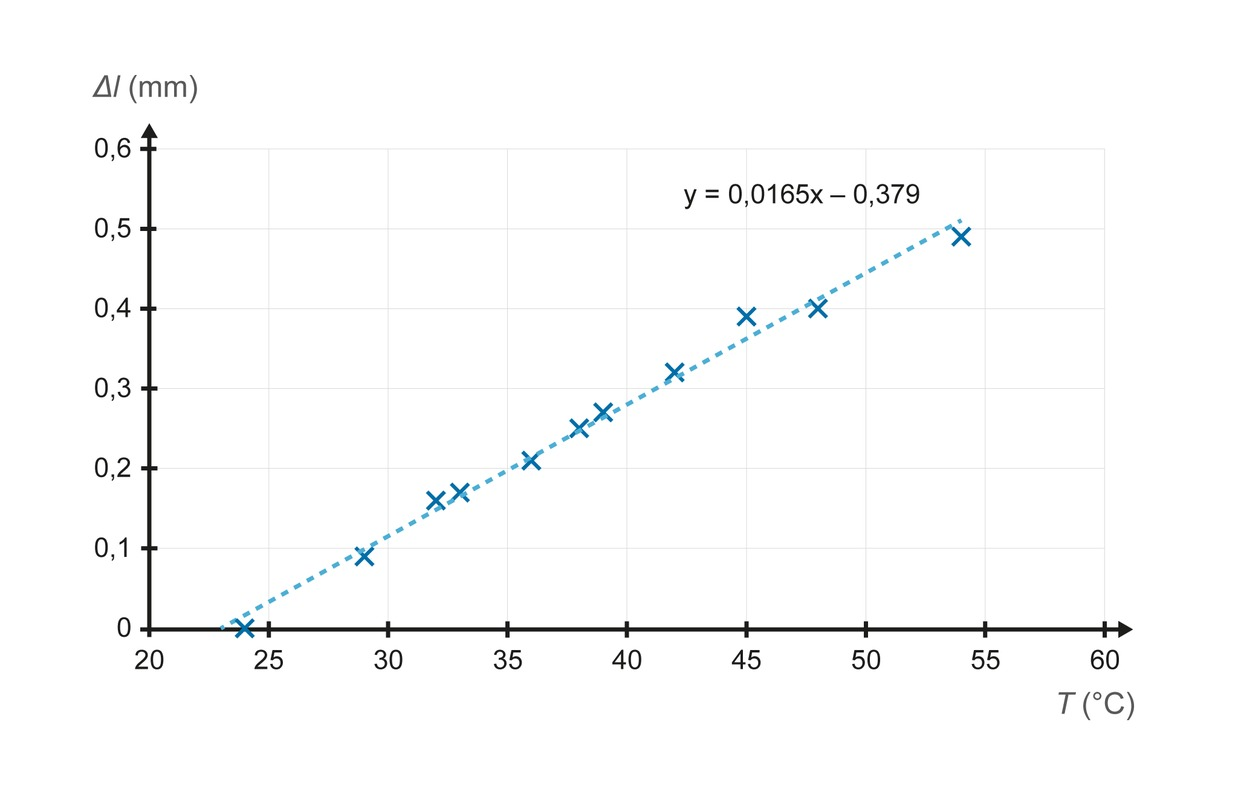
Pituuden lämpölaajeneminen
- Lämpölaajenemista voidaan tutkia kuvan laitteistolla
- Putki näyttää pitenevän tasaisesti lämpötilan noustessa
- Pituuden lämpölaajenemiselle saadaan matemaattinen malli

Tilavuuden lämpölaajeneminen
- Pinta-ala lasketaan kahden pituuden avulla (kaksi suuntaa)
- Tilavuus lasketaan kolmen pituuden avulla (kolme suuntaa)
- Jokainen suunnista lämpölaajenee!
- Nesteet mukautuvat laajetessaan astian muotoon
- Jos astia ei lämpölaajene tarpeeksi, nesteen voi valua astiasta yli tai rikkoutua
- Kaasut lämpölaajenevat voimakkaasti lämmetessään
- Niitä voi myös puristaa kasaan, joten tilanne on monimutkaisempi
- Ratkaistaan tilanyhtälöiden avulla

Huomaa, että lämpötilakerroin ei välttämättä pysy vakiona!
Lämpölaajenemisen mallia ei voi siis käyttää kaikissa tilanteissa.
Ei ole lineaarinen riippuvuus!
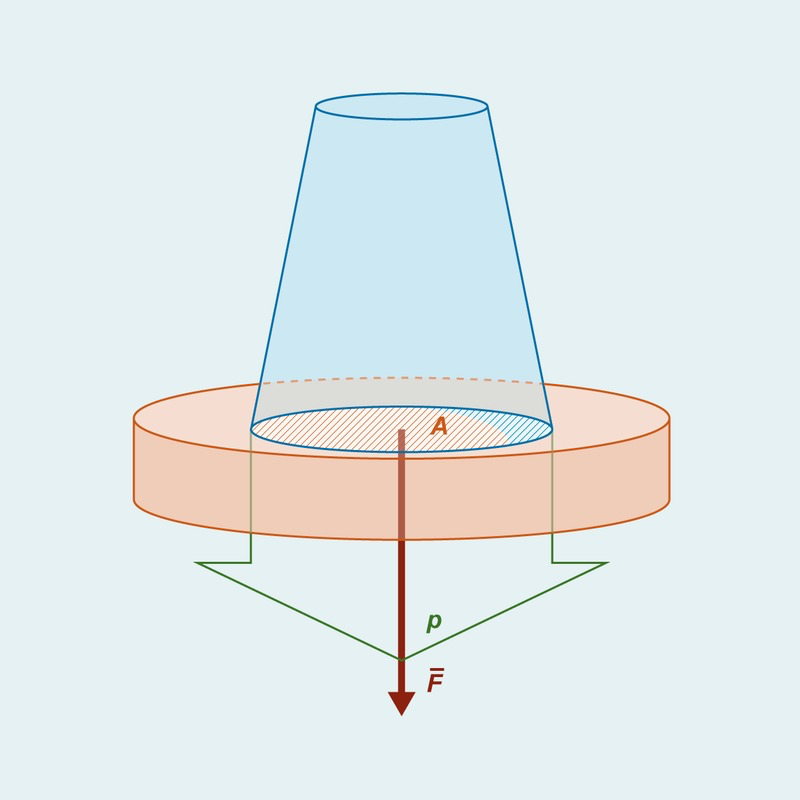
Mekaaninen paine
- Kun kahta kappaletta painetaan vastakkain, kosketuspinnan suuruus vaikuttaa tulokseen
- Sama voima saa aikaan suuremman muodonmuutoksen (tai esim. tuntoaistimuksen), jos kosketuspinta on pieni
- Ilmiötä kutsutaan paineeksi
Kaasun paine
- Suljetussa astiassa kaasumolekyylit törmäilevät astian seiniin ja kohdistavat astian pintaan paineen (mikrotaso)
- Kaasu levittäytyy tasaisesti säiliön sisällä
- Kaikkialla säiliössä ja täten myös kaasussa vallitsee sama paine
- Voidaan puhua kaasupullon sisällä olevasta paineesta
- Makrotasolla kaasu kohdistaa voiman säiliön seiniin
- Kaasun paine voidaan määritellä samalla tavalla kuin mekaaninen paine
Paine-erovoima
- Säiliön seinämien eri puolilla voi olla eri paine
- Tällöin säiliön seinämään kohdistuu sisä- ja ulkopuolelta eri suuret voimat
- Paine-eroista voidaan laskea säiliön seinämän kohdistuva kokonaisvoima

Paine-erot
- Paine-erot pyrkivät aina tasoittumaan
- Kaasuhiukkaset pyrkivät liikkumaan siihen suuntaan, missä vallitsee pienempi paine
- Jos paine on suurempi tai matalampi kuin ympäristössään, voidaan puhua yli- tai alipaineesta
- Sääilmiöiden yhteydessä myös korkea- ja matalapaineesta
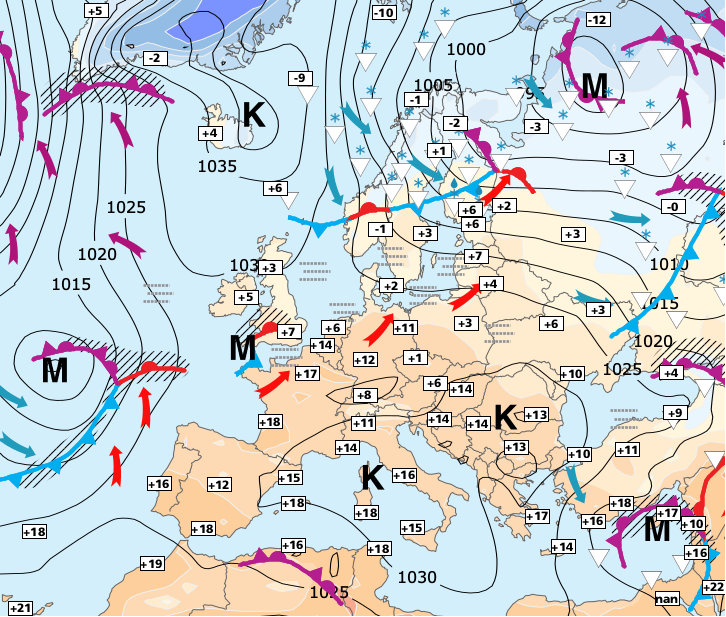
Kuva: Ilmatieteen laitos

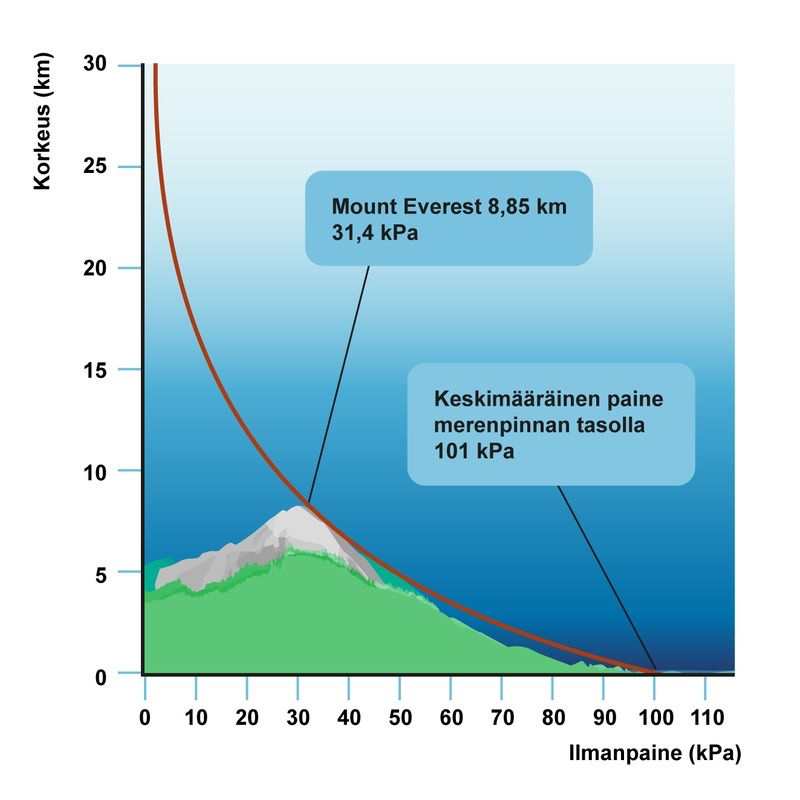
Ilmanpaine
- Ilma painaa maata painollaan ja aiheuttaa paineen
- Normaalipaine 101 325 Pa (1013,25 hPa)
- Pienenee ylöspäin noustessa (vähemmän ilmaa yläpuolella)
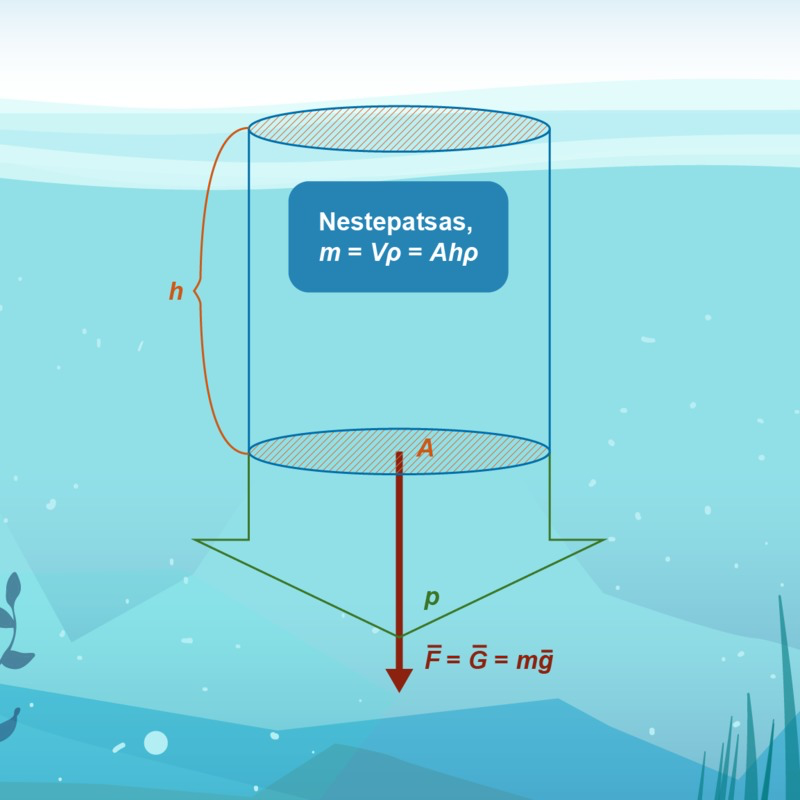
Nesteen paine
- Paine nesteessä kasvaa tasaisesti syvemmälle mentäessä
- Hydrostaattinen paine on
Kokonaispaine
- Jos sekä ilmanpaine että hydrostaattinen paine huomioidaan, voidaan laskea kappaleeseen kohdistuva kokonaispaine syvyydellä h
- Kokonaispaine p on
Kaasujen tila ja tilanmuutokset
- Verrattuna kiinteään aineeseen tai nesteeseen kaasu on aineen olomuotona erittäin harva ja käyttäytyy tästä johtuen eri tavoin
-
Suljetussa systeemissä kaasun tila riippuu tilanmuuttujista
- Paineesta p
- Lämpötilasta T
- Tilavuudesta V
- Yhden tilanmuuttujan arvon muuttuessa vähintään yhden muun tilanmuuttujan arvo muuttuu
Isokoorinen prosessi
- Muutosprosessia vakiotilavuudessa kutsutaan isokooriseksi prosessiksi
- Suljetun systeemin tilavuuden V ollessa vakio kaasun paineen p ja absoluuttisen lämpötilan T suhde on vakio
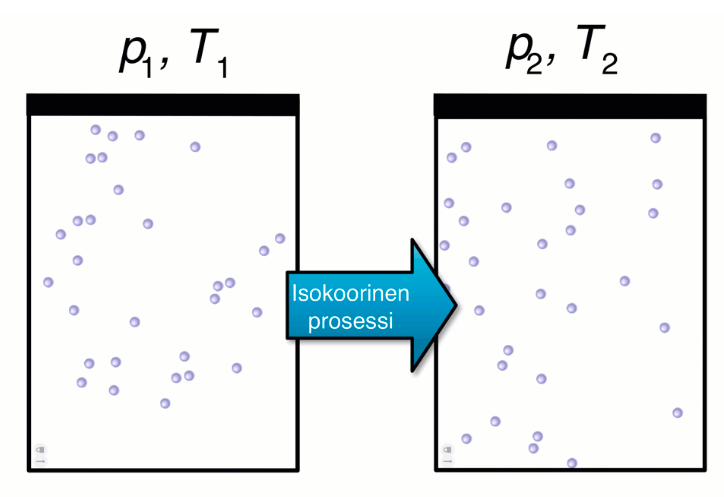
Laskuissa lämpötila aina kelvineinä!
Isobaarinen prosessi
- Kaasun tilanmuutosta vakiopaineessa kutsutaan isobaariseksi prosessiksi
- Paineen p ollessa vakio kaasun tilavuuden V ja absoluuttisen lämpötilan T suhde on vakio suljetussa systeemissä
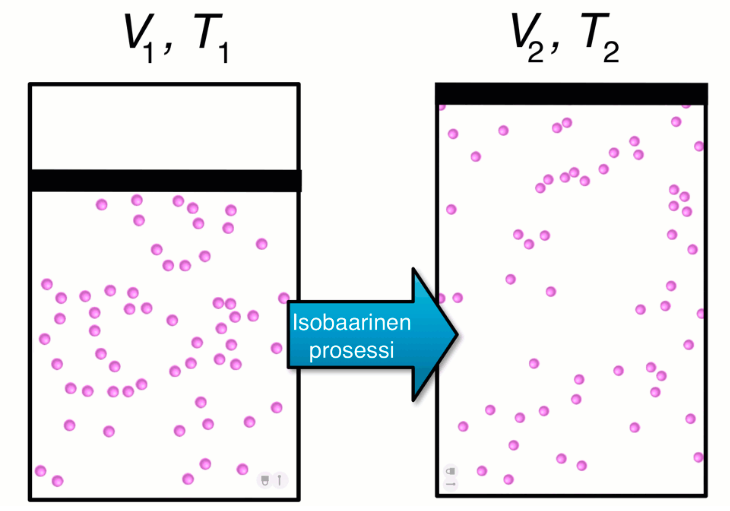
Laskuissa lämpötila aina kelvineinä!
Isoterminen prosessi
- Tilanmuutosta vakiolämpötilassa kutsutaan isotermiseksi prosessiksi
- Lämpötilan T ollessa vakio suljetussa systeemissä kaasun paineen p ja tilavuuden V tulo on vakio
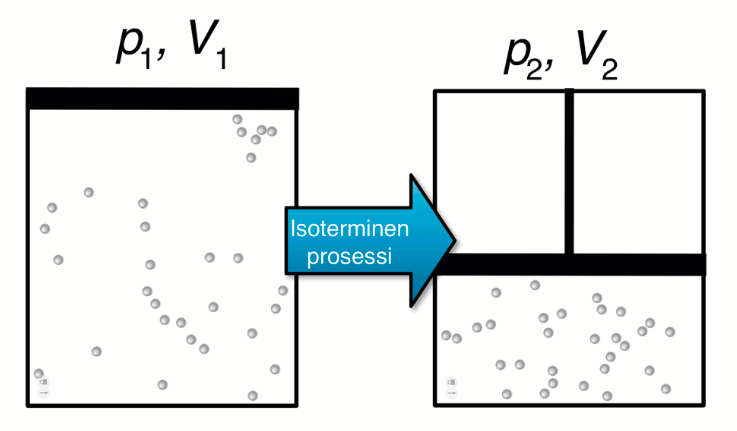
Suljetun kaasusysteemin tilanyhtälö
-
Kaasujen tilanyhtälöt käsittelevät ainoastaan kaasun alkutilannetta ja lopputilannetta
- Niiden välinen prosessi voi olla millainen tahansa
- Suljetussa systeemissä kaasun paineella p, tilavuudella V ja absoluuttisella lämpötilalla T on voimassa seuraava riippuvuus
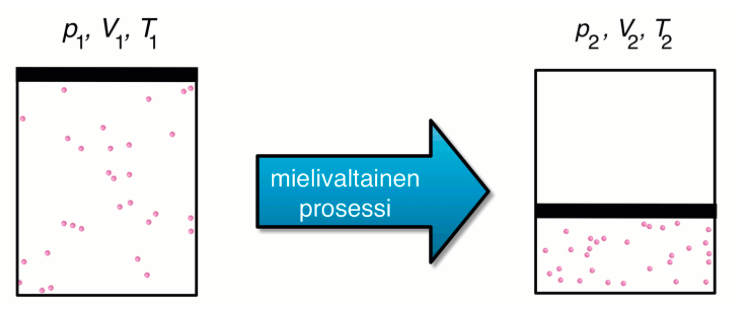
Laskuissa lämpötila aina kelvineinä!
Yleinen ideaalikaasun tilanyhtälö
- Avogadron lain mukaan kaasun tilavuus on suoraan verrannollinen ainemäärään, joten
- Tämä vakio on sama kaikille kaasusysteemeille, sitä kutsutaan yleiseksi kaasuvakioksi (moolinen kaasuvakio)
- Paineen, tilavuuden, lämpötilan ja ainemäärän välinen riippuvuus on nimeltään kaasun yleinen tilanyhtälö
Laskuissa lämpötila aina kelvineinä!
Ideaalikaasu reaalikaasun mallina
- Edellä johdettu kaasuyhtälö pätee vain reaalikaasun mallille, ideaalikaasulle
- Ympäristössä olevat kaasut ovat reaalikaasuja
- Ideaalikaasu on reaalikaasun yksinkertaistus
- Normaaliolosuhteissa (NTP) tai niiden läheisyydessä monia kaasuja voidaan tarkastella ideaalikaasuina
- Ideaalikaasun kaasumolekyylit
- ovat keskenään samanlaisia
- ovat pistemäisiä
- liikkuvat täysin satunnaisiin suuntiin (lämpöliike)
- törmäilevät kimmoisasti (eivät takerru toisiinsa)
- eivät vuorovaikuta toisiinsa muutoin kuin törmäämällä
- liikkuvat törmäysten välillä tasaisella nopeudella ja suoraviivaisesti
- Kaasut noudattavat ideaalikaasun mallia parhaiten normaaliolosuhteita korkeammassa lämpötilassa ja alhaisemmassa paineessa
Faasikaavio
- Aineen sulamis- ja höyrystymislämpötila riippuu paineesta
- Olomuodon riippuvuutta sekä lämpötilasta että paineesta voidaan kuvata faasikaaviolla
- Olomuodot omina alueinaan
- Käyrillä olomuoto muuttuu
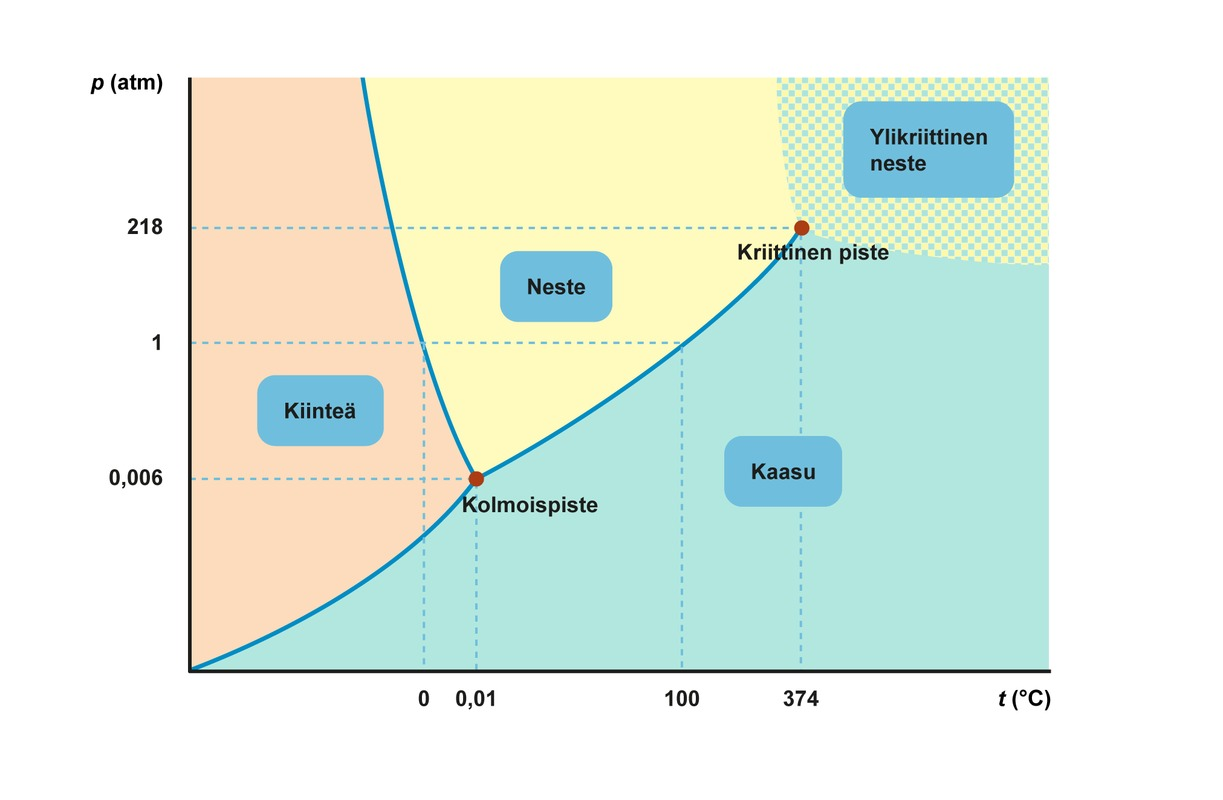
Veden faasikaavio
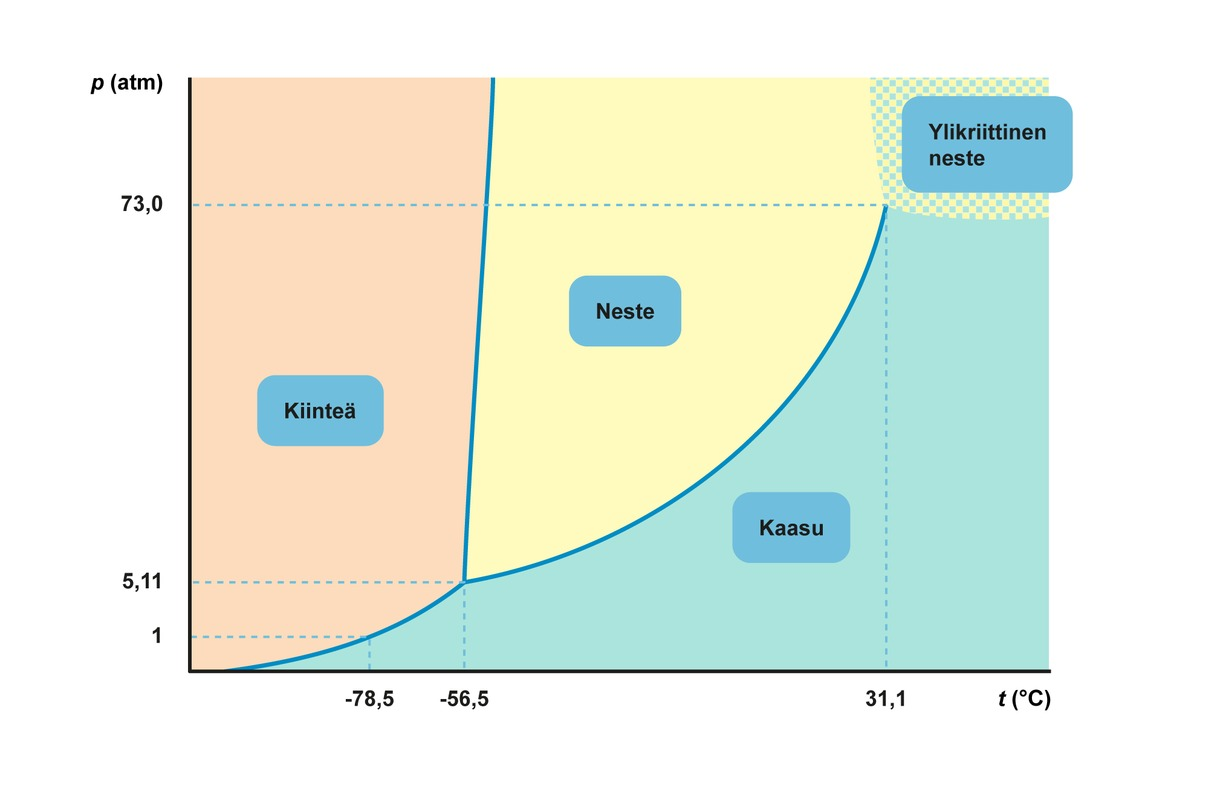
Hiilidioksidin faasikaavio
Paine yksikössä atm eli ilmakehän paine
Kriittinen piste ja kolmoispiste
-
Kriittinen piste on piste, johon nesteen ja kaasun välinen raja päättyy
- Tätä korkeammassa lämpötilassa kaasu ei nesteydy painetta kasvattamalla
- Kriittistä pistettä alemmassa lämpötilassa kaasua kutsutaan höyryksi
- Kiinteän, nesteen ja kaasun faasirajat kohtaavat kolmoispisteessä
- Kolmoispisteen lämpötilassa ja paineessa aine voi esiintyä jokaisessa olomuodossa yhtä aikaa
- Veden kolmoispiste on 273,16 K (0,01 °C)

Vuorovaikutus ja lämpö
- Energian säilymislaki: Energiaa ei voi koskaan hävitä tai syntyä, mutta se muuttaa muotoaan
- Mekaaninen energia (liike- ja potentiaalienergia) ja lämpö ovat energian lajeja, jotka voivat muuttua toisikseen
- Voiman vaikutuksesta siirtyvää energiaa kutsutaan mekaaniseksi työksi
- Sisäenergian suurentuminen nostaa kappaleen lämpötilaa
- Esim. liukuvan kappaleen liike-energiaa muuttuu pintoihin siirtyväksi lämmöksi (kitka)

Energiaperiaate
- Mekaanisen energian muuntuminen lämmöksi on yleinen ilmiö
- Muutkin energian muodot muuntuvat usein lämmöksi
- Energiaperiaate, joka kuvaa lämmön ja mekaanisen energian yhteyttä, voidaan muotoilla
E on systeemin mekaaninen energia alussa tai lopussa, W on systeemiin tehty työ ja Q siihen siirtynyt lämpö
Termodynamiikan pääsäännöt
- Termodynamiikan 0. pääsääntö: tasapaino
- Eristetyssä systeemissä eri lämpöiset kappaleet asettuvat lopulta samaan lämpötilaan
- Termodynamiikan 1. pääsääntö: energian säilyminen
- Energiaa ei voida luoda eikä hävittää, vain muuttaa muodosta toiseen
- Sisäenergian muutos ΔU on systeemiin tuodun energian määrä
- Termodynamiikan 2. pääsääntö: entropian kasvu
- Kaikki ajautuu järjestyksestä epäjärjestykseen (entropia eli epäjärjestys kasvaa)
- Termodynamiikan 3. pääsääntö: entropian nollapiste
- Täydellisen kiteen entropia on nolla
- Kaikki toiminta lakkaa absoluuttisessa nollapisteessä
Termodynamiikan 1. pääsääntö
-
Systeemiin siirtynyt energia kasvattaa sen sisäenergiaa
- Energia voi siirtyä lämpönä (säteily, johtuminen, kuljettuminen) tai mekaanisen työn kautta (systeemiin kohdistuva voima)
- Sisäenergian muutos havaitaan systeemin lämpötilan nousuna tai olomuodon muutoksena
- Termodynamiikan 1. pääsääntö:
- Merkkisäännöt:
- Systeemiin siirtyvä lämpö ja systeemiin tehty työ ovat positiivisia eli Q > 0 ja W > 0
- Systeemistä pois siirtyvät lämpö ja ympäristöön tehty työ ovat negatiivisia
- Sisäenergian kasvaessa sen muutos on positiivinen eli ΔU > 0
Kaasun tilavuuden muutostyö
- Kun kaasua puristetaan hitaasti kasaan, kaasun lämpötila pysyy vakiona (isoterminen prosessi: pV = vakio)
- Kun kaasua puristetaan nopeasti kasaan, kaasun lämpötila ei ehdi tasaantua ympäristön kanssa
- Kaasu lämpenee voimakkaasti
- Sylinterin mäntää puristava voima tekee työtä
- Vakiopaineessa mäntää puristavan voiman tekemä työ on
- Kaasun tilavuuden kasvaessa kaasu tekee samansuuruisen työn ympäristöön
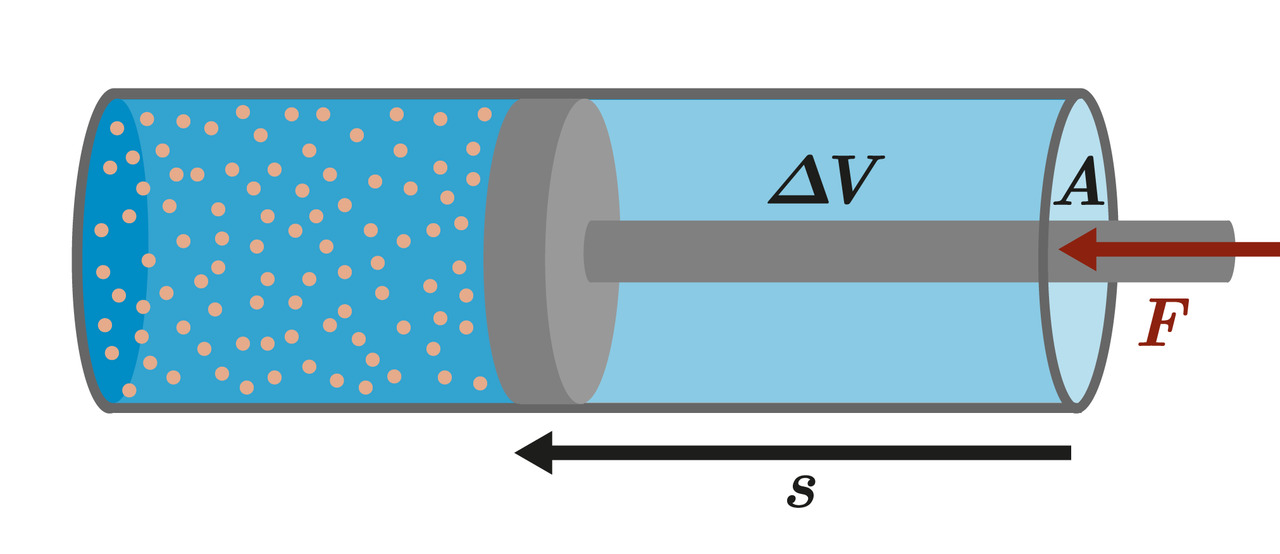
1. pääsääntö kaasua puristettaessa
- Isotermisessä tilavuuden muutoksessa kaasun lämpötila ei muutu
- Kaasun sisäenergia ei muutu
- Kaasusta siirtyy tehdyn työn verran lämpöä ympäristöön
- Nopeassa tilavuuden muutoksessa kaasun lämpötila kasvaa
- Osa tehdystä työstä muuttuu kaasun sisäenergiaksi
-
Adiabaattisessa tilanmuutoksessa lämpöä ei siirry lainkaan systeemistä ympäristöön
- Erikoistapaus, monet ilmakehän prosessit adiabaattisia
| Isoterminen puristaminen | Adiabaattinen puristaminen | |
|---|---|---|
| Työ W | Voima tekee kaasuun työtä, W > 0 | Voima tekee kaasuun työtä, W > 0 |
| Lämpö Q | Lämpöä siirtyy kaasusta ympäristöön, Q < 0 | Lämpöä ei siirry, Q = 0 |
| Sisäenergian muutos | Lämpötila ja sisäenergia eivät muutu, W + Q = 0 | Lämpötila nousee, sisäenergia kasvaa |
Kaasuprosessit (V, p)-koordinaatistossa
- Isotermisessä prosessissa pV = vakio eli
- Kuvaaja on hyperbeli
- Vakion arvo riippuu lämpötilasta
- Sama esitystapa soveltuu myös muihin prosesseihin
- Kaasun alkutilaa edustaa yksi piste (V, p)-koordinaatistossa ja lopputilaa toinen piste
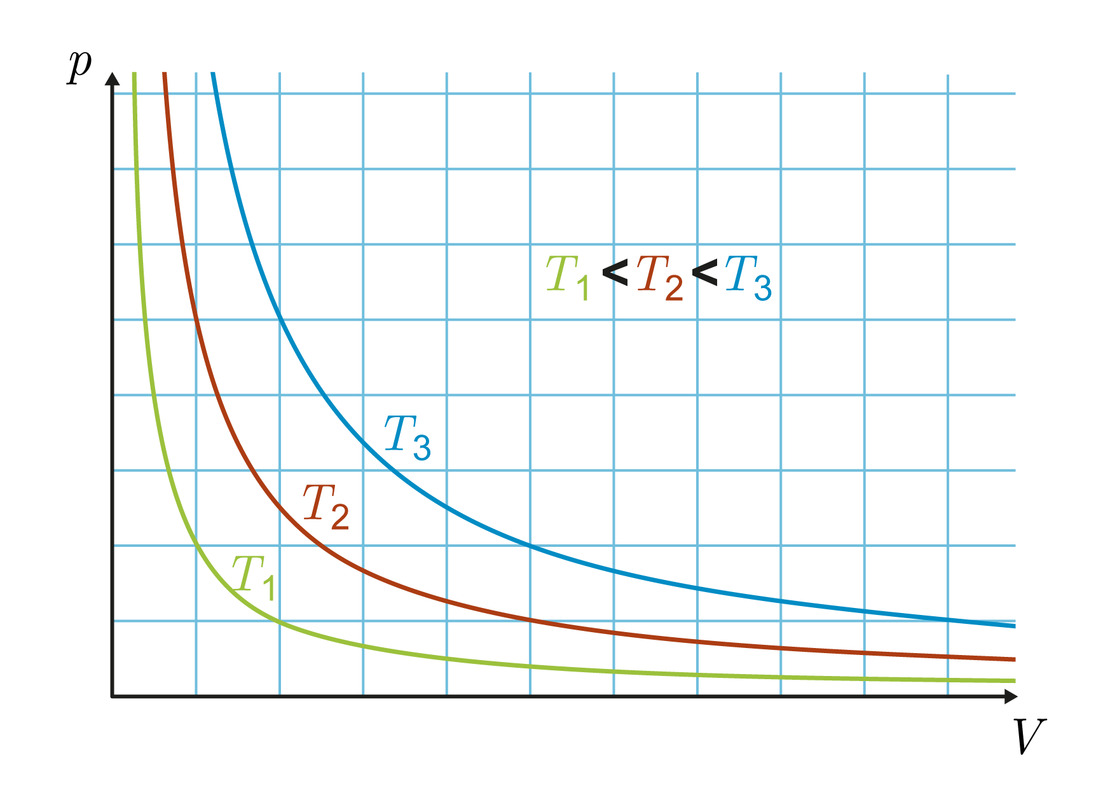
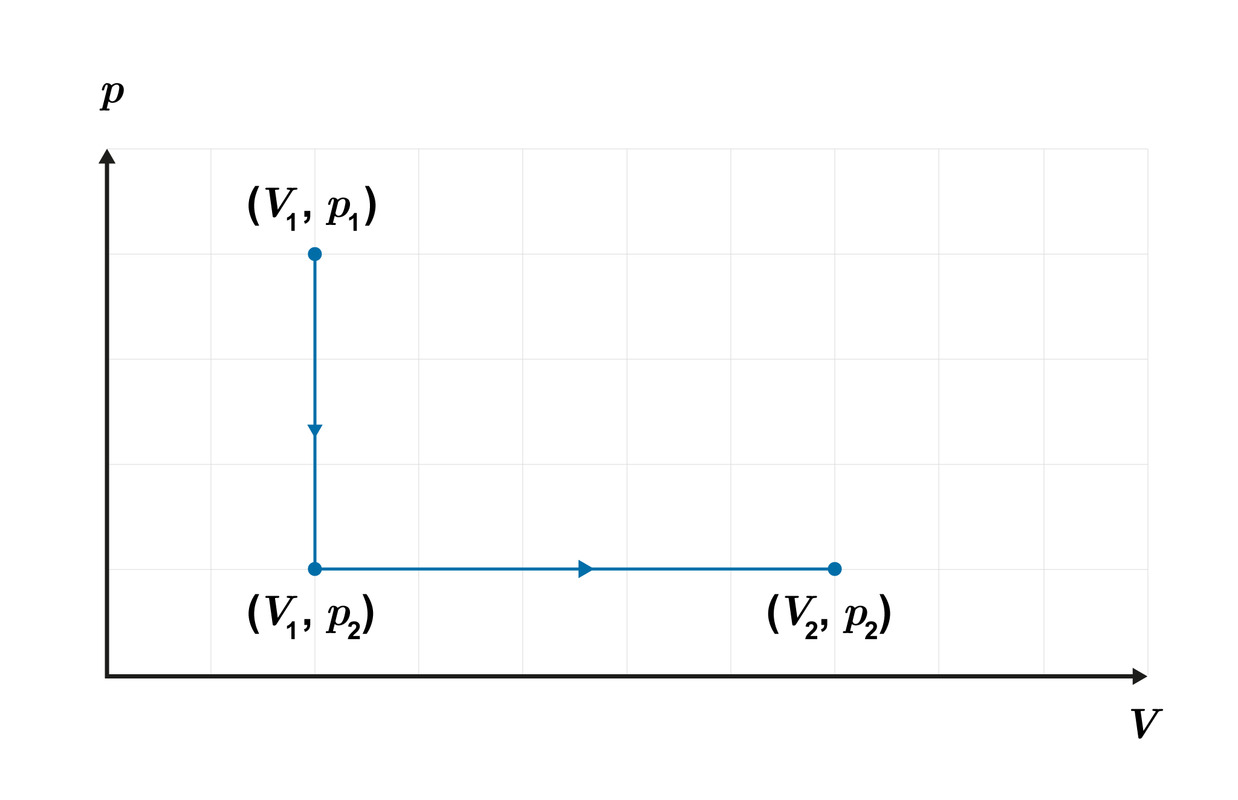
Isokoorinen prosessi
Isobaarinen prosessi
lämpötila laskee
lämpötila nousee
Carnot'n kierto
- Sadi Carnot'n vuonna 1824 keksimä idealisaatio lämpövoimakoneesta, jonka hyötysuhde on mahdollisimman suuri
1-2: Kaasu laajenee isotermisesti, sitoo lämpöä itseensä (W < 0, Q > 0)
2-3: Kaasu laajenee adiabaattisesti, lämpötila laskee (W < 0, Q = 0)
3-4: Kaasu puristuu isotermisesti, luovuttaa lämpöä (W > 0, Q < 0)
4-1: Kaasu puristuu adiabaattisesti, lämpötila nousee (W > 0, Q = 0)
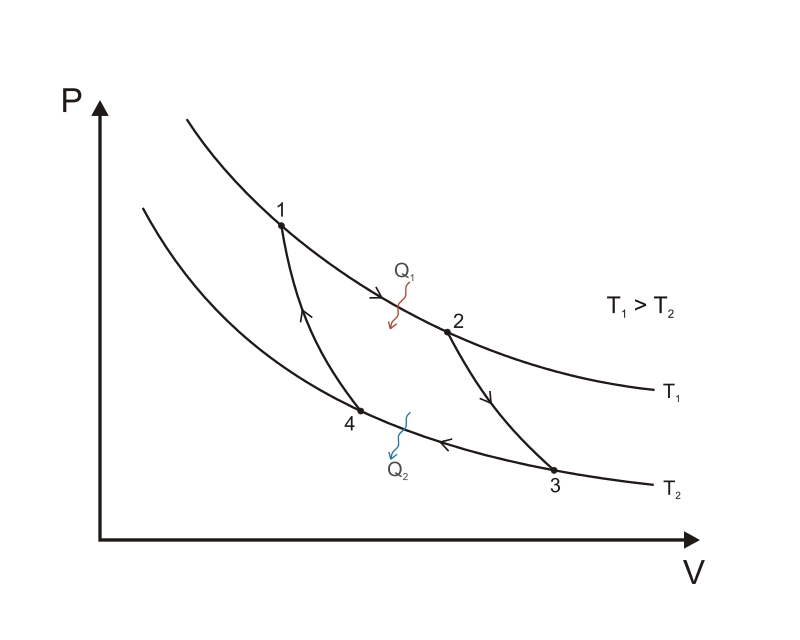
Kuva: Wikipedia
Lämpö energiamuotona
-
Lämpöenergia on energian hyödyttömin muoto
- Sitä voidaan muuttaa työksi vain lämpötilaeroja hyödyntämällä aine virtaa kuumasta kylmään lämpöenergia muuttuu liike-energiaksi
- Ilman lämpötilaeroja ei lämpöenergiaa voi hyödyntää
- Maailmankaikkeus siirtyy kohti tilaa, jossa lämpötila on kaikkialla sama (lämpökuolema)
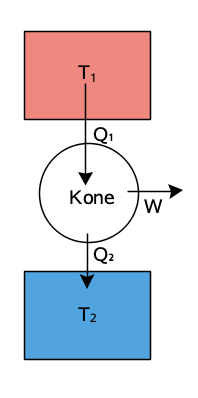
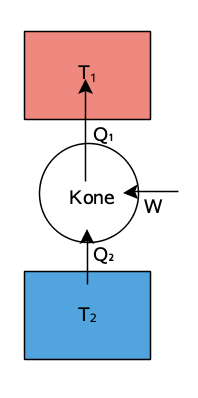
Lämpövoimakone:
lämpöenergiaa siirtyy kuumasta kylmään, osa energiasta muuttuu työksi
Jäähdytin:
tekemällä työtä energiaa voidaan siirtää kylmästä kuumaan
Lämpövoimakone
- Laite, joka tuottaa lämmöstä mekaanista energiaa
- Useimmiten hyödynnetään laajenevan kaasun tekemää työtä
- Kaasua lämmitetään, se laajenee ja tekee työtä
- Kaasun sisäenergia muuttuu mekaaniseksi energiaksi
- Mekaanisella energialla voidaan työntää mäntää tai pyörittää turbiinia
- Laajetessaan jäähtynyt kaasu ohjataan uudelleen lämmitettäväksi
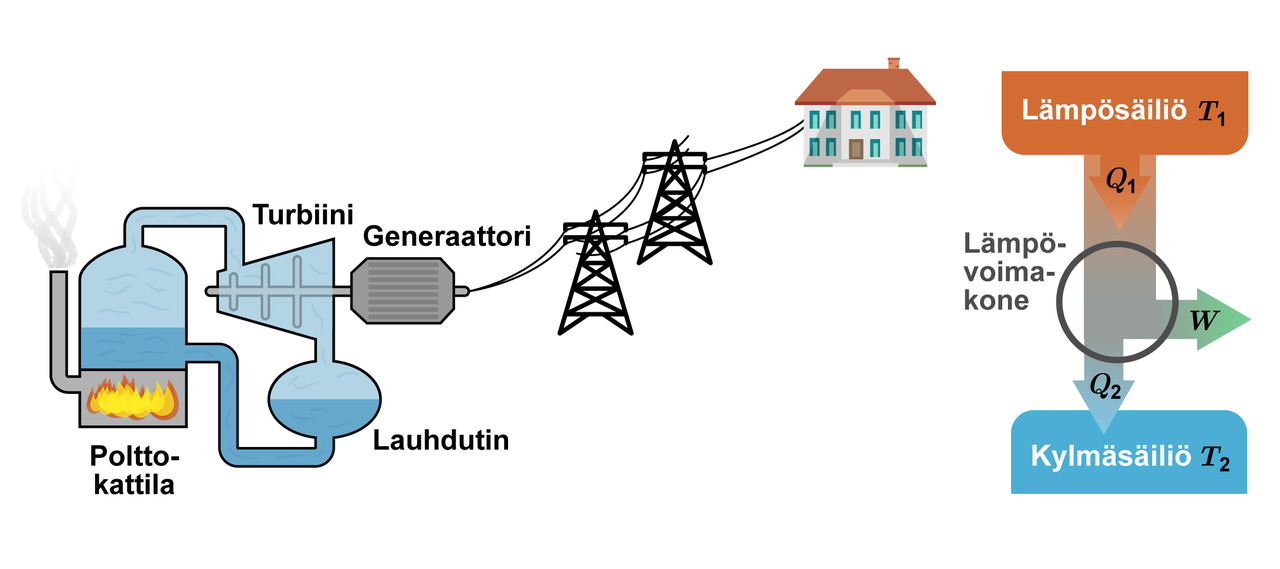
Yläraja noin 60 %
Hyötysuhde:
Jäähdytyskone
- Laite, joka siirtää lämpöä kylmäsäiliöstä lämpösäiliöön
- Lämmön siirtämiseksi pitää tehdä työtä
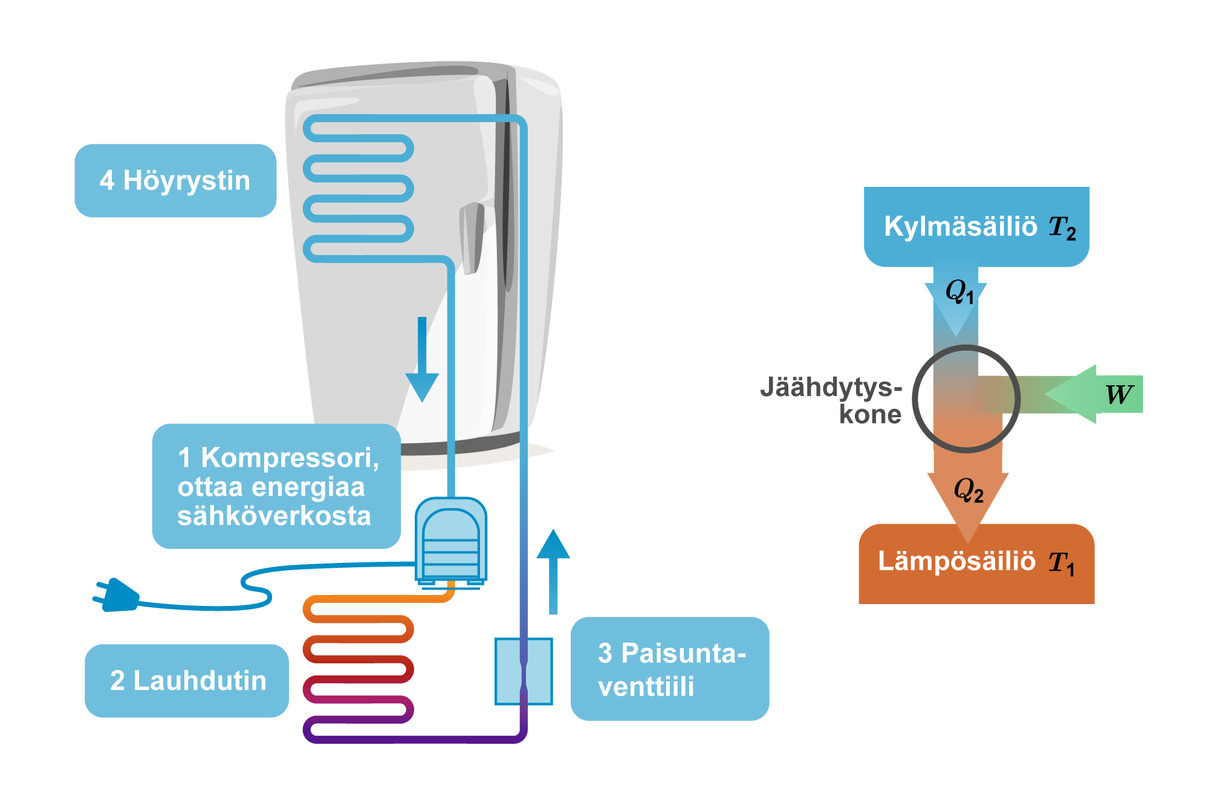
- Jäähdytys perustuu pakotettuihin olomuodon muutoksiin
- Jäähdytysnesteen paineen aleneminen paisuntaventtiilissä (3) saa nesteen höyrystymään
- Höyrystymisessä (4) neste ja laitteen sisäosat jäähtyvät
- Kompressorissa (1) höyry puristetaan uudestaan korkeapaineiseksi nesteeksi
- Nesteytyksessä (2) vapautuu lämpöä, lämpö siirtyy huoneilmaan laitteen takana
Ilmakehän säteilytase
- Maapallo saa energiaa imemällä (absorboimalla) Auringon näkyvää valoa
- Maapallo menettää energiaa säteilemällä (emittoimalla) infrapunasäteilyä avaruuteen
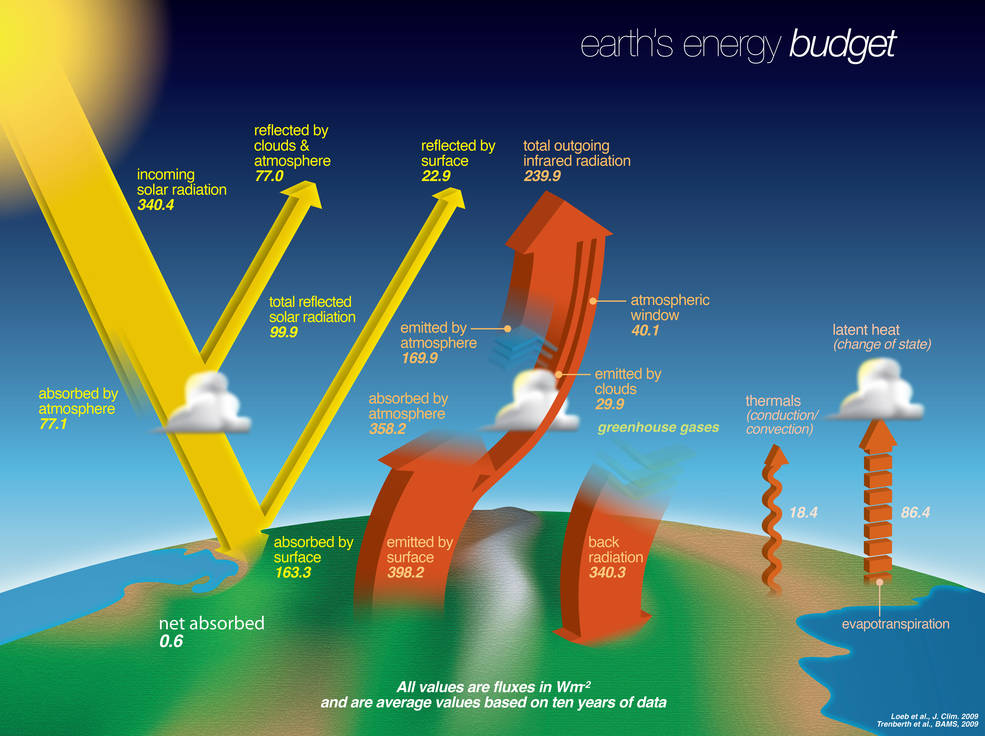
- Tasapainon vallitessa: absorboitunut Auringon säteily = emittoitunut lämpösäteily
- Todellisuus on monimutkainen
- Pitää huomioida mm. säteilyn heijastuminen, ilmakehän vastasäteily ja olomuodonmuutokset
- Avaruuteen kaikkiaan karkaava säteilymäärä on vain 60 % pinnalta lähtevästä säteilystä
Lähde: NASA
Näkyvä valo
IR-säteily
Kasvihuoneilmiö
- Jos maapallolla ei olisi ilmakehää, pinnan lämpösäteily pääsisi karkaamaan suoraan avaruuteen
- Tällöin maapallon keskilämpötila olisi noin -18 °C
- Havaittu keskilämpötila maapallon pinnalla on kuitenkin +14 °C
- Ilmakehän vaikutus on siis noin +32 astetta!
- Kasvihuoneilmiö pähkinänkuoressa: absorboitunut auringonsäteily ≠ emittoitunut lämpösäteily
- Tästä pitävät huolen kasvihuonekaasut!
- Maapallon lähettämää infrapunasäteilyä absorboituu ilmakehään
-
Kaasumolekyylit alkavat värähdellä tietyillä säteilyn aallonpituuksilla
- Värähtely lisää kaasun lämpöliikettä eli nostaa kaasun lämpötilaa
- Kaasu emittoi infrapunasäteilyä takaisin kohti maanpintaa
- Samalla lämpötila maapallon pinnalla kasvaa
Säteilyn absorptio kasvihuonekaasuihin
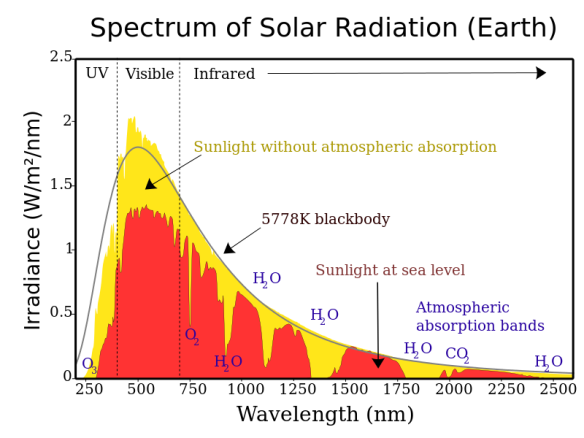
Lähde: Wikipedia
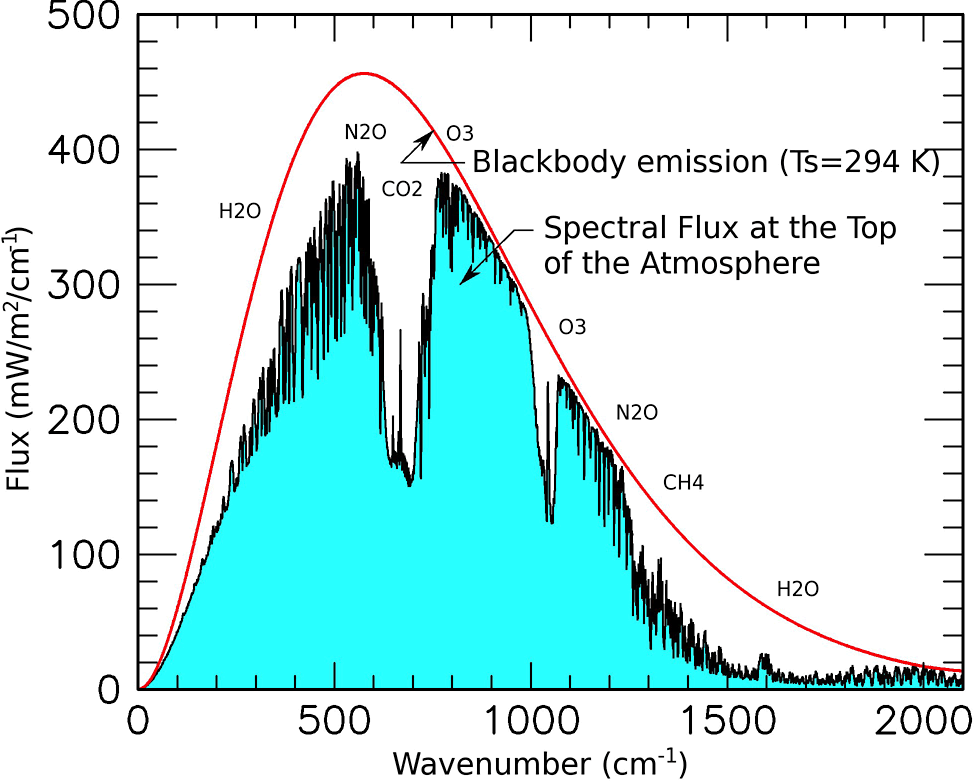
Lähde: NASA
Auringon emissiospektri
Maapallon emissiospektri
Vaaka-akselilla aaltoluku eli aallonpituuden käänteisluku
Säteilyn absorptio kasvihuonekaasuihin
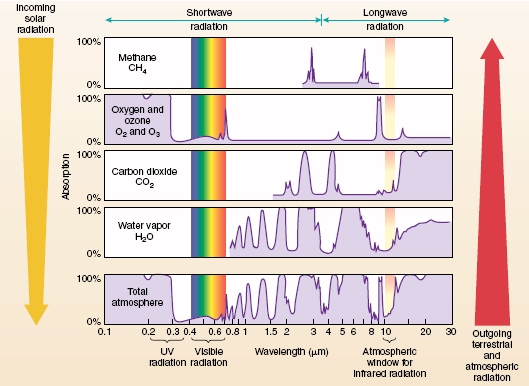
Lähde: University of Wisconsin-Madison
Kasvihuonekaasut
- Merkittävimmät kasvihuonekaasut ovat
- Vesihöyry (määrä 0,4 %, kasvihuonevaikutus 60 %)
- Hiilidioksidi (määrä 0,04 %, kasvihuonevaikutus 26 %)
- Metaani (määrä 0,000 2 %) ja ilokaasu (määrä 0,000 03 %, kasvihuonevaikutus yht. 6 %)
- Otsoni (määrä 0,000 04 %, kasvihuonevaikutus 8 %)
- Ihmisen toiminta lisää pääasiassa hiilidioksidin, metaanin ja otsonin määriä
- Vesihöyryn määrä riippuu toisaalta ilmakehän keskilämpötilasta (positiivinen takaisinkytkentä)
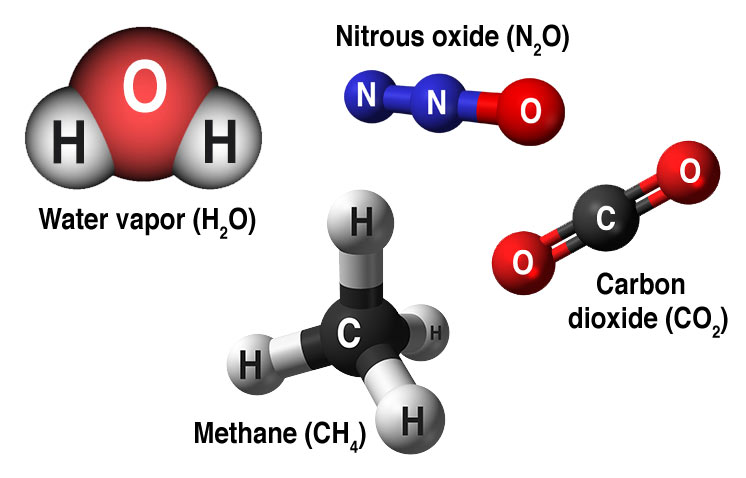
Lähde: NASA
Lämpöopin kertaus (FY03)
By pauliinak
Lämpöopin kertaus (FY03)
FY10 Kertausta ylioppilaskokeeseen
- 518



